Fターム[4C076AA11]の内容
Fターム[4C076AA11]の下位に属するFターム
Fターム[4C076AA11]に分類される特許
2,101 - 2,120 / 2,153
酸を含むオキサリプラチン製剤
経口的投与のためのオキサリプラチンの薬事用液体製剤であって、(i) オキサリプラチン; (ii) 水; 及び (iii) 酸を含み、この酸が安定化に寄与していて、マロン酸、乳酸またはシュウ酸でない製剤を提供する。さらに、癌治療のための医薬品の調製における製剤の使用および薬事用製剤の治療量を投与することを含む癌を処置する方法を提供する。 (もっと読む)
ポリペグ化されたプロテアーゼインヒビター
(i)プロテアーゼに結合して、それを阻害するKunitzドメインを含む、Kunitzドメインポリペプチド、および(ii)Kunitzドメインポリペプチドに結合した複数のポリエチレングリコール部分を含む化合物が開示される。Kunitzドメインポリペプチドの接触可能な各第一級アミンは、前記部分の一つに結合することができる。さらに、関連する方法も開示される。上記化合物は、12、14または16kDaの分子量を有する。一つの実施態様において、各非タンパク質部分の平均分子量は、3〜20kDa、3〜12kDa、3〜10kDa、3〜8kDa、4〜6kDaであり、例えば、約4、5、6、7または8kDaである。  (もっと読む)
(もっと読む)
グルカゴン様ペプチド(GLP)−1化合物またはメラノコルチン4受容体(MC4)アゴニストペプチドの経口デリバリーのための化合物、方法および製剤
本発明は、GLP−1化合物またはMC4アゴニストペプチドの経口デリバリーに有用な新規化合物、方法および製剤に関する。 (もっと読む)
尋常性ざ瘡の治療薬及び使用方法
尋常性ざ瘡の治療薬は、局所治療に提供される。本発明によれば、方法は、感染域に組成物物質を適用する段階と、感染域内に組成物を作用させる段階と、感染域から組成物を除去する段階とが提供される。組成物は、ラウロイルサルコシンナトリウムと組合せて、少なくとも1つのエトキシレートを含む。或いは、エトキシレートをメトキシレート又はプロポキシレートに置換することができる。ポリエチレンビーズのような不活性洗浄剤もまた含めることができる。アセチル化ラノリンアルコール、ラウロイルサルコシンナトリウム、EDTA、気泡安定剤、及び水もまた、作用を助けるために組成物に添加することができる。 (もっと読む)
流動性の止血用の組成物を作成する方法およびこれらの組成物を収容している装置
【課題】本発明は、流動性の止血用の組成物を作成する方法と、内部に配置されているその流動性の止血用の組成物を含んでいる装置と、に関連している。
【解決手段】流動性の止血用の組成物を形成するために、連続的な液体の相の全体に亘って実質的に均質に分散されている不連続な気体の相および固体の粒子を含んでいる実質的に均質な組成物を形成するために、所与の容積の生体適合性の液体と、所与の容積の生体適合性の気体と、所与の量の生体適合性のポリマーの固体の粒子と、が一緒に混合されている。その後、上記の組成物は、上記の液体の相の全体における気体の相および固体の粒子の実質的に均質な分散を維持するために有効な条件下において、止血を必要としている体の部位にその流動性の止血用の組成物を供給するために適している装置の中に移される。
(もっと読む)
アリピプラゾールの投与方法
本発明は、一部、ボーラス注入で投与されるアリピプラゾールおよび担体を含有する医薬組成物が、活性薬剤を含むポリラクチド−コ−グリコライドミクロスフェア製剤の注入により得られるのと同様の長期放出プロフィールを生じたという発見に関する。この驚くべき結果は、ミクロスフェアの製造に係わる複雑さと費用を伴うことなく、薬理的に有益な長期放出製剤が得られ得ることを示唆している。 (もっと読む)
火傷した皮膚を治療するための方法及び組成物
本発明は、日焼けした皮膚を治療するための方法及び組成物に関する。本発明は、日焼けした皮膚にインドメタシン及び加湿ローションの混合物を局所的に適用するための方法及び組成物を提供する。当該組成物は、実質的に30ccの加湿ローション当たり100mgのインドメタシンを有する混合物を含む。加湿ローションは、商品名Cetaphil(登録商標)で販売されており、以下の成分:精製水、グリセリン、水素化ポリイソブテン、セテアリルアルコール(及び)セテアレス-20、マカダミアナッツ油、ジメチコーン、酢酸トコフェロール、ステアロキシトリメチルシラン(及び)ステアリルアルコール、パンテノール、ファルネソール、ベンジルアルコール、フェノキシエタノール、アクリレート/C10-30アルキルアクリレートクロスポリマー、水酸化ナトリウム、及びクエン酸を含む。Cetaphil(登録商標)はあるpH及び粘度レベルを提供し、Cetaphil(登録商標)内におけるインドメタシンの安定化及び可溶化を可能にすることが理論づけられている。本発明はさらに、放射線治療及び過度の熱によって引き起こされた皮膚火傷を治療するために用いられてもよい。 (もっと読む)
アリピプラゾールおよびハロペリドールのパモ酸塩
本発明は、ハロペリドールおよびアリピプラゾールのパモ酸塩が、良好ないし優れた持続性および/または長時間放出性プロフィールをもたらすという知見に関する。したがって、本発明の一局面において、本発明は、ハロペリドールまたはアリピプラゾールのパモ酸塩を含む。好ましくは、パモ酸塩は、ハロペリドールのパモ酸塩に対する比が1:1または2:1であることを特徴とする。パモ酸塩は、針状物または緻密な結晶(例えば、図面に示したもの)などの結晶性であり得る。本発明は、さらに、ハロペリドールおよびアリピプラゾールのパモ酸塩を含有する医薬組成物を投与することを含む、処置を必要とする個体の処置方法に関する。 (もっと読む)
融合タンパク質のアフィニティ精製およびプロセッシングのための修飾されたプロテアーゼ
本発明は、高い親和性で対応するプロテアーゼと結合できるプロテアーゼプロドメインの同定を対象とする。本発明のプロテアーゼプロドメインは、第2のタンパク質と融合して、プロテアーゼプロドメイン融合タンパク質を形成する。融合タンパク質中のプロテアーゼプロドメインタンパク質の存在によって、対応するプロテアーゼと共にインキュベーションすることにより、第2のタンパク質の簡単かつ選択的な精製が可能になる。  (もっと読む)
(もっと読む)
アゼチジン誘導体を含有する半固体系
アゼチジン誘導体を含有する半固体系が開示されている。本発明は経口投与用アゼチジン誘導体の新規製剤に関する。 (もっと読む)
肝胆道系障害改善剤
本発明は、プロアントシアニジンを有効成分として含有することを特徴とする肝胆道系障害改善剤を提供する。 (もっと読む)
ベータ受容体刺激薬及び抗コリン作用薬を含有する吸入用医薬品
本発明は、ベータ2作用薬及び新規な抗コリン作用薬の塩を基礎とした新規な医薬組成物、その製造方法ならびに呼吸器疾患の治療におけるその使用に関するもので、該抗コリン作用薬は式(I)で表される。
【化1】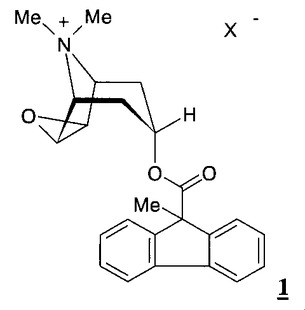
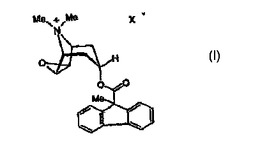 (もっと読む)
(もっと読む)
高繊維高カロリーの液状又は粉末状栄養組成物
本発明は、液状で貯蔵安定又は粉末状で再構成可能な栄養組成物に関する。この組成物の繊維含有量は、組成物100ml当り2.5g/繊維より多い。さらに、そのエネルギー含有量は、1.3〜1.8kcal/mlである。この組成物は、特に栄養不良の傾向がある老人患者において、腸管の快適性の改善及び維持、バランスの良い腸管フローラの回復に有用である。本発明はさらに、この栄養組成物を調製するプロセスに関する。 (もっと読む)
抗コリン作用薬とベータ受容体刺激薬を含む吸入用薬剤
本発明は1つ以上、好ましくは1つの抗コリン作用薬1と式2のベータ受容体刺激薬を含む新規な医薬組成物、その製法及び呼吸器系疾患の治療のための使用に関する。 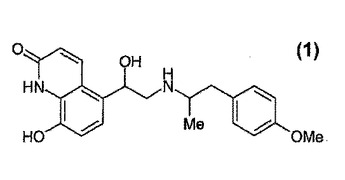 (もっと読む)
(もっと読む)
分泌促進物質の使用
本発明は、1態様において、処置が必要な個体における癌性悪液質の予防または治療のための薬剤の製造における、分泌促進物質化合物の使用を提供する。別の態様において、本発明は、個体に該薬剤の皮下用量を投与することによって、悪液質の予防または治療のための薬剤の製造における、グレリン−様化合物の使用を提供する。更なる態様において、本発明は、個体に該薬剤の皮下用量を投与することによって、個体における食欲の刺激のための薬剤の製造における、グレリン−様化合物またはその医薬的に許容し得る塩の使用を提供する。更に、本発明は、多数の新規なグレリン−様化合物、およびそれらの使用、並びに該新規なグレリン−様化合物を含有する医薬組成物および医学的なパッケージングを提供する。 (もっと読む)
抗コリン作用薬とステロイドとの併用剤及び吸入により呼吸障害を治療するためのその使用
本発明は、ステロイド及び抗コリン作用薬の塩をベースとする新規医薬組成物、それらを製造する方法及び呼吸器疾患の治療におけるそれらの使用に関する。 (もっと読む)
メルドニウム(Meldonium)塩、メルドニウム塩の調製方法、およびメルドニウム塩を主成分とする薬学的組成物
新規なメルドニウム塩、これらのメルドニウム塩を調製する方法、およびこれらのメルドニウム塩を主成分とする薬学的製剤について記載した。これらの塩の一般式はX−(CH3)3N+NHCH2CH2COOHで、その式のX−は、薬学的に受容可能な酸の中から選んだ酸のアニオンである。実際には、吸湿性がない、および/または熱的安定性が高い、および/または作用が持続する、フマル酸、リン酸、シュウ酸、マレイン酸およびパモ酸のメルドニウム水素塩、ならびにオロチン酸メルドニウムおよびガラクタル酸メルドニウムが特に適している。経口投与、非経口投与、直腸投与および経皮投与をするための、吸湿性がない、および/または熱的安定性が高い、および/または作用が持続する、3−(2,2,2−トリメチルヒドラジニウム)プロピオネートの塩を含む、新規な薬学的製剤も同じく記載している。 (もっと読む)
依存性退薬症状の治療
妊娠中の患者の薬物依存症又はオピオイド耐性患者における退薬症候群又は禁断症候群を治療するためのブプレノルフィンの投与計画が記載されている。本方法は、退薬症候群を軽減するためにブプレノルフィンの有効量の経皮投与による患者の退薬症候群又は禁断症候群を治療することを含む。例えば、第1のブプレノルフィン含有経皮剤形は、約5日以内の第1の投与期間に投与することができ;約5日以内の第2の投与期間に第2のブプレノルフィン含有経皮剤形を投与することができ、第2の剤形が、第1の剤形と同一か、又は第1の剤形よりも高用量のブプレノルフィンを含み;及び少なくとも2日間の第3の投与期間に第3のブプレノルフィン含有経皮剤形を投与することができ、第3の剤形が、第2の剤形と同一か、又は第2の剤形よりも高用量のブプレノルフィンを含む。 (もっと読む)
トリアジンを含む生理活性組成物
生理活性化合物と、以下の式(I):
または式(II):
およびそのプロトン互変異性体ならびにそれらの塩を含むトリアジン化合物とを含む組成物および方法。各R2は、独立して、いずれかの電子供与性基、電子求引性基および電子中性基から選択される。R3は、R3の環内の窒素原子を通してトリアジン基に結合された、置換された芳香族複素環、未置換の芳香族複素環、置換された複素環式環および未置換の複素環式環よりなる群から選択される。  (もっと読む)
(もっと読む)
局所適用医薬組成物
式Iの化合物は皮膚透過増強剤として有用であり、(I)式中、Rは、直鎖の飽和または不飽和、置換または非置換ヒドロカルビル基を表し、Xは、-(CO)O-、-O(CO)-、C=O、CONH、O、NHCONH、S、またはS=O基を表す。これらの化合物を用いる組成物および方法も記載する。 (もっと読む)
2,101 - 2,120 / 2,153
[ Back to top ]


