Fターム[4C085GG06]の内容
抗原、抗体含有医薬:生体内診断剤 (92,173) | 適用部位 (8,178) | 注射 (6,087) | 腹腔 (526)
Fターム[4C085GG06]に分類される特許
481 - 500 / 526
シヌクレイノパシー(synucleinopathic)およびアミロイド生成性疾患の予防および処置
本発明は、患者の脳内にあるα−シヌクレインのレビー小体など、シヌクレインが原因となる疾患に関連する疾患の治療用の改善された薬剤および方法を提供する。このような方法は、レビー小体に対する有益な免疫原性反応を誘導する薬剤を投与することを伴う。本方法はパーキンソン病の予防上および治療上の処置に特に有用である。1つの局面において、本発明は、脳におけるレビー小体またはα−シヌクレイン凝集を特徴とする疾患の予防または治療を達成する方法であって、該疾患に罹病しているか、そのリスクを有する患者に、配列番号1によって番号付けされた、ヒトα−シヌクレインの1〜20位の残基の中にあるエピトープに特異的に結合する抗体の有効な投与計画を行うことを含む方法を提供する。  (もっと読む)
(もっと読む)
RAGE融合タンパク質及び使用方法
第二の非RAGEポリペプチドと連結したRAGEポリペプチド配列を含むRAGE融合タンパク質を開示する。前記RAGE融合タンパク質は、RAGEリガンド結合部位を含むRAGEポリペプチド・ドメイン、及び免疫グロブリンCH2ドメインに直接連結されたドメイン間リンカーを利用できる。そのような融合タンパク質は、RAGEリガンドに対する特異的で、高い親和性結合を提供しうる。また、RAGE媒介性病理の治療法としてのRAGE融合タンパク質の使用も開示しうる。 (もっと読む)
バイオマーカーを用いたアッセイおよび方法
哺乳動物組織または細胞試料における一ないし複数のバイオマーカーの発現を検査する方法およびアッセイを提供する。開示した方法およびアッセイによって、一ないし複数のバイオマーカーの発現の検出が、該組織または細胞試料がApo2L/TRAILおよび抗DR5アゴニスト抗体などのアポトーシス誘導剤に対して感受性があるか否かを予測するものである。試験しうる特定のバイオマーカーには、フコシルトランスフェラーゼ、特にフコシルトランスフェラーゼ3(FUT3)および/またはフコシルトランスフェラーゼ6(FUT6)、並びにシアリルルイスAおよび/またはX抗原が含まれる。また、キットおよび製造品も提供される。 (もっと読む)
トランスフェクト細胞を含有するカプセル、それを調製する方法、並びに免疫及びワクチン接種するためのその使用
本発明は、対象の遺伝子を一過性にトランスフェクトし、生体適合性ポリマー膜内に包含させた細胞を含有するカプセル、これらのカプセルを調製する方法、対象の遺伝子によって分泌されたタンパク質の活性をin vivoで評価する方法であって、カプセルを多細胞生物に投与するステップと活性を検出するステップとを含む方法、このようなカプセルを含む医薬組成物、並びに対象のタンパク質を被検体に投与するためのその使用に関する。 (もっと読む)
新規な抗IGF−IR抗体及びその使用
本発明は、ヒトインスリン様成長因子I受容体IGF−IRと特異的に結合することができ、且つ/又はそのIGF−IRのチロシンキナーゼ活性を特異的に阻害することができる新規な抗体、特にマウスのモノクローナル抗体、キメラモノクローナル抗体及びヒト化モノクローナル抗体、並びにこれらの抗体をコードするアミノ酸配列及び核酸配列に関する。本発明はまた、IGF−IRを過剰発現する癌又はその受容体の過剰発現に関連した病状の予防的処置及び/又は治療的処置を目的とした薬剤としての、並びにIGF−IRの過剰発現に関連した疾患の診断のための方法又はキットにおけるこれら抗体の使用を含む。本発明は最後に、このような抗体と、抗EGFR抗体、及び/又は抗VEGF抗体、及び/又は腫瘍進行もしくは転移に関与する他の成長因子に対する抗体、及び/又は化合物、及び/又は抗癌剤、又は毒素と共役した物質とを組み合わせて含む、製品及び/又は組成物、並びに特定の癌の予防及び/又は治療のためのその使用に関する。
【配列表】
SEQUENCE LISTING
<110> PIERRE FABRE MEDICAMENT
<120> Novel anti-IGF-IR antibodies and uses thereof
<130> D22514
<140> PCT/IB2005/002619
<141> 2005-07-27
<150> US 60/591 932
<151> 2004-07-29
<150> FR 04/08379
<151> 2004-07-29
<160> 26
<170> PatentIn version 3.1
<210> 1
<211> 16
<212> PRT
<213> Mus musculus
<400> 1
Arg Ser Ser Gln Thr Ile Ile His Ser Asn Gly Asn Thr Tyr Leu Glu
1 5 10 15
<210> 2
<211> 7
<212> PRT
<213> Mus musculus
<400> 2
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 3
<211> 10
<212> PRT
<213> Mus musculus
<400> 3
Phe Gln Gly Ser His Val Pro Tyr Thr Phe
1 5 10
<210> 4
<211> 5
<212> PRT
<213> Mus musculus
<400> 4
Asp Tyr Trp Met Asn
1 5
<210> 5
<211> 17
<212> PRT
<213> Mus musculus
<400> 5
Leu Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asp Gln Asn Phe Tyr
1 5 10 15
Asp
<210> 6
<211> 13
<212> PRT
<213> Mus musculus
<400> 6
Ser Val Ile Tyr Tyr Gly Asn Tyr Arg Trp Tyr Phe Asp
1 5 10
<210> 7
<211> 11
<212> PRT
<213> Mus musculus
<400> 7
Lys Ala Ser Gln Asn Val Val Thr Asn Val Ala
1 5 10
<210> 8
<211> 7
<212> PRT
<213> Mus musculus
<400> 8
Ser Ala Ser Tyr Arg Tyr Ser
1 5
<210> 9
<211> 9
<212> PRT
<213> Mus musculus
<400> 9
His Gln Tyr Asn Asn Phe Pro Leu Thr
1 5
<210> 10
<211> 5
<212> PRT
<213> Mus musculus
<400> 10
Glu Tyr Gly Val Ser
1 5
<210> 11
<211> 16
<212> PRT
<213> Mus musculus
<400> 11
Val Ile Trp Gly Gly Arg Asp Thr Tyr Tyr His Ser Pro Leu Lys Ser
1 5 10 15
<210> 12
<211> 6
<212> PRT
<213> Mus musculus
<400> 12
His Glu Gly Met Asp Tyr
1 5
<210> 13
<211> 11
<212> PRT
<213> Mus musculus
<400> 13
Ile Thr Ser Thr Asp Ile Asp Asp Asp Met Asn
1 5 10
<210> 14
<211> 7
<212> PRT
<213> Mus musculus
<400> 14
Glu Gly Asn Thr Leu Arg Pro
1 5
<210> 15
<211> 9
<212> PRT
<213> Mus musculus
<400> 15
Leu Gln Ser Asp Lys Met Pro Leu Thr
1 5
<210> 16
<211> 5
<212> PRT
<213> Mus musculus
<400> 16
Asn Tyr Ala Met Ser
1 5
<210> 17
<211> 16
<212> PRT
<213> Mus musculus
<400> 17
Ser Ile Gly Ser Ala Gly Tyr Ile His Tyr Pro Asp Ser Val Lys Gly
1 5 10 15
<210> 18
<211> 9
<212> PRT
<213> Mus musculus
<400> 18
Glu Gly Gly Leu Val Trp Phe Ala Tyr
1 5
<210> 19
<211> 112
<212> PRT
<213> Mus musculus
<400> 19
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Thr Ile Ile His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 20
<211> 123
<212> PRT
<213> Mus musculus
<400> 20
Gln Ala Gln Leu Gln Gln Pro Gly Ala Val Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Ser Tyr Ser Phe Thr Asp Tyr
20 25 30
Trp Met Asn Trp Val Lys Arg Arg Pro Gly Gln Gly Leu Gln Trp Ile
35 40 45
Gly Leu Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asp Gln Asn Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Phe Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Asn Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser Val Ile Tyr Tyr Gly Asn Tyr Arg Trp Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 21
<211> 107
<212> PRT
<213> Mus musculus
<400> 21
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Val Thr Asn
20 25 30
Val Ala Trp Tyr Gln His Lys Pro Gly His Ser Pro Lys Pro Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Glu Tyr Phe Cys His Gln Tyr Asn Asn Phe Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 22
<211> 114
<212> PRT
<213> Mus musculus
<400> 22
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Asn Glu Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Gly Arg Asp Thr Tyr Tyr His Ser Pro Leu Lys
50 55 60
Ser Arg Leu Ser Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Lys His Glu Gly Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
100 105 110
Ser Ser
<210> 23
<211> 114
<212> PRT
<213> Mus musculus
<400> 23
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Asn Glu Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Gly Gly Asp Thr Tyr Tyr His Ser Pro Leu Lys
50 55 60
Ser Arg Leu Ser Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Lys His Glu Gly Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
100 105 110
Ser Ser
<210> 24
<211> 107
<212> PRT
<213> Mus musculus
<400> 24
Glu Thr Thr Val Thr Gln Ser Pro Ala Ser Leu Ser Val Ala Thr Gly
1 5 10 15
Glu Lys Val Thr Ile Arg Cys Ile Thr Ser Thr Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Pro Pro Lys Leu Leu Ile
35 40 45
Ser Glu Gly Asn Thr Leu Arg Pro Gly Val Pro Ser Arg Phe Ser Ser
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Val Leu Thr Ile Glu Asn Thr Leu Ser
65 70 75 80
Glu Asp Val Ala Asp Tyr Tyr Cys Leu Gln Ser Asp Lys Met Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 25
<211> 117
<212> PRT
<213> Mus musculus
<400> 25
Glu Val Asn Leu Val Glu Ser Gly Gly Ile Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Gly Ser Ala Gly Tyr Ile His Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Gly Leu Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ala
115
<210> 26
<211> 16
<212> PRT
<213> Mus musculus
<400> 26
Val Ile Trp Gly Gly Gly Asp Thr Tyr Tyr His Ser Pro Leu Lys Ser
1 5 10 15
(もっと読む)
VEGF媒介性活性をブロックすることによるI型糖尿病を処置する方法
VEGF媒介性活性をブロックまたは阻害することによって、哺乳動物、特にヒトにおける糖尿病を処置する方法。VEGF媒介性活性の好ましいインヒビターは、VEGFに結合および阻害し得る配列番号2のVEGF融合タンパク質トラップのようなVEGFアンタゴニストである。本発明の方法は、インスリン治療法のような他の治療法と組み合わせられ得る。特定の実施形態において、本発明の処置する方法は、血清グルコースレベルの低下、グルコース耐性の改善、および/または血糖コントロールの改善を生じる。 (もっと読む)
ヒト・パピローマウイルスに対するワクチン用ベクターおよび同ベクターによって形質転換された微生物
【課題】パピローマウイルスの表面カプシド抗原または癌誘発関連抗原に対するワクチンを発現させるベクター、前記ベクターによって形質転換された微生物、および前記形質転換された微生物またはその抽出精製物を用いたワクチンを提供する。
【解決手段】ポリ−γ−グルタミン酸合成酵素複合体をコードする遺伝子pgsB、pgsC、pgsAのうちのいずれか1つまたは2つ以上と、ヒト・パピローマウイルス(HPV)の表面カプシド抗原タンパク質または癌誘発関連抗原タンパク質遺伝子を含むワクチン製造用表面発現ベクターを提供する。 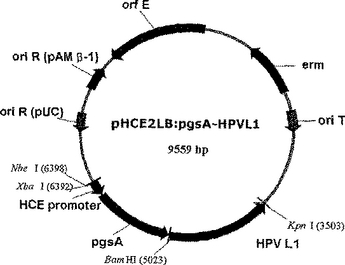 (もっと読む)
(もっと読む)
陽イオン性カルジオリピン類似体およびその使用
本発明は陽イオン性カルジオリピン化合物、並びにそれらをリポソーム調製、遺伝子トランスフェクションなどにおいて合成および使用する方法を提供する。特に、本発明は、ヒトおよび動物の疾患を治療する為に活性な薬剤を送達すること、および/または診断分析における、陽イオン性カルジオリピン類似体を含むリポソーム、陽イオン性カルジオリピン類似体を含む医薬組成物、並びにかかるリポソームおよび組成物の使用方法を提供する。 (もっと読む)
アトピー性皮膚炎の検査方法
アトピー性皮膚炎患者の皮疹部と無疹部、または患者皮疹部と健常者との間で発現レベルに差が見られる遺伝子SK404を見出した。そしてこの遺伝子が、アトピー性皮膚炎の検査や治療薬のスクリーニングにおいて指標として有用であることを明らかにした。すなわち本発明は、こうして見出された指標遺伝子SK404の発現レベルの比較に基づく、アトピー性皮膚炎の検査方法、および該疾患の治療のための化合物のスクリーニング方法を提供する。 (もっと読む)
精巣精上皮腫の診断方法
精巣精上皮腫(TS)を検出および診断する客観的な方法を本明細書において記述する。一つの態様において、本診断法は、TS細胞と正常細胞とを識別するTS関連遺伝子の発現レベルを決定する段階を含む。本発明は、TSの治療において有用な治療薬剤をスクリーニングする方法、TSを治療する方法、およびTSに対するワクチンを被験者に接種する方法をさらに提供する。 (もっと読む)
新規モノクローナル抗体および線虫幼虫抗原
本発明は、線虫L3の表面抗原と結合する、2002年1月24日にATCCに寄託され受託番号PTA‐4005を与えられた、単離されたモノクローナル抗体mAb PAB‐1に関する。また本発明は、該モノクローナル抗体と結合する抗原、および線虫感染の診断および治療または予防における該モノクローナル抗体および抗原の使用にも関する。 (もっと読む)
魚類類結節症ワクチン
【課題】 魚類類結節症ワクチンを提供する。
【解決手段】 フォトバクテリウム ダムセラ サブスピース ピシシーダの対数増殖期の不活化菌体又はその成分を有効成分とする魚類類結節症ワクチン。
(もっと読む)
ヘルペスウイルス科の核酸配列および/またはポリペプチド配列を含むワクチンの同定方法およびワクチン接種用組成物
本発明は、ヘルペスウイルスゲノム、特にHSV-1ゲノムのスクリーニングによって得ることができる抗原およびこのような抗原をコードする核酸に関する。より詳細な局面では、本発明は、このような抗原および核酸の単離方法ならびに免疫応答を生じさせるためのこのような単離抗原の使用方法に関する。抗原が免疫応答を生じさせる能力を、ワクチン接種または抗体調製技術で使用することができる。 (もっと読む)
癌治療のための組成物および方法
抗CEACAM6抗体および抗体断片、それらをコード化する核酸、それらを製造する方法、ならびにそれらの組成物を用いて癌を治療する方法が提供される。 (もっと読む)
5’−デオキシ−5’−メチルチオアデノシンに対する抗体及びその使用
本発明は新規な免疫原、MTA(5’−デオキシ−5’−メチルチオアデノシン)に高い特異性を有する新規な抗体、この抗体を用いた治療及び製剤、及びスペルミジンシンターゼの活性を測定する高感度なアッセイを提供する。 (もっと読む)
低用量のHib結合体との組合せワクチン
ジフテリア、破傷風、百日咳、およびHibに対して免疫するための抗原を含有する組合せワクチンは、公知である(「DTP−Hib」ワクチン)。本発明は、コストを低減するために低用量のHib抗原を用い、現場における再構成を必要としない、そのようなワクチンに対する必要性に取り組む。従って、本発明は、少なくともジフテリア、破傷風、百日咳、およびHibから被験体を防御するための抗原を含有する組合せワクチンを提供し、ここで:(a)このHibから防御するための抗原は、Hib莢膜糖類の結合体であり;(b)このワクチン中のHib結合体の濃度は、15μg/ml未満であり;そして(c)このHib結合体は、一度も凍結乾燥されていない。本発明のワクチンは、安全であり、かつ免疫原性が高いことが見出された。 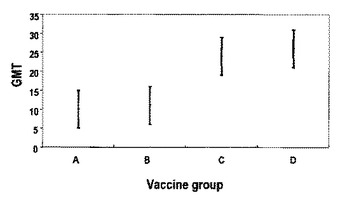 (もっと読む)
(もっと読む)
自己免疫疾患の治療のための方法および組成物
本発明は、一つ以上のHLA-DQ分子に結合し、DQ限定的T細胞応答を調節するコポリマーを投与することを含む、自己免疫疾患および他の望ましくない免疫応答を治療するための方法および組成物を提供する。該コポリマーは、アミノ酸のランダムコポリマーおよびDQ結合ポケットへの結合を容易にするアンカー残基を含むコポリマーである。 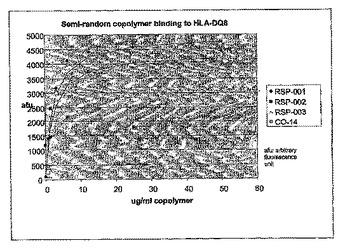 (もっと読む)
(もっと読む)
B細胞疾患の標的
本発明は、多発性骨髄腫(MM)などのB細胞疾患の診断および治療に関する。特に、本発明は、リンパ系癌細胞の表面上に発現された遊離のλ軽鎖に結合するリガンドを用いたB細胞疾患の治療に関する。 (もっと読む)
インターロイキン−33(IL33)およびIL−33レセプター複合体の使用
本発明は、IL−33もしくはIL−33レセプターのアゴニストまたはアンタゴニスト(IL−100およびIL−100レセプターとして公知である)が、多くの免疫状態および炎症性状態に対する応答を調節するという知見に、部分的に基づく。例えば、免疫障害および炎症障害(腫瘍および癌を含む)を処置するという目的のために、サイトカイン活性を調節する方法が提供される。IL−33およびIL−33レセプターのアゴニストまたはアンタゴニストを投与する方法もまた、提供される。 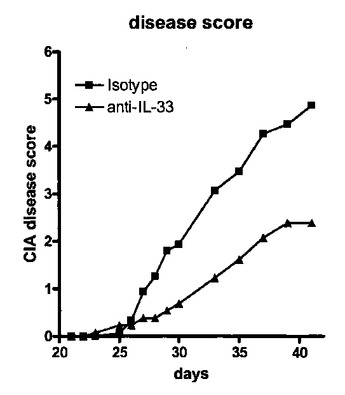 (もっと読む)
(もっと読む)
抗EpCAM免疫グロブリン
本発明は、特に、ヒトEpCAM抗原に特異的に結合するヒト免疫グロブリンであって少なくとも15日の血清中半減期を示す免疫グロブリンを患者に投与することにより、ヒト患者における腫瘍性疾患を処置する方法であって、前記免疫グロブリンを毎週1回を上回らない頻度で、好ましくは2週毎に1回を上回らない頻度で投与する段階を含む方法に関する。 (もっと読む)
481 - 500 / 526
[ Back to top ]

