Fターム[4C204BB04]の内容
Fターム[4C204BB04]に分類される特許
161 - 180 / 203
ペリンドプリルおよびその薬理上許容される塩を合成する新規な方法
本発明は、式(I)のペリンドプリルおよびその薬理上許容される塩類を合成する方法に関する。 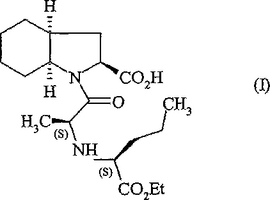 (もっと読む)
(もっと読む)
2,3−ジ置換インドール類の製造方法
a) ブロモインドール化合物(i)を、リガンド、パラジウム触媒および塩基の存在下に、ジアルコキシルC1-5ボランと反応させて、一般式(ii)の化合物を製造するか、或いは、化合物(i)をトリアルキルマグネシアート試薬と反応させ、次いでホウ酸塩で処理する工程;b) 工程aの生成物をR2-Hal (R2-Halは、明細書中に定義している)と反応させる工程からなる、一般式Iの化合物のような2,3 ジ置換インドール化合物の製造方法を開示する。 (もっと読む)
高分子固定化ルテニウム触媒及びその使用
【課題】 本発明は、ルテニウム触媒を両親媒性の架橋性高分子中に固定することにより調整された、高分子固定化ルテニウム触媒を用いる有機合成反応方法を提供する。
【解決手段】 ルテニウムを架橋高分子に担持させてなる高分子固定化ルテニウム触媒であって、該架橋高分子が芳香族側鎖及び親水性側鎖を有する架橋性高分子を架橋させてなることを特徴とする高分子固定化ルテニウム触媒である。この高分子担持ルテニウム触媒は、例えば極性溶媒を含む溶液中で該架橋性高分子に該ルテニウムの超微粒子を担持したミセルを形成した後、該架橋性高分子を架橋反応に付すことによって形成されることが好ましい。この触媒は、アルコールやスルフィドの酸化反応に用いることができる。
(もっと読む)
ポリメチン系エーテル化合物
所望のカウンターイオンを有するポリメチン系化合物を高純度、高収率で製造するために有用な中間体である新規化合物を提供する。
下記一般式(I)のポリメチン系エーテル化合物。また、該化合物と酸を接触することを特徴とするポリメチン系化合物の製造方法。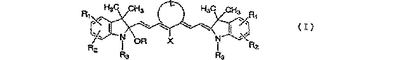
(式中、Rはアルキル基等を示し、R1およびR2はそれぞれ独立に水素原子、ハロゲン原子、ニトロ基、アルキル基等を示し、R1とR2は互いに連結して環を形成しても良い。R3は置換基を有してもよいアルキル基を示す。Lは環状構造を形成するのに必要なアルキレン基であり、Xは水素原子、ハロゲン原子等を示す。)  (もっと読む)
(もっと読む)
ウイルスポリメラーゼインヒビター
HCV NS5Bポリメラーゼのインヒビターとしての、下記式Iで表される化合物の異性体、エナンチオマー、ジアステレオマー若しくは互変異性体、又はその塩。
【化1】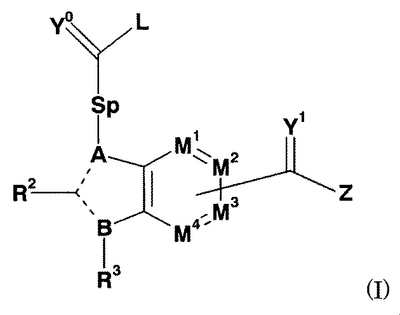
(式中、A、B、R2、R3、L、M1、M2、M3、M4、Y1、Y0、Z及びSpは、請求項1で定義されるとおりである。) 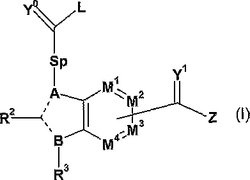 (もっと読む)
(もっと読む)
芳香族フッ素化合物の製造方法
【課題】芳香族ハロゲン化合物とフッ素化剤とのハロゲン交換反応をより高収率なものとし、最終的に得られる芳香族ハロゲン化合物を安定に高収率で製造する方法を提供する。
【解決手段】下記一般式(1)又は(2);
【化1】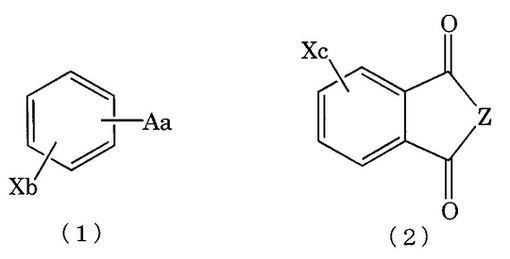
(式中、Xは、ハロゲン原子を表す。Aは、−CN、−NO2、−COF又は−COClを表す。aは、Aの置換数であり、b及びcは、Xの置換数である。Zは、−O−又は=N−Rを表す。Rは、水素原子、アルキル基又はアリール基を表す。)で表される芳香族ハロゲン化合物を有機溶媒中でフッ素化剤によりフッ素化する工程により、下記一般式(3)又は(4);
【化2】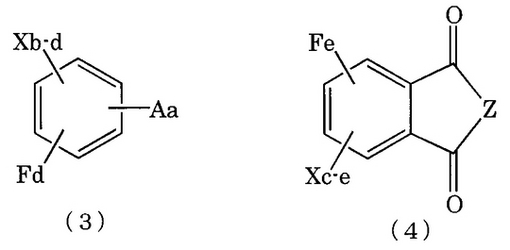
(式中、Fは、フッ素原子を表す。d及びeは、Fの置換数であり、b−d及びc−eは、残存Xの置換数である。)で表される芳香族フッ素化合物を製造する方法であって、該フッ素工程は、遊離酸の含有量を500ppm以下としてフッ素化する芳香族フッ素化合物の製造方法。
(もっと読む)
光学活性なインドリン−2−カルボン酸の調製方法
本発明は、場合により置換された光学活性なインドリン−2−カルボン酸またはその塩の調製方法であって、光学活性なキラルなオルト−X−置換フェニルアラニン化合物(式中、Xは脱離基である)を好ましくは約140℃未満の温度で環化させることによって上記光学活性なインドリン−2−カルボン酸化合物を形成させる方法に関する。 (もっと読む)
スタチンの調製に有用な製造方法及び中間体化合物
式(7):
【化1】
[式中、Rは場合により置換されていてもよいヒドロカルビル基又は場合により置換されていてもよい複素環式基を表わす、但しRは式(a):
【化2】
(ここで、RaはC1−16アルキル基のようなアルキル基、そして好ましくはイソプロピル基を表わし、Rbはアリール基、好ましくは4−フルオロフェニル基を表わし、Rcは水素、保護基又はC1−16アルキル基のようなアルキル基、そして好ましくはメチル基を表わし、そしてRdは水素、保護基又はSO2Re基を表わし、ここでReはC1−16アルキル基のようなアルキル基、そして好ましくはメチル基である)の化合物ではないことを条件とする]の化合物の製造方法が提供される。  (もっと読む)
(もっと読む)
トランドラプリル合成中間体の製造方法
本発明は、(2S,3aR,7aS)−ヘキサヒドロインドリン−2−カルボン酸及び(2R,3aS,7aR)−ヘキサヒドロインドリン−2−カルボン酸からなるラセミ体、ベンジルアルコール並びに光学活性10−カンファースルホン酸を非水溶媒中で加熱して前記ラセミ体をベンジルエステル化し、同一反応系内で生成したベンジルエステル体と光学活性10−カンファースルホン酸とのジアステレオ異性体塩を、有機溶媒への溶解度差を利用して光学分割し、さらに塩基で処理することを特徴とする(2S,3aR,7aS)−ヘキサヒドロインドリン−2−カルボン酸ベンジルエステルの製造方法に関する。 (もっと読む)
環状アミン類の製造方法
本発明は、イミド類を金属触媒存在下、水素還元することにより、該金属触媒が副生する水の影響を受けることのなく環状アミン類を収率よく製造できる工業的に有利な方法を提供する。イミド類を水溶性有機溶媒(特に、溶解度パラメーター8〜11.5の水溶性有機溶媒)中、金属触媒存在下、水素還元して環状アミン類を製造する。また、本発明は、イミド類を金属触媒存在下、有機溶媒中で、水素還元して環状アミン類を製造するに際し、該金属触媒が副生する水の影響を受けることなく、且つ立体保持性よく環状アミン類を工業的に有利に製造する方法を提供する。イミド類を金属触媒存在下、有機溶媒中で、水素還元して環状アミン類を製造するに際し、生成水及び該環状アミンを連続的に又は間欠的に抜き出しながら水素還元反応を行う。さらに、本発明は、トランス−オクタヒドロイソインドールを立体異性化することによりシス−オクタヒドロイソインドールを工業的に有利に製造できる方法を提供する。トランス−オクタヒドロイソインドールを金属触媒存在下、反応温度150〜350℃、水素分圧0.001〜30MPaで立体異性化する。 (もっと読む)
N−(インドールエチル)シクロアミン化合物
式(I)のN-(インドールエチル)シクロアミン化合物(式中R1’、R1’’、X、Arおよびnは、請求項1で示した意味を有する)は、セロトニン再摂取阻害剤(SSRIs)およびセロトニン受容体5−HT1Aおよび5−HT2Aのエフェクターであり、したがって、うつ病、ジスキネジー、パーキンソン病、痴呆、脳梗塞、統合失調症、アルツハイマー病、レビー小体型痴呆、ハンチントン病、トゥレットシンドローム、心配症、学習および記憶障害、痛み、睡眠障害および神経変性病といった中枢神経系の種々の病気の予防または治療に適する。
【化1】
 (もっと読む)
(もっと読む)
CNS障害の治療のための5−HT6レセプターリガンドとしてのアミノアルコキシインドール
本発明は、式(I)の化合物および医薬的に許容される塩(式中、R1、R2、R3、R4、mおよびnは、本明細書で定義されるとおりである)を提供する。本発明は、式(I)の化合物を調製するための方法、それを含む組成物、および5−HT6仲介疾患の治療のための医薬を製造するための式(I)の化合物の使用も提供する。  (もっと読む)
(もっと読む)
1,3,4,9−テトラヒドロピラノ[3,4−b]インドール誘導体の大規模実施可能な合成方法
本発明は、式(VI):
[但し、R1、R9、R3'、R4及びYが明細書に規定されている。]
で表される化合物の合成方法を対象とし、該方法は、化合物の大規模合成に有用である。更に本発明は、式(VI)で表される化合物の合成に有用な中間体及び該中間体の合成方法を対象とする。  (もっと読む)
(もっと読む)
cPLA2阻害剤として有用なC−2,C−3置換N−アルキル化インドールを合成する方法
本発明は、式1の化合物を製造する方法を提供する。該方法は、式2の化合物と式3の化合物とを反応させて、式4の化合物を生成する工程を包含する:ここで、R1、R2、R3、R4およびR5は、本明細書中で記述したように定義される。次いで、式4の化合物は、式1の化合物に変換される。本発明は、さらに、式3および4の化合物、ならびに式3および4の化合物を製造する方法を包含する。式2の化合物と式3の化合物とのカップリング反応は、銅触媒が少なくとも約5モル%で存在しかつ少なくとも約2当量(すなわち、約200モル%)の塩基が使用されるという条件で、パラジウム触媒の量を少なくしたとき(例えば、約0.5モル%〜約1.5モル%)、効率的に進行して、高収率で、式4の化合物が生成することが発見された。より少ないパラジウム触媒を使用すると、本発明の方法は、効率的かつ経済的になる。  (もっと読む)
(もっと読む)
オキシムエステル光開始剤
式(I)の化合物(式中、R1、R2およびR10は、互いに独立して、C1〜C20アルキル、フェニル、C1〜C12アルキルフェニルまたはフェニル−C1〜C6アルキルであり;R3およびR4は、互いに独立して、水素、C1〜C20アルキル、NR6R7またはSR8であるが、ただしR3とR4の少なくとも一つは、NR6R7またはSR8であり;R5は、水素またはC1〜C20アルキルであり;R6およびR7は、互いに独立して、C1〜C20アルキルであるか、またはR6およびR7は、それらが結合しているN原子と一緒になって、5員環もしくは6員環を形成し、それはO、SもしくはNR9で場合により中断されており、かつ1以上のC1〜C4アルキルで場合によりさらに置換されており;R8は、フェニル、ビフェニリル、ナフチル、アントリルまたはフェナントリルであり、それらのすべては、1個以上のC1〜C4アルキルで場合により置換されており;R9は、水素、C1〜C20アルキル、C2〜C4ヒドロキシアルキルまたはフェニルである)は、光重合反応において、予想外の良好な性能を示す。 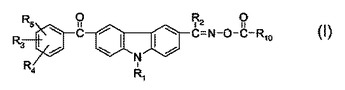 (もっと読む)
(もっと読む)
過酸化水素製造中の有機化学物質の酸化
貴金属ナノ触媒作用によって、高い選択性を有して、かつ低い水素濃度において生成される過酸化水素(H2O2)を酸化剤として用い、種々の有機化学品原料から酸化された有機化学品生成物を製造するための方法。有機化学品酸化のプロセス工程は、任意選択的に過酸化水素の製造と同時にインサイチューで、あるいは2段階プロセスにおいて実施することができる。2段階プロセスにおいて、過酸化水素中間体は、第1の触媒反応工程において、適当な溶媒に加えた水素および酸素の供給物から、貴金属ナノ触媒作用によって直接的に生成される。有機化学品原料および過酸化水素中間体および溶媒の溶液を第2の触媒反応器中へ供給して、酸化された有機化学品生成物を生成する。 (もっと読む)
1−アミド−3−(2−ヒドロキシフェノキシ)−2−プロパノール誘導体、ならびに2−アミドメチル−1,4−ベンゾジオキサン誘導体の製造法
【課題】 医薬品や生理活性物質の合成中間体として重要な1−アミド−3−(2−ヒドロキシフェノキシ)−2−プロパノール誘導体およびその光学活性体の提供。
【解決手段】 下記式(1)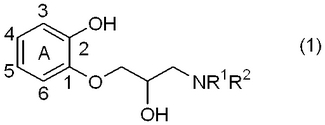
(式中、環Aは更なる1〜4個の置換基を有してもよく、該置換基はアルキル基、アラルキル基、芳香族基、ハロゲン、ハロゲン化アルキル基、アルカノイル基、アルキルカルバモイル基、シアノ基、またはニトロ基から選ばれた置換基を意味する。また該環Aは、縮合多環式炭化水素でもよい。R1はアルカノイル基またはアロイル基を表し、そしてR2は水素、アルカノイル基またはアロイル基を表すか、あるいはR1とR2が結合し、N原子と共に環状イミド基を形成してもよい。)で表される1−アミド−3−(2−ヒドロキシフェノキシ)−2−プロパノール誘導体。
(もっと読む)
オキシム誘導体および潜在酸としてのそれらの使用
本発明は、式(I、IIまたはIII)の新規な光酸発生剤化合物であり、ここで、R1は、例えばC1〜C18アルキルスルホニルまたはフェニルスルホニル、フェニル−C1〜C3アルキルスルホニル、ナフチルスルホニル、アントラシルスルホニルまたはフェナントリルスルホニルであり、すべては、場合により置換されているか、あるいはR1は、基(a,bまたはc)であり;X1、X2およびX3は、互いに独立に、OまたはSであり;R’1は、例えば、フェニレンジスルホニル、ナフチレンジスルホニル、ジフェニレンジスルホニルまたはオキシジフェニレンジスルホニルであり、すべては、場合により置換されているか;R2は、ハロゲンまたはC1〜C10ハロアルキルであり;Xは、ハロゲンであり;Ar1はヘテロアリーレンであり、例えば、ビフェニリルまたはフルオレニルであり、あるいは置換ナフチルであり;Ar’1は、場合により置換されており;R8、R9、R10およびR11は、例えば、非置換またはハロゲンで置換されているC1〜C6アルキルであるか;あるいはR8、R9およびR10は、非置換またはC1〜C4アルキルもしくはハロゲンで置換されているフェニルであるか;あるいはR10およびR11は一緒に、非置換またはC1〜C4アルキルもしくはハロゲンで置換されている1,2−フェニレンまたはC2〜C6アルキレンである。 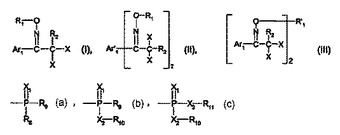 (もっと読む)
(もっと読む)
インドロン誘導体、その製造方法及びその使用
本発明は、インドロン誘導体、これらの製造方法、これらを含む薬剤組成物及び薬剤としてのこれらの使用に関する。 (もっと読む)
ピロロトリアジン化合物の製造法
本発明は、式(I):
【化1】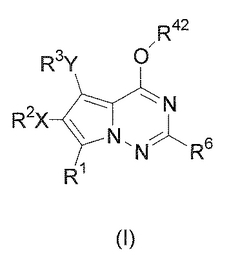
のピロロトリアジン化合物、およびそれらの医薬的に許容し得る塩を製造するための製法を提供する。式(I)の化合物は、増殖因子受容体(例えば、VEGFR−2およびFGFR−1)のチロシンキナーゼ活性を抑制し、従ってそれらは抗癌剤として有用である。式(I)の化合物はまた、増殖因子受容体を通じて作動するシグナル伝達経路に関係する他の疾患の処置のためにも有用である。 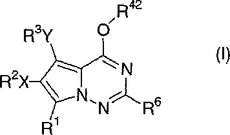 (もっと読む)
(もっと読む)
161 - 180 / 203
[ Back to top ]

