Fターム[4H045BA35]の内容
Fターム[4H045BA35]に分類される特許
61 - 80 / 97
リン脂質−PEG−生体分子コンジュゲートの合成法
【課題】本発明は、標的診断または治療およびにおける診断用または治療用リポソーム/ミセルの成分としての使用に適当なリン脂質−PEG−生体分子コンジュゲートの製造法、かつ具体的にはリン脂質生体分子、例えばペプチド、コンジュゲートの合成、精製および分析の単純な方法を提供すること。
【解決手段】ペグ化リン脂質と生体分子を共有結合的付着によりカップリングさせ、得られたコンジュゲートを精製する工程により解決される。
(もっと読む)
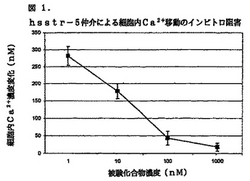
ソマトスタチンアンタゴニスト
【課題】ソマトスタチンアンタゴニストの提供。
【解決手段】次式の化合物A1-cyclo[D-Cys-A2-D-Trp-A3-A4-Cys]-A5-Y1またはその医薬的に許容できる塩[式中:A1は、置換されていてもよい芳香族α−アミノ酸であり;A2は、置換されていてもよい芳香族α−アミノ酸であり;A3は、Dab、Dap、LysまたはOrnであり;A4は、β−ヒドロキシバリン、Ser、HserまたはThrであり;A5は、置換されていてもよいD−またはL−芳香族α−アミノ酸であり;Y1は、OH、NH2またはNHR1であり、ここでR1は(C1-6)アルキルであり;式(I)の各アミドペプチド結合およびA1のアミノ基のアミン窒素はメチル基で置換されていてもよく、ただしそのようなメチル基が少なくとも1つある]、およびその使用について提供する。
(もっと読む)
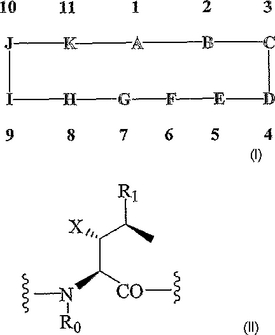
新規サイクロスポリン
本発明の化合物は式Iに見られる化学構造により表される: 式中AはR0、R1、B、C、D、E、F、G、H、I、J、およびKが本明細書で定義された、式IIのアミノ酸: またはその薬学的に許容される塩である。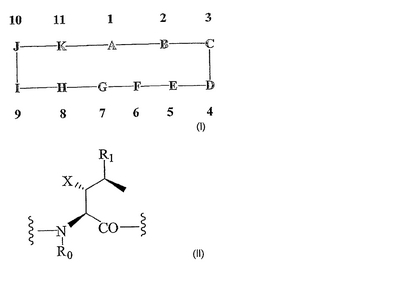
 (もっと読む)
(もっと読む)
単色蛍光プローブ
この出願の発明は、蛍光蛋白質の変異体であって、circular−permuted蛍光蛋白質(cpFP)、基質ドメインおよびリン酸化認識ドメインを有することを特徴とする単色蛍光プローブである。このような特徴を有する単色蛍光プローブによって、細胞や組織が生きた状態(リアルタイム)で蛋白質リン酸化酵素の活性測定ができ、1種類の蛋白質リン酸化酵素の活性測定するために2種類もの蛍光団を用意することなく、しかも複数の細胞や組織においての蛋白質リン酸化酵素の活性を同時に可視化検出、測定することができる。 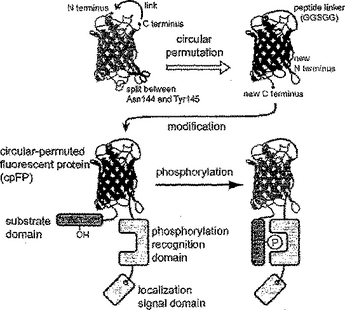 (もっと読む)
(もっと読む)
二環式ヘキサペプチド、ネパデュタントの製造方法
本発明は、薬理学的活性を有する化合物を調製するための中間体として有用な式(I)の高純度二環式ペプチド化合物の高収率での調製のために、溶液中で専ら実行される新規の方法に関する。
【化1】
 (もっと読む)
(もっと読む)
アビプタジルのための処方物
本発明は、アビプタジルおよびその誘導体の薬学的処方物に関する。規定のpH範囲を有するバッファーで調製した規定濃度のアビプタジルを含有する処方物によりアビプタジル処方物の安定性は明らかに向上した。 (もっと読む)
HCV処置用組成物
本発明は、a)非免疫抑制性シクロフィリン結合性サイクロスポリンである第一剤、例えば式Iの化合物およびb)併用剤を含む、医薬組み合わせ剤に関する。  (もっと読む)
(もっと読む)
新規な多量体CD40リガンド、その製造方法及び医薬を製造するためのそれらの使用
本発明は式(I)
(式中、Yは大員環を表し、この環は9〜36の原子を含み、3つのアミン又はCOOH官能基により機能化され、Rcは式H−Xa−Xb−Xc−Xd−Xe−(Xf)i−(式中、iは0又は1を表し、Xaは特にリジン、アルギニン、オルニチン残基から選択され、Xbは特にグリシン、アスパラギン、L−プロリン又はD−プロリン残基から選択され、Xc及びXdは特にチロシン、フェニルアラニン又は3−ニトロチロシン残基から選択され、Xe及びXfは特に下記のアミノ酸残基NH2−(CH2)n−COOH(nは1〜10の範囲である)又はNH2−(CH2−CH2−O)m−CH2CH2COOH(mは3〜6の範囲である)から選択され、但し、アミノ酸残基Xa、Xb、Xc及びXdのうちの少なくとも1つが天然のCD40Lの143Lys−Gly−Tyr−Tyr146断片の配列において対応するアミノ酸とは異なる))
の化合物に関する。 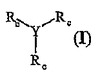 (もっと読む)
(もっと読む)
抗インテグリン活性を有するフルオロ−アルキル−シクロペプチド誘導体
式(I)の化合物:シクロ[NX1−R1−CO−NX2−R2−CO−NX3−R3−CO−NX4−CO−NX5−R5−CO](式中、様々な基の意味は明細書中に記載するとおりである)は、インテグリン、特にαvβ3およびαvβ5ファミリーに属するものの阻害剤であり、したがって医薬、特に異常な血管新生の原因である疾患、例えば、網膜症、急性腎不全、骨粗鬆症および転移の治療のための医薬として有用である。本明細書に記載する化合物はまた、適当に標識すると診断薬としても有用であり、特に小さい腫瘤および動脈閉塞現象の検出と位置づけのために有用である。 (もっと読む)
IRES仲介性翻訳の複素環式阻害剤およびその使用法
本発明は、IRES阻害活性を示す複素環式化合物を提供する。複素環式化合物は一般にアミド結合を通して共有結合している三つの反復C-C-Nサブユニット、および各サブユニットの中心炭素に連結している様々な側鎖の9員環である。本発明の化合物を含む製剤およびキットも提供する。 (もっと読む)
新規な誘導システムの合成及び特徴付け、並びに標的細胞への治療対象分子のベクター化
本発明は、2つの面、いわゆる上面及びいわゆる下面を画定し、前記2つの面が両方ともグラフトされるフレームを形成するグラフトホモデティックシクロペプチドの調製方法であって、線状ペプチドを合成し、前記合成は、修飾された又は修飾されないアミノ酸から行われ、アミノ酸の内幾つかは、直交保護基を持ち、得られた保護線状ペプチドの分子内環化を行い、保護前駆物質により直交保護基の全部又は一部を置換し、少なくとも1つの対象分子をオキシム結合により前記フレームの一方及び/又は他方の面にグラフトすることを特徴とする方法に関する。 (もっと読む)
肥満症の治療に使用するためのペプチド
本発明は、1以上のメラノコルチン受容体タイプを調節することにおいて有効な新規なペプチド化合物、該化合物の治療における使用、それを必要としている患者に対して当該化合物を投与することを含んでなる治療方法、医薬の製造における該化合物の使用に関する。本発明の化合物は、肥満の治療、並びに肥満に付随する種々の疾患または状態の治療に関して特に興味あるものである。 (もっと読む)
肥満症の治療に使用するためのペプチド
本発明は、1以上のメラノコルチン受容体タイプを調節することにおいて有効な新規なペプチド化合物、該化合物の治療における使用、それを必要としている患者に対して当該化合物を投与することを含んでなる治療方法、医薬の製造における該化合物の使用に関する。本発明の化合物は、肥満の治療、並びに肥満に付随する種々の疾患または状態の治療に関して特に興味あるものである。 (もっと読む)
肥満症の治療に使用するためのペプチド
本発明は、1以上のメラノコルチン受容体タイプを調節することにおいて有効な新規なペプチド化合物、該化合物の治療における使用、それを必要としている患者に対して当該化合物を投与することを含んでなる治療方法、医薬の製造における該化合物の使用に関する。本発明の化合物は、肥満の治療、並びに肥満に付随する種々の疾患または状態の治療に関して特に興味あるものである。 (もっと読む)
結合分子
本発明は、側鎖サブユニットが天然および/または非天然のD−および/またはL−アミノ酸からなるポリペプチド鎖であり、そして側鎖サブユニットが支持体構造に共有結合で結合している、少なくとも一つの環状分子サブユニットおよび少なくとも二つの側鎖サブユニットの担体構造からなる結合分子に関する。 (もっと読む)
カーボンナノチューブ精製方法、精製装置、及び精製キット
【課題】 原料の固体状のカーボンナノ粒子などの不純物からカーボンナノチューブを寸法径の差を利用して篩い分ける。
【解決手段】 カーボンナノチューブを含む炭素化合物を分散させた溶液にカーボンナノチューブと複合体を形成する分子ピンセットを添加・混合して、カーボンナノチューブを可溶化する。可溶化したカーボンナノチューブと分子ピンセットの複合体と不溶物とを電気泳動法等で分離して、カーボンナノチューブと分子ピンセットの複合体のみを含む溶液を得る。得られたカーボンナノチューブと分子ピンセットの複合体溶液に分子ピンセットを切断する酵素を加えて、カーボンナノチューブと分子ピンセットの複合体を壊して、カーボンナノチューブを不溶化させる。不溶化したカーボンナノチューブをろ過して単離後、蒸留水、メタノール洗浄して、精製したカーボンナノチューブを得る。
(もっと読む)
シクロスポリンアルキンおよびそれらの医用薬剤としての有用性
本発明の化合物は、本明細書において定義されるX、R0、およびR1を有する、式(I)において見出される化学構造またはその薬学的に許容される塩によって示される。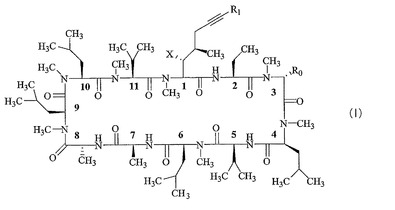
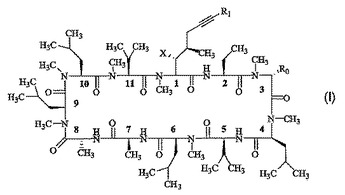 (もっと読む)
(もっと読む)
新規シクロスポリン類似体およびそれらの薬学的使用
本発明の化合物は、下記の式I、またはその薬学的に許容される塩で表され、式中、X、R0、R1、およびR2は本明細書中に定義される。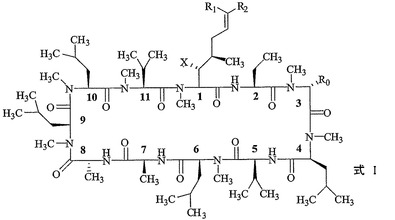
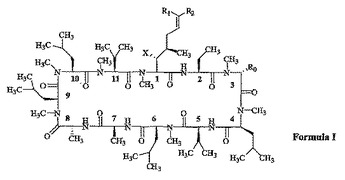 (もっと読む)
(もっと読む)
シクロスポリンアルキン類似体およびそれらの薬学的使用
本発明の化合物は、本明細書において定義されるX、R0、R1、およびR2を有する、式(I)において見出される化学構造またはその薬学的に許容される塩によって示される。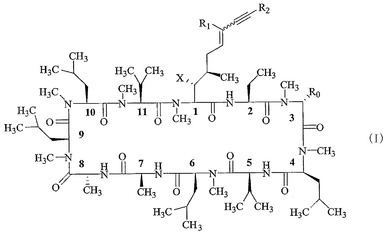
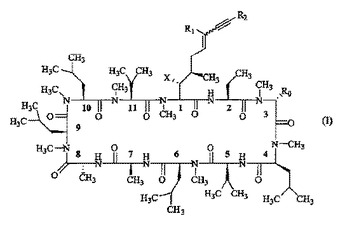 (もっと読む)
(もっと読む)
超臨界流体中の閉環複分解方法
好適な有機溶媒中でルテニウム触媒の存在下で式IIIのジエン化合物を環化することを含む式Iの化合物の調製方法であって、その方法を超臨界条件又は超臨界付近の条件でガス流体中で行なうことを特徴とする前記化合物の調製方法が開示される。
【化1】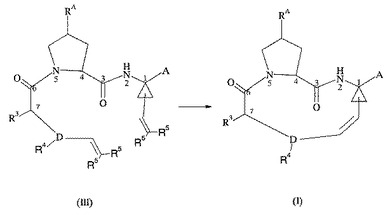
式Iの化合物はC型肝炎ウイルス(HCV)感染症の治療のための活性薬剤であり、又は坑HCV薬剤の調製に有益な中間体である。 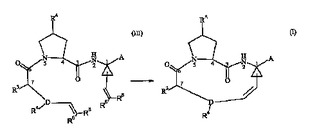 (もっと読む)
(もっと読む)
61 - 80 / 97
[ Back to top ]