質量分析装置
【課題】試料に含まれる物質を網羅的に同定する際にMS2分析する分画数を抑えることで分析時間を短縮しながら同定の正確性を確保する。
【解決手段】全ての分画試料をMS1分析した結果に基づき作成した、保持時間、m/z、信号強度を3軸とする3次元グラフに対し(S1-S2)、ωよりも大きな閾値θNで強度を判定してピーク検出を行い、検出されたピークのピークトップが存在する分画試料をMS2分析対象として選択する(S3-S5)。次に、選択された分画試料にピークトップが存在し、強度が閾値ω以上であるピークを検出し、検出されたピークをプリカーサイオン候補として挙げる(S6)。そして、選択された分画試料の含有物質が同定されるまでプリカーサイオン候補についてのMS2分析を順次実行する(S7-S9,S14-S15)。1つの分画試料に対し多くのプリカーサイオン候補が挙げられるので、分画試料の含有物質の同定確率が高まる。
【解決手段】全ての分画試料をMS1分析した結果に基づき作成した、保持時間、m/z、信号強度を3軸とする3次元グラフに対し(S1-S2)、ωよりも大きな閾値θNで強度を判定してピーク検出を行い、検出されたピークのピークトップが存在する分画試料をMS2分析対象として選択する(S3-S5)。次に、選択された分画試料にピークトップが存在し、強度が閾値ω以上であるピークを検出し、検出されたピークをプリカーサイオン候補として挙げる(S6)。そして、選択された分画試料の含有物質が同定されるまでプリカーサイオン候補についてのMS2分析を順次実行する(S7-S9,S14-S15)。1つの分画試料に対し多くのプリカーサイオン候補が挙げられるので、分画試料の含有物質の同定確率が高まる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、液体クロマトグラフ(LC)、ガスクロマトグラフ(GC)、キャピラリ電気泳動装置(CE)などによって各種物質が分離されて分画された試料に対し、質量分析を行って各物質を同定する質量分析装置に関し、さらに詳しくは、MSn分析(nは2以上の整数)を行うことが可能な質量分析装置に関する。
【背景技術】
【0002】
生命科学の研究や医療、医薬品開発などの分野においては、生体試料を対象として、タンパク質、ペプチド、核酸、糖鎖など様々な物質を網羅的に同定することがますます重要になってきている。特にタンパク質やペプチドを対象とするこうした網羅的な解析手法はショットガン・プロテオミクス(Shotgun Proteomics)と呼ばれている。こうした解析のために、LCやGC、或いはCEなどのクロマトグラフィと、タンデム型質量分析装置(MSn型質量分析装置)とを組み合わせた分析手法が非常に威力を発揮している。
【0003】
タンデム型質量分析装置を用いた生体試料中の各種物質の網羅的同定手法として、従来知られている一つの手法の手順は次のとおりである(非特許文献1参照)。
[ステップ1] 分析対象である試料に含まれる各種物質をLC、CE等により分離し、その溶出液を分取・分画して多数のサンプルを調製する(ここでは、分取・分画により得られた1つ1つのサンプルを「分画試料」と呼ぶこととする)。なお、試料を分取・分画する際には、予め決めた一定の時間間隔で分画を行う又は一定量の試料液を採取するように分画を行うことにより、全ての物質が漏れなくいずれかの分画試料に含まれるようにする(例えば特許文献1参照)。
【0004】
[ステップ2]各分画試料に対するMS1スペクトルをそれぞれ取得し、該MS1スペクトル上で同定対象の物質群に由来すると考えられるピークを選択する。
[ステップ3]上記ステップ2で選択したピークをプリカーサイオンに設定して当該分画試料に対しMS2分析を実行し、その結果に基づいてデータベース検索やデノボシーケンスサーチを行い、分画試料に含まれる物質を同定する。
[ステップ4]十分な確度で特定の物質が同定されなかった場合には、MS1スペクトル上で見つけた別のピークをプリカーサイオンに設定してMS2分析を実行するか、或いは、さらに高次(つまりnが3以上)のMSn分析を実行し、その結果に基づくデータベース検索やデノボシーケンスサーチなどにより、分画試料に含まれる物質を同定する。
[ステップ5]上記ステップ2〜4の処理を複数の分画試料それぞれに対して行い、元の試料に含まれていた様々な物質を網羅的に同定する。
【0005】
LCやGCなどのカラムを用いた分離手法では、試料中の各種物質はカラムを通過するに要する時間(保持時間、以下「RT」と称す)の大きさによって分離される。この場合、MS1分析で検出されたイオン強度の総和を保持時間の経過に沿って表したプロファイルは一般にTIC(トータルイオンクロマトグラム)と呼ばれ、特定の質量電荷比m/zに着目し、その質量電荷比のイオン強度を保持時間の経過に沿って表したプロファイルはMC(マスクロマトグラム)と呼ばれる。
【0006】
上記のような網羅的同定のための分析手法において、高い確度で以て物質を同定するには、同一の分画試料に含まれる物質の種数が少ない(できれば1種類のみである)ことが望ましい。そのためには1つの分画試料を分取する時間を短くすればよいが、その場合、分画数が多くなる。元の試料に含まれていた物質を網羅的に同定するために全ての分画試料を対象としてMSn分析及び同定処理を行う場合、分画数が増えるほど分析や処理に掛かる手間や時間が膨大なものとなる。特に、異なる分画試料を分析する場合には、機械的に試料を交換したり分析対象の試料を分析位置まで搬送したりする必要があるため、分析に要する時間が長くなり、分析対象である分画試料の数が増えると分析効率の低下が顕著である。
【0007】
一般に、全ての分画試料に有意な物質が含まれているというわけではないため、実際には、網羅的同定であっても、必ずしも全ての分画試料を分析する必要はない。そこで、元の試料に含まれていた物質を網羅的且つ効率的に同定するには、同定すべき物質が含まれる可能性が高い分画試料を優先的に選択してMSn分析することが重要である。そのための一つの手法として、各分画試料に含まれる物質の総量に対応するTICをモニタリングし、TICに現れるピークの保持時間に対応した分画試料を優先的にMSn分析することが考えられる。しかしながら、同定対象である物質の質量電荷比におけるMCとTICとを比較したとき、両者のピークの発生位置(つまりは保持時間)が必ずしも一致するとは限らない。
【0008】
図6は、或る試料に対するTICと該試料に含まれるm/z1956である物質のMCとの測定結果例を示す図である。この例では、MCではRT=6100付近で大きなピークが生じているのに対し、TICでは同RTにピークが現れておらず、両者のピークの発生位置は一致しない。このような場合には、TIC上で現れるピークの保持時間に対応した分画試料をMS2分析の対象として選択したとしても、その分画試料には同定対象である物質が十分な濃度で含まれていない可能性がある。一方、同定対象である物質が十分な濃度で含まれる分画試料を選択するには、その物質に対するMCにおいて現れるピークの保持時間に対応した分画試料を選択すればよい。しかしながら、分画試料に含まれる物質が未知である状態においては、いずれの質量電荷比に対応するMCを用いればよいのか判断することはできないため、MCを用いて分画試料を選択することはできない。
【0009】
上記課題を解決するために、従来、非特許文献2に記載の方法が知られている。即ち、まず、各RTでのピークリスト(又はMS1スペクトル)を並べた連結ピークリストを作成する。図5はこの連結ピークリストを3次元グラフ化した図であり、保持時間(RT)と質量電荷比とが紙面上の2軸であり、各ピークの信号強度は色とその濃淡という別の軸で示される。なお、この図5中の横方向の2本の点線で挟まれた保持時間範囲が図6に示したTIC及びMCの時間範囲であり、図5中の縦方向の点線がm/z1956のMCに対応したピークデータである。
【0010】
次に、この3次元グラフに対し2次元平面上でピーク検出を行う。以下、このピーク検出を「2Dピーク検出」といい、これにより検出されたピークを「2Dピーク」ということとする。図7に示すように、或る分画に対応するRT(図7中に横方向の点線で示すRT)には、幾つかの質量電荷比において2Dピークが観測される。このように分画された分画試料には同定対象である物質の少なくとも1つが含まれている可能性が高いと判断できるので、この分画試料をMS2分析の対象として選択する。さらに、このときに見つかった2Dピーク(図7中に○囲みで示した点で示されるピーク)は、当該分画に含まれていた物質を同定するためのMS2分析のプリカーサイオン候補となり、その分画に含まれる物質が同定されるまで順次nの数を増加させる(開裂の段数を増加させる)MSn分析を行う対象となる。
【0011】
上述した2Dピーク検出に基づく分画試料の選択処理においては、予め定めた閾値を超えるような信号強度を有する2DピークがMS2分析のプリカーサイオン候補として抽出される。そのため、抽出される2Dピークの数は閾値によって変化し、結果として、選択される分画試料の数やリストアップされるプリカーサイオン候補の数も閾値によって増減することになる。閾値が小さい場合には信号強度が比較的小さな2Dピークも選出されるため、プリカーサイオン候補のリストアップ漏れを軽減することができる。その反面、MSn分析の対象とされる分画試料の数も多くなるため、分析や処理の手間が増大し、分析効率の低下に繋がる。一方、閾値を大きくした場合には、MSn分析の対象として選択される分画試料の数を抑えることができるものの、プリカーサイオン候補の数も少なくなるため、選択された分画試料において物質同定に失敗する可能性が高まる。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】特開2010−14559号公報
【非特許文献】
【0013】
【非特許文献1】エドワード・エム・マーコッテ(Edward M Marcotte)、「ハウ・ドゥー・ショットガン・プロテオミクス・アルゴリズムズ・アイデンティファイ・プロテインズ?(How do shotgun proteomics algorithms identify proteins?)」、ネイチャー・バイオテクノロジー(Nature Biotechnology) 25、2007年、p.755-757
【非特許文献2】ユルゲン・コックス(Jurugen Cox)、ほか1名、「マックスクァント・イネーブル・ハイ・アイデンティフィケイション・レイツ、インディビデュアライズド・ピーピービー-レンジ・マス・アキュラサイズ・アンド・プロテオーム-ワイド・プロテイン・クォンティフィケイション(MaxQuant enable high peptide identification rates, individualized p.p.b.-range mass accuracies and proteome-wide protein quantification )」、ネイチャー・バイオテクノロジー(Nature Biotechnology) 26、2008年、p.1367-1372
【発明の概要】
【発明が解決しようとする課題】
【0014】
本発明は上記課題を解決するために成されたものであり、その目的とするところは、例えば保持時間と質量電荷比とを2軸とする2次元平面上で上記のような2Dピーク検出によりMSn分析の対象とする分画試料とMSn分析のプリカーサイオン候補とを抽出する場合に、分析対象とする分画試料の数をできるだけ抑えることによって分析の手間や時間の節約を図りつつ、プリカーサイオン候補の漏れをなくして、同定の失敗を少なくしたり同定の正確性を向上させたりすることができる質量分析装置を提供することにある。
【課題を解決するための手段】
【0015】
上記課題を解決するために成された本発明は、試料に含まれる各種物質を分離用パラメータに従って分離した後に分取・分画して調製された複数の分画試料に対し、MSn分析(nは2以上の整数)をそれぞれ実行することが可能な質量分析装置であって、
a)全ての分画試料に対するMS1分析をそれぞれ実行して得られたMS1スペクトルデータに基づいて、分離用パラメータ及び質量電荷比を2軸とする2次元平面を形成し、該平面に直交する軸に信号強度をとった仮想的な3次元グラフを作成し、該3次元グラフに対し信号強度が第1閾値以上であるピークを抽出し、該ピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択する分画試料選択手段と、
b)前記3次元グラフに対し信号強度が前記第1閾値よりも小さな第2閾値以上であって、前記分画試料選択手段により選択された分画試料に対応する前記分離用パラメータにピークトップが存在するピークを抽出し、該ピークのピークトップに対応した質量電荷比をプリカーサイオンの候補として選択するプリカーサイオン候補選択手段と、
c)前記分画試料選択手段により選択された分画試料に対し、前記プリカーサイオン候補選択手段により該分画試料に対応して選択されたプリカーサイオン候補のうちの1つをプリカーサイオンに設定したMSn分析を実行するMSn分析実行手段と、
d)前記MSn分析実行手段によるMSn分析実行結果に基づいてその分画試料に含まれる物質の同定を行う同定手段と、
を備えることを特徴としている。
【0016】
試料に含まれる各種物質を分離する手段がLCやGCなど、カラムを用いたものである場合には、上記分離用パラメータとは時間(保持時間)である。また、試料に含まれる各種物質を分離する手段がCEである場合には、上記分離用パラメータとは移動度である。即ち、試料に含まれる各種物質を分離する手段が例えばLCである場合には、複数の分画試料はそれぞれ異なる保持時間(厳密には所定の保持時間範囲)において採取(分取)された試料である。
【0017】
本発明に係る質量分析装置において、分画試料選択手段及びプリカーサイオン候補選択手段はいずれも、分離用パラメータ、質量電荷比、及び信号強度を3つの軸にとった仮想的な3次元グラフに対し、信号強度が閾値以上であるか否かを判定することによりピークを検出する。ただし、多数の分画試料の中からMSn分析対象の分画試料を選択するために利用されるピークを検出するための第1閾値は、MSn分析のプリカーサイオン候補を選択するために利用されるピークを検出するための第2閾値よりも大きい。即ち、前者は後者よりも、より厳しい基準で以てピークを検出することになるから、MSn分析の対象となる分画試料は比較的高い濃度で何らかの物質を含む分画試料に限られる。一方、プリカーサイオン候補となるピークを検出する基準は相対的に緩いから、1つの分画試料に対して挙げられるプリカーサイオン候補の数は比較的多くなる傾向にある。
【0018】
即ち、一般的に、MSn分析の対象となる分画試料の数が少ない段階でも、各分画試料中の物質の同定に有益であるプリカーサイオンの候補がそれぞれ複数挙げられる可能性が高くなる。一般に、MS1スペクトル中のピークの中で信号強度が最大であるピークをプリカーサイオンとしてMS2分析を行った結果を利用して含有物質の同定に成功しない場合であっても、同じMS1スペクトル中で信号強度が最大ではないピークをプリカーサイオンとしてMS2分析を行った結果を利用して含有物質の同定に成功することもある。したがって、或る1つの分画試料に対し複数のプリカーサイオン候補を挙げておくことにより、該分画試料の含有物質を同定できる確率を高めることができる。
【0019】
また本発明に係る質量分析装置において好ましくは、前記同定手段により当該分画試料に含まれる物質が同定できない場合に、前記MSn分析実行手段は、該分画試料に対し前記プリカーサイオン候補選択手段により選択されたプリカーサイオン候補のうちの別の1つをプリカーサイオンに設定したMSn分析を実行し、前記同定手段は、その異なるプリカーサイオンに対するMSn分析実行結果に基づいて該分画試料に含まれる物質の同定を試みる構成とするとよい。
【0020】
上述したように、通常、1つの分画試料に対して複数のプリカーサイオン候補が挙げられ、或る1つのプリカーサイオンを設定したMSn分析結果から物質同定ができない場合でも、別のプリカーサイオンを設定したMSn分析結果から物質同定ができる可能性は十分にある。そのため、上記好ましい構成によれば、分画試料に含まれる物質を同定できる確率を一層高めることができる。
【0021】
また本発明に係る質量分析装置では、前記分画試料選択手段により選択された全ての分画試料に対する物質同定が終了した後に、該分画試料選択手段は、第1閾値を第2閾値よりも大きい範囲で減少させた上でピークを抽出し、新たに抽出されるピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択し、その選択された分画試料について、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を実行する構成とするとよい。
【0022】
またこうした構成においては、第1閾値を第2閾値よりも大きい範囲で減少させる毎に、前記分画試料選択手段、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を繰り返し、同定される物質の数が飽和した段階、又は新たに同定される物質の数の増加の程度がそれ以前に比較して大きく減じた段階で、繰り返しを打ち切るようにするとよい。もちろん、同定される物質の数とは無関係に、繰り返しの回数の制約や処理の時間の制約などに基づいて、上記繰り返しを打ち切るようにしてもよい。
【0023】
上記構成では、多数の分画試料の中からMSn分析対象の分画試料を選択するために利用されるピークを検出するための第1閾値が徐々に引き下げられるため、選択される分画試料の総数(累計数)が増加してゆく。つまり、同定対象である物質が含まれる可能性が高い分画試料から、その可能性が低い分画試料にMSn分析及び同定処理の適用範囲が拡げられてゆく。このため、当初の第1閾値の設定に対して求まった分画試料だけでは十分な数の物質同定がなされなかった場合でも、比較的少ない繰り返し回数で以て、つまりは、MSn分析対象の分画試料の数をそれほど増やすことなく、元の試料に含まれる物質の大部分を同定することが可能となる。
【0024】
なお、本発明に係る質量分析装置では、nを2に固定し、MSn分析としてMS2分析のみを実行するようにしてもよいが、対象物質によっては、1回の解離操作だけではデータベース検索等の同定処理が可能な程度の小さな断片にならないことがある。そこで、MS2分析結果から物質同定ができない場合に、MS2分析により得られるMS2スペクトルの中で例えば信号強度の最大のピークをプリカーサイオンとしてMS3分析を実行し、MS3分析結果から物質同定を行う、というようにnが3以上であるMSn分析を行ってそのMSn分析結果から物質を同定するようにしてもよい。
【発明の効果】
【0025】
本発明に係る質量分析装置によれば、元の試料を分取・分画することで得られた多数の分画試料の中で、比較的少数の分画試料に対するMSn分析を行うことにより、元の試料に含まれる多数の物質を正確に同定することが可能となる。それにより、分析に要する手間や時間を節約して効率のよい分析を行いつつ、同定漏れを少なくすることができる。
【図面の簡単な説明】
【0026】
【図1】本発明の一実施例によるLC/MALDI−MSの概略構成図。
【図2】本実施例のLC/MALDI−MSにおけるMS2分析対象分画試料を選択する際の処理の概念図。
【図3】本実施例のLC/MALDI−MSにおいて、サンプルプレート上の各ウェルに調製された分画試料に含まれる物質を網羅的に同定する際の処理及び制御動作を示すフローチャート。
【図4】MS2分析の対象である選択ウェル数と同定されたペプチド数との関係の実験結果を示す図。
【図5】連結ピークリストを3次元グラフ化した図。
【図6】或る試料に対するTICと該試料に含まれるm/z1956である物質のMCとの測定結果例を示す図。
【図7】検出される2Dピークと分画との関係を示す図。
【発明を実施するための形態】
【0027】
以下、本発明の一実施例であるLC/MALDI−MSについて、添付図面を参照して説明する。図1は本実施例のLC/MALDI−MSの概略構成図である。
【0028】
本実施例のLC/MALDI−MSは、液体試料中の各種物質を保持時間に応じて分離するLC部1と、LC部1で分離された物質を含む試料を分取・分画してそれぞれ異なる分画試料を調製する分取分画部2と、複数の分画試料のうちの1つを選択して質量分析に供する試料交換部3と、分画試料に対する質量分析(MS1分析、及びnが2以上であるMSn分析)を実行するMS部4と、MS部4により得られたデータを処理するデータ処理部5と、LC部1や分取分画部2等の各部の動作を制御するとともにデータ処理部5による処理結果に基づいて試料交換部3やMS部4の動作を制御する分析制御部6と、分析条件等を設定するための入力部7、分析結果などを表示する表示部8、を備える。
【0029】
MS部4は、MALDIイオン源、イオンを保持するとともに質量電荷比に応じてイオンを分離する機能や衝突誘起解離(CID)によりイオンを解離させる機能を有するイオントラップ、イオントラップから放出された各種イオンを質量電荷比に応じて分離して検出する飛行時間型質量分析計、などを含み、MS1分析だけでなく、イオン選択とイオン解離とを繰り返すMSn分析が可能となっている。ただし、MS1分析及びMS2分析のみを実行すればよい場合(nが3以上のMSn分析が不要である場合)には、三連四重極型質量分析計のような、より簡単な構成のMSn型質量分析装置を利用することができる。
【0030】
また、データ処理部5は、スペクトルデータ収集部51、2Dピーク検出部52、MSn分析制御情報生成部53、同定処理部54などの機能ブロックを備える。データ処理部5や分析制御部6は、例えばパーソナルコンピュータをハードウエア資源とし、該パーソナルコンピュータにインストールされた専用の制御・処理ソフトウエアを実行することにより、上記のような各機能ブロックが具現化される構成とすることができる。
【0031】
LC部1は注入された試料に含まれる各種物質を時間方向に分離する。したがって、LC部1から出てくる溶出液中に含まれる物質は時間経過に伴って変化する。分取分画部2はこの溶出液を所定の時間間隔で分画し、分画した溶出液をMALDI用のサンプルプレート上に形成された異なるウェルに順次滴下し、それぞれのウェルに分画試料を調製する。即ち、各ウェルの分画試料は順次異なる保持時間、より厳密に言えば、保持時間が或る保持時間の範囲に入る物質を含む。もちろん、溶出液中で或る1つの物質が溶出してくる時間には幅があるから、1つの物質が複数の分画試料に含まれることもある。
【0032】
分取分画部2において多数の分画試料が調製されたサンプルプレートは試料交換部3に搬送され、試料交換部3は分析制御部6の制御の下に、MS部4のMALDIイオン源でイオン化が行われる位置(つまりMALDI用のレーザ光照射位置)に分析対象である分画試料が来るようにサンプルプレートを移動させる。これにより、多数の分画試料の中の任意の分画試料に対するMS1分析やMSn分析が行われる。
【0033】
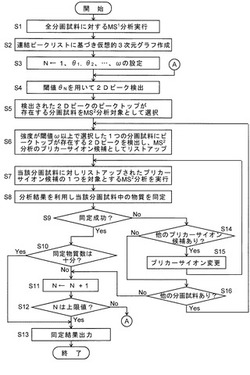
上述したようにサンプルプレート上の各ウェルに調製された分画試料に含まれる物質を網羅的に同定する際の処理及び制御動作を図2、図3により説明する。図3はこの網羅的同定処理及び制御の動作手順を示すフローチャート、図2はMS2分析対象である分画試料を選択する際の処理の概念図である。
【0034】
まず、サンプルプレート上の各ウェルに調製された分画試料の1つ1つについてそれぞれ、MS部4によりMS1分析を実行し、スペクトルデータ収集部51はMS1スペクトルデータを取得する(ステップS1)。スペクトルデータ収集部51は、各MS1スペクトルに対してピーク検出処理を実行し、ピークの質量電荷比と信号強度とを含むピーク情報を収集してピークリストを作成する。そして、分画試料毎に得られたピークリストを連結し、この連結ピークリストに基づいて図5に示したような仮想的な3次元グラフを作成する(ステップS2)。この3次元グラフは、保持時間(RT)と質量電荷比(m/z)を直交する2軸とし、この2軸に直交する方向に信号強度をとったものである。図5では、この信号強度軸は色とその濃淡で示されることは前述したとおりである。
【0035】
この仮想的な3次元グラフに対し、2Dピーク検出部52は特徴的な2Dピーク検出を行う。まず、繰り返し変数Nを1にセットし、信号強度を判定する基準である閾値θ1、θ2、…、ωを適宜設定する(ステップS3)。これら閾値は仮想的3次元グラフ中で信号強度が最大であるピークの信号強度を100%としたときの%値で示され、その大小関係はθ1>θ2>…>θm>…≧ωとする(図2(c)参照)。このθ1、θ2、…が第1閾値であり、ωが第2閾値である。2Dピーク検出部52は第1閾値としてθNを用い、上記仮想的3次元グラフにおいて信号強度が第1閾値θN以上である2Dピークを検出する(ステップS4)。ステップS3の直後にS4が実行されるときにはN=1であるから、信号強度が第1閾値θ1以上である2Dピークが検出される。図2(a)、(b)に示すように、θ1は十分に大きい(100%に近い)ため、通常、信号強度がθ1以上であるピークは全ピークの中で僅かである。
【0036】
次に、MSn分析制御情報生成部53は、ステップS4で新たに検出された2Dピークのピークトップの保持時間に対応した分画試料をMS2分析対象である分画試料として定める(ステップS5)。ステップS4で検出された複数の2Dピークが同一の分画試料に対応する場合もあるから、MS2分析対象とされる分画試料の数は検出された2Dピークの数、又はそれ以下となる。当初第1閾値θ1は高く設定されているため、このときにステップS4で検出される2Dピークの数は少なく、ステップS5で選択される分画試料の数も比較的少ない。一方、検出される2Dピークの信号強度は高いことから、ここで選択された分画試料には同定対象である何らかの物質が含まれる可能性が高いと推定される。
【0037】
次いで、2Dピーク検出部52はステップS5で選択された複数の分画試料のうちの1つについて、上記3次元グラフにおいて保持時間と質量電荷比との2軸が含まれる2次元平面上で、その分画試料にピークトップが存在し、且つ信号強度が第2閾値ω以上である2Dピークを検出する。そして、MSn分析制御情報生成部53は、ここで検出された2Dピークを、その1つの分画試料をMS2分析する際のプリカーサイオン候補としてリストアップする(ステップS6)。図2(a)に示すように第2閾値ωは第1閾値θ1に比べると遙かに小さい(0%に近い)から、ステップS4に比べてステップS6では2Dピークは検出され易い。そのため、通常、ステップS4で検出された2Dピークのほかに、ステップS4では検出されなかった1乃至複数の2Dピークが1つの分画試料に対して抽出される。即ち、1つの分画試料に対して複数の、それも比較的多くの数のプリカーサイオン候補が挙げられることになる。これにより、その分画試料に含まれる物質由来のプリカーサイオンが候補漏れとなることを回避できる可能性が高くなる。
【0038】
ステップS6で求まった分画試料とプリカーサイオン候補リストとは分析制御部6に与えられ、分析制御部6は、その分画試料に対しリストアップされたプリカーサイオン候補のうちの1つをプリカーサイオンに設定したMS2分析を実行するように試料交換部3及びMS部4を制御する。スペクトルデータ収集部51はこのMS2分析により得られるMS2スペクトルデータを収集する(ステップS7)。同定処理部54はMS2分析結果、つまりMS2スペクトルデータを用いMS/MSイオンサーチやデノボシーケシングなどの所定のアルゴリズムにより、その分画試料に含まれる物質の同定を行う(ステップS8)。
【0039】
物質同定が成功した(例えばMS/MSイオンサーチを用いた場合であれば、十分に高い信頼度を示すスコアや期待値で以て化合物が特定された)場合には、ステップS9からS10へと進む。一方、同定に失敗した場合にはステップS9からS14へと進み、MSn分析制御情報生成部53は同じ分画試料に対してリストアップされた他のプリカーサイオン候補があるか否かを判定する。他のプリカーサイオン候補があれば、同じ分画試料に対しプリカーサイオンのみを変更して(ステップS15)ステップS7へと戻り、該プリカーサイオンを設定したMS2分析を実行する。したがって、MS2分析結果から物質同定ができない場合には、ステップS7→S8→S9→S14→S15→S7…の繰り返しによって、物質同定がなされるか、或いはプリカーサイオン候補がなくなるまで、同一分画試料に対し異なるプリカーサイオンを解離させるMS2分析を順次実行することになる。
【0040】
或る1つの分画試料についてリストアップされた全てのプリカーサイオン候補についてのMS2分析を実行しても物質同定ができない場合には、ステップS14からS16へと進み、MSn分析制御情報生成部53は、ステップS5で選択され、MS2分析及び同定処理が未だ行われていない他の分画試料があるか否かを判定する。他の分画試料があればステップS6へと戻り、未処理である他の1つの分画試料について上記と同様にMS2分析と同定処理とを実行する。
【0041】
或る分画試料に含まれる物質の同定に成功した場合には、ステップS9からS10へと進み、それまでに同定された物質が十分な個数であるか否かを判定する。元の試料に含有される物質の種類の数が既知である場合や予め所定数以上の物質が同定されればOKであると定められている場合には、上記「十分」な個数を所定個数以上と定めておけばよいが、含有物質の種類の数が未知である場合には、個数の値で以て良否の判定することはできない。そこで、その場合には、同定される物質個数の累積値を順次求め、累積値の変化が小さくなったり変化しなくなったりしたとき、又は、新たに同定される物質個数を順次求め、その伸びが止まったときなどに、同定される物質個数が飽和した(つまり大部分の物質が同定された)と判断するとよい。
【0042】
ステップS10において物質の同定個数が不十分であると判定されたとき、或いは、ステップS16においてMS2分析する分画試料がなくなったと判定された場合には、変数Nをインクリメントする(ステップS11)。そして、その変数Nが予め定めた上限値に達したか否かを判定し(ステップS12)、変数Nが上限値に達していなければステップS4へと戻る。ステップS12で変数Nの上限値を定める理由は、同定された物質の個数が不十分であっても分析時間が異常に長くなることを避けるためである。
【0043】
ステップS12からS4へと戻ったとき、変数Nはそれ以前より1だけ増加しているから、ステップS4の処理が2回目であるときには第1閾値としてθ2を用いた2Dピーク検出が行われる。図2(b)、(c)に示すように、θ2はθ1よりも小さいから、先に第1閾値がθ1であったときに検出されなかった新たな2Dピークが検出されるようになる。したがって、新たな2Dピークのピークトップの保持時間に応じて、ステップS5でも新たな分画試料が選択される。ただし、新たに検出された2Dピークのピークトップが既にMS2分析済みの分画試料に存在している場合には、この分画試料は選択対象から外される。未だMS2分析が実行されていない新たな分画試料が選択された場合には、該分画試料についてステップS6〜S8の処理を実行し、その新たな分画試料に含まれる物質を同定する。
【0044】
ステップS10において同定された物質の個数が十分であると判定されるまで、或いは、ステップS12において変数Nが上限値に達するまで、ステップS11→S12→S4→…の処理が繰り返される。したがって、図2(c)に示すように、分画試料を選択するための2Dピークを検出する第1閾値は徐々に引き下げられ、MS2分析対象となる分画試料の範囲は拡げられてゆく。ただし、MS2分析対象となる分画試料の範囲が拡げられるほど、新たな分画試料において物質が同定される可能性は低くなる。即ち、多くの物質は変数Nが比較的小さい間に同定される。そして、ステップS10において同定された物質の個数が十分であると判定されるか、ステップS12において変数Nが上限値に達したと判定されたならば、同定処理部54は全ての同定結果を表示部8から出力し、処理を終了する。
【0045】
なお、上記説明では、MS2分析結果から物質同定を行うことを前提としていたが、例えば翻訳後修飾されたタンパク質などを対象とする場合には、nが3以上であるMSn分析結果を利用しないと物質同定が的確に行えないことがある。そこで、MS2分析結果から物質同定ができない場合に、MS2分析により得られるMS2スペクトルの中で例えば信号強度の最大のピークをプリカーサイオンとしてMS3分析を実行し、MS3分析結果から物質同定を行う、というように、nが3以上であるMSn分析を行ってそのMSn分析結果から物質の同定を試みるようにしてもよい。
【0046】
次に、上述したLC/MALDI−MSにより、複数種のペプチドを含む試料を分析した実験例について説明する。図4は、上述した本発明による手法と従来法とを用いたときの、選択されたウェル(分画試料)の累積数と同定できたペプチド数との関係を示したものである。ここでいう従来法とは、図3中のステップS6における閾値ωでの2Dピーク検出を行わず、ステップS4で検出された2Dピークをそのままプリカーサイオン候補とする処理を行う方法である。また、この実験例におけるパラメータは、θ1=15、θ2=10、θ3=9、θ5=8、…、θ8=4、θ9=ω=3である。さらに、図4中の点線は、2Dピーク検出を行わずランダムにMS2分析対象のウェルを選択した場合に同定されると期待されるペプチド数を表わしている。
【0047】
図4により、本発明法では従来法と比較して、少ないウェル選択数(この例では150個程度以下)において多くのペプチドが同定されていることが分かる。例えば、18個中15個のペプチドを同定するために、本発明法では60個程度のウェルをMS2分析すればよいのに対し、従来法では100個程度のウェルをMS2分析する必要がある。このように、本発明法によれば、同数のペプチドが同定されるまでの時間を削減することができる。
【0048】
なお、上記実施例は本発明の一実施例であり、本発明の趣旨の範囲で適宜変形、修正、追加を行っても本願特許請求の範囲に包含されることは当然である。
【符号の説明】
【0049】
1…LC部
2…分取分画部
3…試料交換部
4…MS部
5…データ処理部
51…スペクトルデータ収集部
52…2Dピーク検出部
53…MSn分析制御情報生成部
54…同定処理部
6…分析制御部
7…入力部
8…表示部
【技術分野】
【0001】
本発明は、液体クロマトグラフ(LC)、ガスクロマトグラフ(GC)、キャピラリ電気泳動装置(CE)などによって各種物質が分離されて分画された試料に対し、質量分析を行って各物質を同定する質量分析装置に関し、さらに詳しくは、MSn分析(nは2以上の整数)を行うことが可能な質量分析装置に関する。
【背景技術】
【0002】
生命科学の研究や医療、医薬品開発などの分野においては、生体試料を対象として、タンパク質、ペプチド、核酸、糖鎖など様々な物質を網羅的に同定することがますます重要になってきている。特にタンパク質やペプチドを対象とするこうした網羅的な解析手法はショットガン・プロテオミクス(Shotgun Proteomics)と呼ばれている。こうした解析のために、LCやGC、或いはCEなどのクロマトグラフィと、タンデム型質量分析装置(MSn型質量分析装置)とを組み合わせた分析手法が非常に威力を発揮している。
【0003】
タンデム型質量分析装置を用いた生体試料中の各種物質の網羅的同定手法として、従来知られている一つの手法の手順は次のとおりである(非特許文献1参照)。
[ステップ1] 分析対象である試料に含まれる各種物質をLC、CE等により分離し、その溶出液を分取・分画して多数のサンプルを調製する(ここでは、分取・分画により得られた1つ1つのサンプルを「分画試料」と呼ぶこととする)。なお、試料を分取・分画する際には、予め決めた一定の時間間隔で分画を行う又は一定量の試料液を採取するように分画を行うことにより、全ての物質が漏れなくいずれかの分画試料に含まれるようにする(例えば特許文献1参照)。
【0004】
[ステップ2]各分画試料に対するMS1スペクトルをそれぞれ取得し、該MS1スペクトル上で同定対象の物質群に由来すると考えられるピークを選択する。
[ステップ3]上記ステップ2で選択したピークをプリカーサイオンに設定して当該分画試料に対しMS2分析を実行し、その結果に基づいてデータベース検索やデノボシーケンスサーチを行い、分画試料に含まれる物質を同定する。
[ステップ4]十分な確度で特定の物質が同定されなかった場合には、MS1スペクトル上で見つけた別のピークをプリカーサイオンに設定してMS2分析を実行するか、或いは、さらに高次(つまりnが3以上)のMSn分析を実行し、その結果に基づくデータベース検索やデノボシーケンスサーチなどにより、分画試料に含まれる物質を同定する。
[ステップ5]上記ステップ2〜4の処理を複数の分画試料それぞれに対して行い、元の試料に含まれていた様々な物質を網羅的に同定する。
【0005】
LCやGCなどのカラムを用いた分離手法では、試料中の各種物質はカラムを通過するに要する時間(保持時間、以下「RT」と称す)の大きさによって分離される。この場合、MS1分析で検出されたイオン強度の総和を保持時間の経過に沿って表したプロファイルは一般にTIC(トータルイオンクロマトグラム)と呼ばれ、特定の質量電荷比m/zに着目し、その質量電荷比のイオン強度を保持時間の経過に沿って表したプロファイルはMC(マスクロマトグラム)と呼ばれる。
【0006】
上記のような網羅的同定のための分析手法において、高い確度で以て物質を同定するには、同一の分画試料に含まれる物質の種数が少ない(できれば1種類のみである)ことが望ましい。そのためには1つの分画試料を分取する時間を短くすればよいが、その場合、分画数が多くなる。元の試料に含まれていた物質を網羅的に同定するために全ての分画試料を対象としてMSn分析及び同定処理を行う場合、分画数が増えるほど分析や処理に掛かる手間や時間が膨大なものとなる。特に、異なる分画試料を分析する場合には、機械的に試料を交換したり分析対象の試料を分析位置まで搬送したりする必要があるため、分析に要する時間が長くなり、分析対象である分画試料の数が増えると分析効率の低下が顕著である。
【0007】
一般に、全ての分画試料に有意な物質が含まれているというわけではないため、実際には、網羅的同定であっても、必ずしも全ての分画試料を分析する必要はない。そこで、元の試料に含まれていた物質を網羅的且つ効率的に同定するには、同定すべき物質が含まれる可能性が高い分画試料を優先的に選択してMSn分析することが重要である。そのための一つの手法として、各分画試料に含まれる物質の総量に対応するTICをモニタリングし、TICに現れるピークの保持時間に対応した分画試料を優先的にMSn分析することが考えられる。しかしながら、同定対象である物質の質量電荷比におけるMCとTICとを比較したとき、両者のピークの発生位置(つまりは保持時間)が必ずしも一致するとは限らない。
【0008】
図6は、或る試料に対するTICと該試料に含まれるm/z1956である物質のMCとの測定結果例を示す図である。この例では、MCではRT=6100付近で大きなピークが生じているのに対し、TICでは同RTにピークが現れておらず、両者のピークの発生位置は一致しない。このような場合には、TIC上で現れるピークの保持時間に対応した分画試料をMS2分析の対象として選択したとしても、その分画試料には同定対象である物質が十分な濃度で含まれていない可能性がある。一方、同定対象である物質が十分な濃度で含まれる分画試料を選択するには、その物質に対するMCにおいて現れるピークの保持時間に対応した分画試料を選択すればよい。しかしながら、分画試料に含まれる物質が未知である状態においては、いずれの質量電荷比に対応するMCを用いればよいのか判断することはできないため、MCを用いて分画試料を選択することはできない。
【0009】
上記課題を解決するために、従来、非特許文献2に記載の方法が知られている。即ち、まず、各RTでのピークリスト(又はMS1スペクトル)を並べた連結ピークリストを作成する。図5はこの連結ピークリストを3次元グラフ化した図であり、保持時間(RT)と質量電荷比とが紙面上の2軸であり、各ピークの信号強度は色とその濃淡という別の軸で示される。なお、この図5中の横方向の2本の点線で挟まれた保持時間範囲が図6に示したTIC及びMCの時間範囲であり、図5中の縦方向の点線がm/z1956のMCに対応したピークデータである。
【0010】
次に、この3次元グラフに対し2次元平面上でピーク検出を行う。以下、このピーク検出を「2Dピーク検出」といい、これにより検出されたピークを「2Dピーク」ということとする。図7に示すように、或る分画に対応するRT(図7中に横方向の点線で示すRT)には、幾つかの質量電荷比において2Dピークが観測される。このように分画された分画試料には同定対象である物質の少なくとも1つが含まれている可能性が高いと判断できるので、この分画試料をMS2分析の対象として選択する。さらに、このときに見つかった2Dピーク(図7中に○囲みで示した点で示されるピーク)は、当該分画に含まれていた物質を同定するためのMS2分析のプリカーサイオン候補となり、その分画に含まれる物質が同定されるまで順次nの数を増加させる(開裂の段数を増加させる)MSn分析を行う対象となる。
【0011】
上述した2Dピーク検出に基づく分画試料の選択処理においては、予め定めた閾値を超えるような信号強度を有する2DピークがMS2分析のプリカーサイオン候補として抽出される。そのため、抽出される2Dピークの数は閾値によって変化し、結果として、選択される分画試料の数やリストアップされるプリカーサイオン候補の数も閾値によって増減することになる。閾値が小さい場合には信号強度が比較的小さな2Dピークも選出されるため、プリカーサイオン候補のリストアップ漏れを軽減することができる。その反面、MSn分析の対象とされる分画試料の数も多くなるため、分析や処理の手間が増大し、分析効率の低下に繋がる。一方、閾値を大きくした場合には、MSn分析の対象として選択される分画試料の数を抑えることができるものの、プリカーサイオン候補の数も少なくなるため、選択された分画試料において物質同定に失敗する可能性が高まる。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】特開2010−14559号公報
【非特許文献】
【0013】
【非特許文献1】エドワード・エム・マーコッテ(Edward M Marcotte)、「ハウ・ドゥー・ショットガン・プロテオミクス・アルゴリズムズ・アイデンティファイ・プロテインズ?(How do shotgun proteomics algorithms identify proteins?)」、ネイチャー・バイオテクノロジー(Nature Biotechnology) 25、2007年、p.755-757
【非特許文献2】ユルゲン・コックス(Jurugen Cox)、ほか1名、「マックスクァント・イネーブル・ハイ・アイデンティフィケイション・レイツ、インディビデュアライズド・ピーピービー-レンジ・マス・アキュラサイズ・アンド・プロテオーム-ワイド・プロテイン・クォンティフィケイション(MaxQuant enable high peptide identification rates, individualized p.p.b.-range mass accuracies and proteome-wide protein quantification )」、ネイチャー・バイオテクノロジー(Nature Biotechnology) 26、2008年、p.1367-1372
【発明の概要】
【発明が解決しようとする課題】
【0014】
本発明は上記課題を解決するために成されたものであり、その目的とするところは、例えば保持時間と質量電荷比とを2軸とする2次元平面上で上記のような2Dピーク検出によりMSn分析の対象とする分画試料とMSn分析のプリカーサイオン候補とを抽出する場合に、分析対象とする分画試料の数をできるだけ抑えることによって分析の手間や時間の節約を図りつつ、プリカーサイオン候補の漏れをなくして、同定の失敗を少なくしたり同定の正確性を向上させたりすることができる質量分析装置を提供することにある。
【課題を解決するための手段】
【0015】
上記課題を解決するために成された本発明は、試料に含まれる各種物質を分離用パラメータに従って分離した後に分取・分画して調製された複数の分画試料に対し、MSn分析(nは2以上の整数)をそれぞれ実行することが可能な質量分析装置であって、
a)全ての分画試料に対するMS1分析をそれぞれ実行して得られたMS1スペクトルデータに基づいて、分離用パラメータ及び質量電荷比を2軸とする2次元平面を形成し、該平面に直交する軸に信号強度をとった仮想的な3次元グラフを作成し、該3次元グラフに対し信号強度が第1閾値以上であるピークを抽出し、該ピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択する分画試料選択手段と、
b)前記3次元グラフに対し信号強度が前記第1閾値よりも小さな第2閾値以上であって、前記分画試料選択手段により選択された分画試料に対応する前記分離用パラメータにピークトップが存在するピークを抽出し、該ピークのピークトップに対応した質量電荷比をプリカーサイオンの候補として選択するプリカーサイオン候補選択手段と、
c)前記分画試料選択手段により選択された分画試料に対し、前記プリカーサイオン候補選択手段により該分画試料に対応して選択されたプリカーサイオン候補のうちの1つをプリカーサイオンに設定したMSn分析を実行するMSn分析実行手段と、
d)前記MSn分析実行手段によるMSn分析実行結果に基づいてその分画試料に含まれる物質の同定を行う同定手段と、
を備えることを特徴としている。
【0016】
試料に含まれる各種物質を分離する手段がLCやGCなど、カラムを用いたものである場合には、上記分離用パラメータとは時間(保持時間)である。また、試料に含まれる各種物質を分離する手段がCEである場合には、上記分離用パラメータとは移動度である。即ち、試料に含まれる各種物質を分離する手段が例えばLCである場合には、複数の分画試料はそれぞれ異なる保持時間(厳密には所定の保持時間範囲)において採取(分取)された試料である。
【0017】
本発明に係る質量分析装置において、分画試料選択手段及びプリカーサイオン候補選択手段はいずれも、分離用パラメータ、質量電荷比、及び信号強度を3つの軸にとった仮想的な3次元グラフに対し、信号強度が閾値以上であるか否かを判定することによりピークを検出する。ただし、多数の分画試料の中からMSn分析対象の分画試料を選択するために利用されるピークを検出するための第1閾値は、MSn分析のプリカーサイオン候補を選択するために利用されるピークを検出するための第2閾値よりも大きい。即ち、前者は後者よりも、より厳しい基準で以てピークを検出することになるから、MSn分析の対象となる分画試料は比較的高い濃度で何らかの物質を含む分画試料に限られる。一方、プリカーサイオン候補となるピークを検出する基準は相対的に緩いから、1つの分画試料に対して挙げられるプリカーサイオン候補の数は比較的多くなる傾向にある。
【0018】
即ち、一般的に、MSn分析の対象となる分画試料の数が少ない段階でも、各分画試料中の物質の同定に有益であるプリカーサイオンの候補がそれぞれ複数挙げられる可能性が高くなる。一般に、MS1スペクトル中のピークの中で信号強度が最大であるピークをプリカーサイオンとしてMS2分析を行った結果を利用して含有物質の同定に成功しない場合であっても、同じMS1スペクトル中で信号強度が最大ではないピークをプリカーサイオンとしてMS2分析を行った結果を利用して含有物質の同定に成功することもある。したがって、或る1つの分画試料に対し複数のプリカーサイオン候補を挙げておくことにより、該分画試料の含有物質を同定できる確率を高めることができる。
【0019】
また本発明に係る質量分析装置において好ましくは、前記同定手段により当該分画試料に含まれる物質が同定できない場合に、前記MSn分析実行手段は、該分画試料に対し前記プリカーサイオン候補選択手段により選択されたプリカーサイオン候補のうちの別の1つをプリカーサイオンに設定したMSn分析を実行し、前記同定手段は、その異なるプリカーサイオンに対するMSn分析実行結果に基づいて該分画試料に含まれる物質の同定を試みる構成とするとよい。
【0020】
上述したように、通常、1つの分画試料に対して複数のプリカーサイオン候補が挙げられ、或る1つのプリカーサイオンを設定したMSn分析結果から物質同定ができない場合でも、別のプリカーサイオンを設定したMSn分析結果から物質同定ができる可能性は十分にある。そのため、上記好ましい構成によれば、分画試料に含まれる物質を同定できる確率を一層高めることができる。
【0021】
また本発明に係る質量分析装置では、前記分画試料選択手段により選択された全ての分画試料に対する物質同定が終了した後に、該分画試料選択手段は、第1閾値を第2閾値よりも大きい範囲で減少させた上でピークを抽出し、新たに抽出されるピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択し、その選択された分画試料について、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を実行する構成とするとよい。
【0022】
またこうした構成においては、第1閾値を第2閾値よりも大きい範囲で減少させる毎に、前記分画試料選択手段、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を繰り返し、同定される物質の数が飽和した段階、又は新たに同定される物質の数の増加の程度がそれ以前に比較して大きく減じた段階で、繰り返しを打ち切るようにするとよい。もちろん、同定される物質の数とは無関係に、繰り返しの回数の制約や処理の時間の制約などに基づいて、上記繰り返しを打ち切るようにしてもよい。
【0023】
上記構成では、多数の分画試料の中からMSn分析対象の分画試料を選択するために利用されるピークを検出するための第1閾値が徐々に引き下げられるため、選択される分画試料の総数(累計数)が増加してゆく。つまり、同定対象である物質が含まれる可能性が高い分画試料から、その可能性が低い分画試料にMSn分析及び同定処理の適用範囲が拡げられてゆく。このため、当初の第1閾値の設定に対して求まった分画試料だけでは十分な数の物質同定がなされなかった場合でも、比較的少ない繰り返し回数で以て、つまりは、MSn分析対象の分画試料の数をそれほど増やすことなく、元の試料に含まれる物質の大部分を同定することが可能となる。
【0024】
なお、本発明に係る質量分析装置では、nを2に固定し、MSn分析としてMS2分析のみを実行するようにしてもよいが、対象物質によっては、1回の解離操作だけではデータベース検索等の同定処理が可能な程度の小さな断片にならないことがある。そこで、MS2分析結果から物質同定ができない場合に、MS2分析により得られるMS2スペクトルの中で例えば信号強度の最大のピークをプリカーサイオンとしてMS3分析を実行し、MS3分析結果から物質同定を行う、というようにnが3以上であるMSn分析を行ってそのMSn分析結果から物質を同定するようにしてもよい。
【発明の効果】
【0025】
本発明に係る質量分析装置によれば、元の試料を分取・分画することで得られた多数の分画試料の中で、比較的少数の分画試料に対するMSn分析を行うことにより、元の試料に含まれる多数の物質を正確に同定することが可能となる。それにより、分析に要する手間や時間を節約して効率のよい分析を行いつつ、同定漏れを少なくすることができる。
【図面の簡単な説明】
【0026】
【図1】本発明の一実施例によるLC/MALDI−MSの概略構成図。
【図2】本実施例のLC/MALDI−MSにおけるMS2分析対象分画試料を選択する際の処理の概念図。
【図3】本実施例のLC/MALDI−MSにおいて、サンプルプレート上の各ウェルに調製された分画試料に含まれる物質を網羅的に同定する際の処理及び制御動作を示すフローチャート。
【図4】MS2分析の対象である選択ウェル数と同定されたペプチド数との関係の実験結果を示す図。
【図5】連結ピークリストを3次元グラフ化した図。
【図6】或る試料に対するTICと該試料に含まれるm/z1956である物質のMCとの測定結果例を示す図。
【図7】検出される2Dピークと分画との関係を示す図。
【発明を実施するための形態】
【0027】
以下、本発明の一実施例であるLC/MALDI−MSについて、添付図面を参照して説明する。図1は本実施例のLC/MALDI−MSの概略構成図である。
【0028】
本実施例のLC/MALDI−MSは、液体試料中の各種物質を保持時間に応じて分離するLC部1と、LC部1で分離された物質を含む試料を分取・分画してそれぞれ異なる分画試料を調製する分取分画部2と、複数の分画試料のうちの1つを選択して質量分析に供する試料交換部3と、分画試料に対する質量分析(MS1分析、及びnが2以上であるMSn分析)を実行するMS部4と、MS部4により得られたデータを処理するデータ処理部5と、LC部1や分取分画部2等の各部の動作を制御するとともにデータ処理部5による処理結果に基づいて試料交換部3やMS部4の動作を制御する分析制御部6と、分析条件等を設定するための入力部7、分析結果などを表示する表示部8、を備える。
【0029】
MS部4は、MALDIイオン源、イオンを保持するとともに質量電荷比に応じてイオンを分離する機能や衝突誘起解離(CID)によりイオンを解離させる機能を有するイオントラップ、イオントラップから放出された各種イオンを質量電荷比に応じて分離して検出する飛行時間型質量分析計、などを含み、MS1分析だけでなく、イオン選択とイオン解離とを繰り返すMSn分析が可能となっている。ただし、MS1分析及びMS2分析のみを実行すればよい場合(nが3以上のMSn分析が不要である場合)には、三連四重極型質量分析計のような、より簡単な構成のMSn型質量分析装置を利用することができる。
【0030】
また、データ処理部5は、スペクトルデータ収集部51、2Dピーク検出部52、MSn分析制御情報生成部53、同定処理部54などの機能ブロックを備える。データ処理部5や分析制御部6は、例えばパーソナルコンピュータをハードウエア資源とし、該パーソナルコンピュータにインストールされた専用の制御・処理ソフトウエアを実行することにより、上記のような各機能ブロックが具現化される構成とすることができる。
【0031】
LC部1は注入された試料に含まれる各種物質を時間方向に分離する。したがって、LC部1から出てくる溶出液中に含まれる物質は時間経過に伴って変化する。分取分画部2はこの溶出液を所定の時間間隔で分画し、分画した溶出液をMALDI用のサンプルプレート上に形成された異なるウェルに順次滴下し、それぞれのウェルに分画試料を調製する。即ち、各ウェルの分画試料は順次異なる保持時間、より厳密に言えば、保持時間が或る保持時間の範囲に入る物質を含む。もちろん、溶出液中で或る1つの物質が溶出してくる時間には幅があるから、1つの物質が複数の分画試料に含まれることもある。
【0032】
分取分画部2において多数の分画試料が調製されたサンプルプレートは試料交換部3に搬送され、試料交換部3は分析制御部6の制御の下に、MS部4のMALDIイオン源でイオン化が行われる位置(つまりMALDI用のレーザ光照射位置)に分析対象である分画試料が来るようにサンプルプレートを移動させる。これにより、多数の分画試料の中の任意の分画試料に対するMS1分析やMSn分析が行われる。
【0033】
上述したようにサンプルプレート上の各ウェルに調製された分画試料に含まれる物質を網羅的に同定する際の処理及び制御動作を図2、図3により説明する。図3はこの網羅的同定処理及び制御の動作手順を示すフローチャート、図2はMS2分析対象である分画試料を選択する際の処理の概念図である。
【0034】
まず、サンプルプレート上の各ウェルに調製された分画試料の1つ1つについてそれぞれ、MS部4によりMS1分析を実行し、スペクトルデータ収集部51はMS1スペクトルデータを取得する(ステップS1)。スペクトルデータ収集部51は、各MS1スペクトルに対してピーク検出処理を実行し、ピークの質量電荷比と信号強度とを含むピーク情報を収集してピークリストを作成する。そして、分画試料毎に得られたピークリストを連結し、この連結ピークリストに基づいて図5に示したような仮想的な3次元グラフを作成する(ステップS2)。この3次元グラフは、保持時間(RT)と質量電荷比(m/z)を直交する2軸とし、この2軸に直交する方向に信号強度をとったものである。図5では、この信号強度軸は色とその濃淡で示されることは前述したとおりである。
【0035】
この仮想的な3次元グラフに対し、2Dピーク検出部52は特徴的な2Dピーク検出を行う。まず、繰り返し変数Nを1にセットし、信号強度を判定する基準である閾値θ1、θ2、…、ωを適宜設定する(ステップS3)。これら閾値は仮想的3次元グラフ中で信号強度が最大であるピークの信号強度を100%としたときの%値で示され、その大小関係はθ1>θ2>…>θm>…≧ωとする(図2(c)参照)。このθ1、θ2、…が第1閾値であり、ωが第2閾値である。2Dピーク検出部52は第1閾値としてθNを用い、上記仮想的3次元グラフにおいて信号強度が第1閾値θN以上である2Dピークを検出する(ステップS4)。ステップS3の直後にS4が実行されるときにはN=1であるから、信号強度が第1閾値θ1以上である2Dピークが検出される。図2(a)、(b)に示すように、θ1は十分に大きい(100%に近い)ため、通常、信号強度がθ1以上であるピークは全ピークの中で僅かである。
【0036】
次に、MSn分析制御情報生成部53は、ステップS4で新たに検出された2Dピークのピークトップの保持時間に対応した分画試料をMS2分析対象である分画試料として定める(ステップS5)。ステップS4で検出された複数の2Dピークが同一の分画試料に対応する場合もあるから、MS2分析対象とされる分画試料の数は検出された2Dピークの数、又はそれ以下となる。当初第1閾値θ1は高く設定されているため、このときにステップS4で検出される2Dピークの数は少なく、ステップS5で選択される分画試料の数も比較的少ない。一方、検出される2Dピークの信号強度は高いことから、ここで選択された分画試料には同定対象である何らかの物質が含まれる可能性が高いと推定される。
【0037】
次いで、2Dピーク検出部52はステップS5で選択された複数の分画試料のうちの1つについて、上記3次元グラフにおいて保持時間と質量電荷比との2軸が含まれる2次元平面上で、その分画試料にピークトップが存在し、且つ信号強度が第2閾値ω以上である2Dピークを検出する。そして、MSn分析制御情報生成部53は、ここで検出された2Dピークを、その1つの分画試料をMS2分析する際のプリカーサイオン候補としてリストアップする(ステップS6)。図2(a)に示すように第2閾値ωは第1閾値θ1に比べると遙かに小さい(0%に近い)から、ステップS4に比べてステップS6では2Dピークは検出され易い。そのため、通常、ステップS4で検出された2Dピークのほかに、ステップS4では検出されなかった1乃至複数の2Dピークが1つの分画試料に対して抽出される。即ち、1つの分画試料に対して複数の、それも比較的多くの数のプリカーサイオン候補が挙げられることになる。これにより、その分画試料に含まれる物質由来のプリカーサイオンが候補漏れとなることを回避できる可能性が高くなる。
【0038】
ステップS6で求まった分画試料とプリカーサイオン候補リストとは分析制御部6に与えられ、分析制御部6は、その分画試料に対しリストアップされたプリカーサイオン候補のうちの1つをプリカーサイオンに設定したMS2分析を実行するように試料交換部3及びMS部4を制御する。スペクトルデータ収集部51はこのMS2分析により得られるMS2スペクトルデータを収集する(ステップS7)。同定処理部54はMS2分析結果、つまりMS2スペクトルデータを用いMS/MSイオンサーチやデノボシーケシングなどの所定のアルゴリズムにより、その分画試料に含まれる物質の同定を行う(ステップS8)。
【0039】
物質同定が成功した(例えばMS/MSイオンサーチを用いた場合であれば、十分に高い信頼度を示すスコアや期待値で以て化合物が特定された)場合には、ステップS9からS10へと進む。一方、同定に失敗した場合にはステップS9からS14へと進み、MSn分析制御情報生成部53は同じ分画試料に対してリストアップされた他のプリカーサイオン候補があるか否かを判定する。他のプリカーサイオン候補があれば、同じ分画試料に対しプリカーサイオンのみを変更して(ステップS15)ステップS7へと戻り、該プリカーサイオンを設定したMS2分析を実行する。したがって、MS2分析結果から物質同定ができない場合には、ステップS7→S8→S9→S14→S15→S7…の繰り返しによって、物質同定がなされるか、或いはプリカーサイオン候補がなくなるまで、同一分画試料に対し異なるプリカーサイオンを解離させるMS2分析を順次実行することになる。
【0040】
或る1つの分画試料についてリストアップされた全てのプリカーサイオン候補についてのMS2分析を実行しても物質同定ができない場合には、ステップS14からS16へと進み、MSn分析制御情報生成部53は、ステップS5で選択され、MS2分析及び同定処理が未だ行われていない他の分画試料があるか否かを判定する。他の分画試料があればステップS6へと戻り、未処理である他の1つの分画試料について上記と同様にMS2分析と同定処理とを実行する。
【0041】
或る分画試料に含まれる物質の同定に成功した場合には、ステップS9からS10へと進み、それまでに同定された物質が十分な個数であるか否かを判定する。元の試料に含有される物質の種類の数が既知である場合や予め所定数以上の物質が同定されればOKであると定められている場合には、上記「十分」な個数を所定個数以上と定めておけばよいが、含有物質の種類の数が未知である場合には、個数の値で以て良否の判定することはできない。そこで、その場合には、同定される物質個数の累積値を順次求め、累積値の変化が小さくなったり変化しなくなったりしたとき、又は、新たに同定される物質個数を順次求め、その伸びが止まったときなどに、同定される物質個数が飽和した(つまり大部分の物質が同定された)と判断するとよい。
【0042】
ステップS10において物質の同定個数が不十分であると判定されたとき、或いは、ステップS16においてMS2分析する分画試料がなくなったと判定された場合には、変数Nをインクリメントする(ステップS11)。そして、その変数Nが予め定めた上限値に達したか否かを判定し(ステップS12)、変数Nが上限値に達していなければステップS4へと戻る。ステップS12で変数Nの上限値を定める理由は、同定された物質の個数が不十分であっても分析時間が異常に長くなることを避けるためである。
【0043】
ステップS12からS4へと戻ったとき、変数Nはそれ以前より1だけ増加しているから、ステップS4の処理が2回目であるときには第1閾値としてθ2を用いた2Dピーク検出が行われる。図2(b)、(c)に示すように、θ2はθ1よりも小さいから、先に第1閾値がθ1であったときに検出されなかった新たな2Dピークが検出されるようになる。したがって、新たな2Dピークのピークトップの保持時間に応じて、ステップS5でも新たな分画試料が選択される。ただし、新たに検出された2Dピークのピークトップが既にMS2分析済みの分画試料に存在している場合には、この分画試料は選択対象から外される。未だMS2分析が実行されていない新たな分画試料が選択された場合には、該分画試料についてステップS6〜S8の処理を実行し、その新たな分画試料に含まれる物質を同定する。
【0044】
ステップS10において同定された物質の個数が十分であると判定されるまで、或いは、ステップS12において変数Nが上限値に達するまで、ステップS11→S12→S4→…の処理が繰り返される。したがって、図2(c)に示すように、分画試料を選択するための2Dピークを検出する第1閾値は徐々に引き下げられ、MS2分析対象となる分画試料の範囲は拡げられてゆく。ただし、MS2分析対象となる分画試料の範囲が拡げられるほど、新たな分画試料において物質が同定される可能性は低くなる。即ち、多くの物質は変数Nが比較的小さい間に同定される。そして、ステップS10において同定された物質の個数が十分であると判定されるか、ステップS12において変数Nが上限値に達したと判定されたならば、同定処理部54は全ての同定結果を表示部8から出力し、処理を終了する。
【0045】
なお、上記説明では、MS2分析結果から物質同定を行うことを前提としていたが、例えば翻訳後修飾されたタンパク質などを対象とする場合には、nが3以上であるMSn分析結果を利用しないと物質同定が的確に行えないことがある。そこで、MS2分析結果から物質同定ができない場合に、MS2分析により得られるMS2スペクトルの中で例えば信号強度の最大のピークをプリカーサイオンとしてMS3分析を実行し、MS3分析結果から物質同定を行う、というように、nが3以上であるMSn分析を行ってそのMSn分析結果から物質の同定を試みるようにしてもよい。
【0046】
次に、上述したLC/MALDI−MSにより、複数種のペプチドを含む試料を分析した実験例について説明する。図4は、上述した本発明による手法と従来法とを用いたときの、選択されたウェル(分画試料)の累積数と同定できたペプチド数との関係を示したものである。ここでいう従来法とは、図3中のステップS6における閾値ωでの2Dピーク検出を行わず、ステップS4で検出された2Dピークをそのままプリカーサイオン候補とする処理を行う方法である。また、この実験例におけるパラメータは、θ1=15、θ2=10、θ3=9、θ5=8、…、θ8=4、θ9=ω=3である。さらに、図4中の点線は、2Dピーク検出を行わずランダムにMS2分析対象のウェルを選択した場合に同定されると期待されるペプチド数を表わしている。
【0047】
図4により、本発明法では従来法と比較して、少ないウェル選択数(この例では150個程度以下)において多くのペプチドが同定されていることが分かる。例えば、18個中15個のペプチドを同定するために、本発明法では60個程度のウェルをMS2分析すればよいのに対し、従来法では100個程度のウェルをMS2分析する必要がある。このように、本発明法によれば、同数のペプチドが同定されるまでの時間を削減することができる。
【0048】
なお、上記実施例は本発明の一実施例であり、本発明の趣旨の範囲で適宜変形、修正、追加を行っても本願特許請求の範囲に包含されることは当然である。
【符号の説明】
【0049】
1…LC部
2…分取分画部
3…試料交換部
4…MS部
5…データ処理部
51…スペクトルデータ収集部
52…2Dピーク検出部
53…MSn分析制御情報生成部
54…同定処理部
6…分析制御部
7…入力部
8…表示部
【特許請求の範囲】
【請求項1】
試料に含まれる各種物質を分離用パラメータに従って分離した後に分取・分画して調製された複数の分画試料に対し、MSn分析(nは2以上の整数)をそれぞれ実行することが可能な質量分析装置であって、
a)全ての分画試料に対するMS1分析をそれぞれ実行して得られたMS1スペクトルデータに基づいて、分離用パラメータ及び質量電荷比を2軸とする2次元平面を形成し、該平面に直交する軸に信号強度をとった仮想的な3次元グラフを作成し、該3次元グラフに対し信号強度が第1閾値以上であるピークを抽出し、該ピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択する分画試料選択手段と、
b)前記3次元グラフに対し信号強度が前記第1閾値よりも小さな第2閾値以上であって、前記分画試料選択手段により選択された分画試料に対応する前記分離用パラメータにピークトップが存在するピークを抽出し、該ピークのピークトップに対応した質量電荷比をプリカーサイオンの候補として選択するプリカーサイオン候補選択手段と、
c)前記分画試料選択手段により選択された分画試料に対し、前記プリカーサイオン候補選択手段により該分画試料に対応して選択されたプリカーサイオン候補のうちの1つをプリカーサイオンに設定したMSn分析を実行するMSn分析実行手段と、
d)前記MSn分析実行手段によるMSn分析実行結果に基づいてその分画試料に含まれる物質の同定を行う同定手段と、
を備えることを特徴とする質量分析装置。
【請求項2】
請求項1に記載の質量分析装置であって、
前記同定手段により当該分画試料に含まれる物質が同定できない場合に、前記MSn分析実行手段は、該分画試料に対し前記プリカーサイオン候補選択手段により選択されたプリカーサイオン候補のうちの別の1つをプリカーサイオンに設定したMSn分析を実行し、前記同定手段は、その異なるプリカーサイオンに対するMSn分析実行結果に基づいて該分画試料に含まれる物質の同定を試みることを特徴とする質量分析装置。
【請求項3】
請求項1又は2に記載の質量分析装置であって、
前記分画試料選択手段により選択された全ての分画試料に対する物質同定が終了した後に、該分画試料選択手段は、第1閾値を第2閾値よりも大きい範囲で減少させた上でピークを抽出し、新たに抽出されるピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択し、その選択された分画試料について、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を実行することを特徴とする質量分析装置。
【請求項4】
請求項3に記載の質量分析装置であって、
前記第1閾値を第2閾値よりも大きい範囲で減少させる毎に、前記分画試料選択手段、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を繰り返し、同定される物質の数が飽和した段階、又は新たに同定される物質の数の増加の程度がそれ以前に比較して大きく減じた段階で、繰り返しを打ち切ることを特徴とする質量分析装置。
【請求項1】
試料に含まれる各種物質を分離用パラメータに従って分離した後に分取・分画して調製された複数の分画試料に対し、MSn分析(nは2以上の整数)をそれぞれ実行することが可能な質量分析装置であって、
a)全ての分画試料に対するMS1分析をそれぞれ実行して得られたMS1スペクトルデータに基づいて、分離用パラメータ及び質量電荷比を2軸とする2次元平面を形成し、該平面に直交する軸に信号強度をとった仮想的な3次元グラフを作成し、該3次元グラフに対し信号強度が第1閾値以上であるピークを抽出し、該ピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択する分画試料選択手段と、
b)前記3次元グラフに対し信号強度が前記第1閾値よりも小さな第2閾値以上であって、前記分画試料選択手段により選択された分画試料に対応する前記分離用パラメータにピークトップが存在するピークを抽出し、該ピークのピークトップに対応した質量電荷比をプリカーサイオンの候補として選択するプリカーサイオン候補選択手段と、
c)前記分画試料選択手段により選択された分画試料に対し、前記プリカーサイオン候補選択手段により該分画試料に対応して選択されたプリカーサイオン候補のうちの1つをプリカーサイオンに設定したMSn分析を実行するMSn分析実行手段と、
d)前記MSn分析実行手段によるMSn分析実行結果に基づいてその分画試料に含まれる物質の同定を行う同定手段と、
を備えることを特徴とする質量分析装置。
【請求項2】
請求項1に記載の質量分析装置であって、
前記同定手段により当該分画試料に含まれる物質が同定できない場合に、前記MSn分析実行手段は、該分画試料に対し前記プリカーサイオン候補選択手段により選択されたプリカーサイオン候補のうちの別の1つをプリカーサイオンに設定したMSn分析を実行し、前記同定手段は、その異なるプリカーサイオンに対するMSn分析実行結果に基づいて該分画試料に含まれる物質の同定を試みることを特徴とする質量分析装置。
【請求項3】
請求項1又は2に記載の質量分析装置であって、
前記分画試料選択手段により選択された全ての分画試料に対する物質同定が終了した後に、該分画試料選択手段は、第1閾値を第2閾値よりも大きい範囲で減少させた上でピークを抽出し、新たに抽出されるピークのピークトップが現れる前記2次元平面上の位置に対応した分画試料をMSn分析対象の分画試料として選択し、その選択された分画試料について、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を実行することを特徴とする質量分析装置。
【請求項4】
請求項3に記載の質量分析装置であって、
前記第1閾値を第2閾値よりも大きい範囲で減少させる毎に、前記分画試料選択手段、前記プリカーサイオン候補選択手段、前記MSn分析実行手段、及び前記同定手段による処理を繰り返し、同定される物質の数が飽和した段階、又は新たに同定される物質の数の増加の程度がそれ以前に比較して大きく減じた段階で、繰り返しを打ち切ることを特徴とする質量分析装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2013−88215(P2013−88215A)
【公開日】平成25年5月13日(2013.5.13)
【国際特許分類】
【出願番号】特願2011−227620(P2011−227620)
【出願日】平成23年10月17日(2011.10.17)
【出願人】(000001993)株式会社島津製作所 (3,708)
【Fターム(参考)】
【公開日】平成25年5月13日(2013.5.13)
【国際特許分類】
【出願日】平成23年10月17日(2011.10.17)
【出願人】(000001993)株式会社島津製作所 (3,708)
【Fターム(参考)】
[ Back to top ]

