Fターム[4B029CC03]の内容
微生物・酵素関連装置 (40,912) | 生物材料の存在状態 (7,687) | 固定 (1,880)
Fターム[4B029CC03]の下位に属するFターム
Fターム[4B029CC03]に分類される特許
1,521 - 1,540 / 1,741
遺伝子
本発明は、B-Raf遺伝子生成物中の突然変異に関する。記載する突然変異は、天然由来源のヒト腫瘍において同定される。これらの突然変異は、癌性表現型に関連し、ヒト被験体における癌の診断、癌性細胞、または癌に対する素因の基準として、および抗癌治療薬の開発のために使用され得る。 (もっと読む)
反応容器及びその反応容器を用いた反応装置並びに検出装置
【課題】CCDカメラ等の検出手段の撮像画像の方向とスポットの配列方向とを一致させるための技術、具体的には、反応容器の方向を検知し、または補正することの可能な技術を提供すること。
【解決手段】生体関連物質を検出するためのプローブを固相化した基材(102)を有する反応容器(101)において、前記基材の反応を検出するための検出手段(129)の検出方向と前記基材の方向とを一致させるための補正手段(105、106、107、108、109)を備えた。
(もっと読む)
膀胱癌を検出するための尿マーカー
腫瘍の早期発見は、膀胱腫瘍を含む腫瘍に罹患している患者の生存期間の主要な決定要因である。BTMまたはUBTMファミリーメンバーは、膀胱腫瘍組織および他の腫瘍組織において高度にまた一貫して蓄積されることができ、および/または患者の尿に蓄積されることができる。したがって、それらは膀胱癌および他の型の癌に対するマーカーである。ある実施態様では、BTMまたはUBTMが尿に蓄積することができ、UBTMファミリーメンバーの検出が有効な診断手法になりえる。いくつかの実施態様では、定量的PCR法がマイクロアレイ法に優る長所を持つ。他の実施態様では、複数のBTMまたはUBTMの検出および定量化が、膀胱癌検出の感度および特異性を増大させることができ、したがって、膀胱癌の病期および型を決定するための方法を提供する。キットは、本発明の方法を実行するための容易で便利な手段を提供する。 (もっと読む)
反応検出チップ
【課題】スポットのサイズが縮小され、単位面積あたりに積載されるスポットの数と種類とが増大された、高いスポット密度を有する3次元配置プローブ型反応検出チップを提供する。
【解決手段】少なくともその表面の一部に複数の穴を有する基板と;該穴の中にそれぞれ分離して埋め込まれた多孔質物質と;該多孔質物質の細孔表面を含む表面に固定されたプローブ分子と;を含んでなる、プローブ分子が固定された該多孔質物質を反応検出用スポットとして用いる反応検出チップであって、該穴の開口部の大きさが100μm以下である上記反応検出チップである。
(もっと読む)
アトピー性皮膚炎の検査方法
アトピー性皮膚炎患者および乾癬患者において、皮疹部と無疹部の間で発現レベルに差が見られる遺伝子を見出した。またこれらの疾患の無疹部と健常者の間で発現レベルに差が見られる遺伝子を見出した。そしてこれらの遺伝子が、アトピー性皮膚炎あるいは乾癬の検査や治療薬のスクリーニングにおいて指標として有用であることを明らかにした。すなわち本発明は、こうして見出された指標遺伝子の発現レベルの比較に基づく、アトピー性皮膚炎または乾癬の検査方法、およびこれらの疾患の治療のための化合物のスクリーニング方法を提供する。 (もっと読む)
生体関連物質検出用固相化担体及びプローブの固相化方法、並びに生体関連物質解析方法
【課題】 高い信頼性をもって、かつ効率よく、試料中の生体関連物質を解析することを可能ならしめる生体関連物質検出用固相化担体及びプローブの固相化方法、並びに生体関連物質解析方法を提供する。
【解決手段】 生体関連物質を検出するための複数種のプローブが、同一アドレスに固相化されており、該固相化された比率が既知である生体関連物質検出用固相化担体。及び、1以上の生体関連物質を検出するための複数種のプローブを準備する第一ステップ、該複数種のプローブを混合して混合プローブを得る第二ステップ、及び、該混合プローブを担体の同一アドレスに接触させる第三ステップを有し、かつ、該複数種のプローブの比率を、第一ステップと第二ステップとの間、もしくは第二ステップと第三ステップとの間、又は第三ステップの後に測定するプローブの固相化方法。並びに、本発明の固相化担体を用いる生体関連物質の解析方法。
(もっと読む)
びまん型胃癌を診断する方法
びまん型胃癌(DGC)を検出および診断する客観的な方法を本明細書において記述する。一つの態様において、本診断法は、DGC細胞と正常細胞とを識別するDGC関連遺伝子の発現レベルを決定する段階を含む。本発明は、DGCの治療において有用な治療薬剤をスクリーニングする方法、DGCを治療する方法、およびDGCに対するワクチンを被験者に接種する方法をさらに提供する。 (もっと読む)
撮像装置、生体高分子分析チップ及び分析支援装置
【課題】 低感度であっても蛍光を検知することができる撮像装置を提供すること。
【解決手段】 生体高分子分析チップ1は、透明基板17と、透明基板17上においてダブルゲートトランジスタ20を二次元アレイ状に配列してなる固体撮像デバイス3と、固体撮像デバイス3の受光面上に成膜された反射防止膜35と、反射防止膜35の表面上においてマトリクス状に点在したスポット60,60,…と、を具備する。
(もっと読む)
生体関連物質測定装置及び測定方法
【課題】ランニングコストが安く、検出用プローブが容易に固定化でき、簡便に使用できる生体分子検出素子を提供する。
【解決手段】ソース2、ドレイン3間のゲート絶縁物4の表面に導電性電極5を設けた絶縁ゲート電界効果トランジスタ1を用い、導電性電極5の表面に生体分子検出用プローブ6を固定化する。測定の際には、表面に生体分子検出用プローブ6を固定化した導電性電極5と参照電極7を測定セル8中の試料溶液9中に配置し、参照電極7に電源10により交流電圧を印加し、試料溶液9中に含まれるDNAやタンパク等の測定測定対象物と生体分子検出用プローブ6との結合の前後で変化する絶縁ゲート電界効果トランジスタ1の電気特性変化、すなわちソース2とドレイン3との間を流れる電流値の変化を検出する。
(もっと読む)
転写調節に関与する因子
HDARTは、HDAC(ヒストン脱アセチル化酵素)に結合しリプレッサーとして機能する。また、HDARTは、核内レセプターの転写コアクチベーターとして機能するSkipと直接結合し、核内レセプターの転写を抑制する。さらに、HDARTは核内レセプターの転写コリプレッサーの1つであり、HDACと結合しHDACのヒストン脱アセチル化により強力に転写を抑制し得る。一方、HDARTのドミナントネガティブペプチドも得られ、このペプチドは完全長のHDARTたんぱく質とは逆に転写を活性化することをも確認した。特にこのペプチドによるレチノイン酸レセプターの転写活性化能はall−trans Retinoic Acid(ATRA)を上回る活性を有していた。 (もっと読む)
生体関連物質検出用プローブ及び生体関連物質検出用固相化担体、並びに生体関連物質検出方法
【課題】 複数の生体関連物質を同一プローブスポット内で定量的に検出可能とし、低コストで生産可能な生体関連物質検出用プローブと、生体関連物質検出方法の提供。
【解決手段】 試料中の複数の生体関連物質検出用の、担体に固相化される生体関連物質検出用プローブであって、互いに異種の生体関連物質と特異的に結合可能な複数のプローブ領域を既知の比率で含み、プローブ領域の少なくとも1に他の蛍光物質と蛍光共鳴エネルギー転移(FRET)を生じ得る第一蛍光物質が結合され、少なくとも1に該第一蛍光物質が結合されていない生体関連物質検出用プローブ。試料中の生体関連物質に、第一蛍光物質とFRETを生じ得る第二蛍光物質を結合させて標識試料とし、本発明のプローブを担体に固相化し、標識試料とプローブとを接触させ、第二蛍光物質の励起光を照射し、第二蛍光物質の発光信号及びFRETに特異的な発光信号を検出する生体関連物質検出方法。
(もっと読む)
ヘマトクリット及び酸素バイアスを有するバイオセンサ
バイオセンサのヘマトクリットバイアス及び酸素バイアスを改善するために、メディエイター、すなわちフェナントロリンキノンの異性体である1,10−フェナントロリン−5,6−ジオン及びマンガンなどの金属イオンを、例えばグルコースデヒドロゲナーゼなどの、NAD(P)+に依存する酵素と共に使用するバイオセンサ。このメディエイターと金属イオンを使用するバイオセンサの電極は、約20%から約70%にわたるヘマトクリット範囲及び約1kPaから約20kPaにわたる酸素圧範囲で正確な臨床応答を提供する。  (もっと読む)
(もっと読む)
電磁気誘導を用いたバイオ結合検出装置及びこれによる検出方法
【課題】 電磁気誘導を用いてバイオ結合前後の物性の変化を電気的な信号に変換することにより、バイオ結合の有無を検出する電磁気誘導を用いたバイオ結合検出装置及びこれによる検出方法を提供する。
【解決手段】 一端が固定され、他端は揺動自在に設けられた片持ち梁と、片持ち梁の板面上に形成され、周波数成分を有する信号が加えられる第1の金属と、第1の金属の上部に形成され、分析しようとする試料に関する特定の情報を探索できるプローブ生分子が形成されたバイオチップと、第1の金属に加えられる信号の方向と同じ平面上に、信号が加えられる方向と直交する方向に磁場を形成する磁場ソースと、第1の金属に周波数成分を有する信号を加えるように配置される信号ソース部と、プローブ生分子と試料間のバイオ結合前後のそれぞれの第1の金属の信号値を測定するように配置される検出部とを備える電磁気誘導を用いたバイオ結合検出装置。
(もっと読む)
核酸の検出方法
【課題】 煩雑な操作を必要としないので、迅速で容易に再現性の良い結果が得られる、試料中の核酸配列を明確にまた簡便に検出できる方法を提供する。
【解決手段】 特定の核酸配列を含む試料溶液に核酸配列増幅用オリゴヌクレオチドを用いて増幅反応と同時およびまたは増幅反応後、該核酸配列に特異的に結合するリガンドが結合されたオリゴヌクレオチドを接触させ、特定の核酸配列と結合したリガンドを検出することによって試料溶液中に含まれる核酸配列を検出する方法において、増幅された核酸配を特異的に認識するオリゴヌクレオチドが結合された通液性フィルターおよび上記リガンドに結合する、標識された生理活性物質を用いることを特徴とする核酸配列の検出方法。
(もっと読む)
初代ラット肝細胞毒性モデリング
本発明は、遺伝子発現の全体的な変化の解明と既知の毒に曝された組織又は細胞中の毒性マーカーの同定に基づいている。医薬スクリーニング及び毒性アッセイにおいて、遺伝子が毒性マーカーとして使われる。本発明は、マイクロアレイ及びその他の固相プローブと共に使用するように設計された、毒に誘導された差次的な発現によって特徴づけられる遺伝子のデータベースを含む。 (もっと読む)
DNA及び/またはRNAの検出方法、仲介オリゴヌクレオチド及びDNA及び/またはRNAの検出のためのキット
【課題】 標的DNAの検出のために従来用いられていたハイブリダイゼーションでは、二本鎖PCR産物の一方が他方のハイブリダイゼーションを競合的に阻害し、効率が悪く、検出感度が上がらないという問題があった。
【解決手段】 支持体上に固定された検出用オリゴヌクレオチドと特異的に結合し得る第1のオリゴヌクレオチド部分と、試料中のDNA及び/またはRNAに特異的に結合し得る第2のオリゴヌクレオチド部分とを連結してなる仲介オリゴヌクレオチドを、上記検出用オリゴヌクレオチドと接触させることを含む、試料中のDNA及び/またはRNAの検出方法を提供する。
(もっと読む)
磁気移動法、微子移動装置と反応装置ユニット
微粒子(22)または磁気粒子を磁場を使用することにより同一の液体(23)中でまたは一つの液体(23a)から他の液体(23b)へのいずれかにて、分類、集合、移動または投与するための磁気移動法。移動装置(10)は保護膜(21)の内部に配置された磁石(13)からなり、そして集合または投与は磁石(13)の磁場を変更することにより達成される。磁場の変更は、微粒子を集合させる場合は磁石の一部または全体が強磁性体の外側にあり、そして粒子を解放または投与する場合は磁石の一部または全体が強磁性体の内部または背後にあるような方法で移動装置に含まれる板または管(12)状の強磁性体を使用することにより達成される。 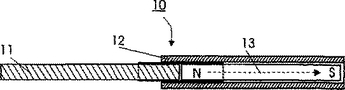 (もっと読む)
(もっと読む)
センサーチップの品質検査方法、サンプル評価方法、DNAチップ、プロテインチップ
【課題】
実際に相互作用可能に固定されているかどうかを判別する方法を提供すること。サンプルの採取及び調製が的確に行われているかを評価する方法を提供すること。前記方法を適用可能なセンサーチップを提供すること。
【解決手段】
(1)複数の概日リズム制御遺伝子の発現レベルにおける相関、又は、(2)特定の概日リズム制御遺伝子の発現レベルにおける経時的パターン、のいずれかを判断指標として用いたセンサーチップの品質検査方法、を提供する。また、物質間の相互作用の検出に供するサンプルの採取及び調製が的確に行われているか否かを評価する方法であって、上記(1)、(2)のいずれかを判断指標として用いたサンプル評価方法を提供する。さらに、特定の基板領域をセンサーチップの品質検査用領域又はサンプル評価用領域として用いたDNAチップ及びプロテインチップを提供する。
(もっと読む)
成形体、同成形体を形成する方法、および同成形体の使用
本発明は、箔が1μm〜1000μmの厚さDを有しており、箔の中に少なくとも1つの中空構造があり、中空構造の外径dは箔の厚さDの少なくとも2倍の値を有しており、中空構造の高さhは外径dの高々2倍の値をとり、中空構造の壁強度bは箔の厚さDの0.02倍から箔の厚さDまでの間にあり、中空構造の局所的曲率rは壁強度bの0.2倍から5倍までの間にあり、前記箔と前記少なくとも1つの中空構造が多数の有利には統計的に分布した細孔を有しており、細孔の直径が好ましくは10nm〜10μmであるような、箔から成る成形体に関するものである。
本発明はさらに、上記成形体を形成する方法と、上記成形体の、マイクロ構造化された部材のハウジングとしての使用、無機分子または有機分子、生体分子、原核細胞または真核細胞の固定化のための使用、原核細胞または真核細胞の培養のための使用、バイオセンサまたはバイオリアクタとしての使用にも関するものである。 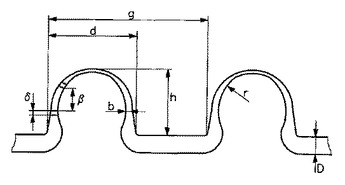 (もっと読む)
(もっと読む)
核酸検出装置及び核酸検出方法
【課題】高精度に核酸を検出する。
【解決手段】センサ電極11が、MOSFETのゲート電極に接続された電極又はMOSFETのゲート電極に、標的核酸分子とハイブリダイゼーションすることが可能なプローブ核酸分子を固定化する。制御回路30が、センサ電極の電位を制御してセンサ電極上で化学反応を発生させるための対向電極32を備える。スイッチ31が、ゲート電極を接地点又は基準電圧源に短絡して化学反応を発生させるか否かを切り替える。測定手段22が、化学反応前後でMOSFETの特性変調の強度を測定する。判定手段が、化学反応前後で生じたFETの電気的特性を示す物理量の差分の大きさが予め設定されたある値よりも大きいか否かを判定する。
(もっと読む)
1,521 - 1,540 / 1,741
[ Back to top ]



