Fターム[4B029CC03]の内容
微生物・酵素関連装置 (40,912) | 生物材料の存在状態 (7,687) | 固定 (1,880)
Fターム[4B029CC03]の下位に属するFターム
Fターム[4B029CC03]に分類される特許
1,481 - 1,500 / 1,741
ω3脂肪酸不飽和化活性を有するポリペプチドおよびそのポリペプチドをコードするポリヌクレオチドならびにそれらの利用
【課題】広い基質特異性を有し、効率よくω3位に不飽和結合を生成させるω3脂肪酸不飽和化活性を有するポリペプチド、およびそのポリペプチドをコードするポリヌクレオチドを提供する。このポリヌクレオチドを生物体内で発現させることにより、n−3系PUFAsの大量生産を可能とする。
【解決手段】ω3脂肪酸不飽和化活性を有するポリペプチドであって特定のアミノ酸配列からなるポリペプチド、ω3脂肪酸不飽和化活性を有するポリペプチドをコードするポリヌクレオチドであって特定の塩基配列からなるポリヌクレオチド等。
(もっと読む)
遺伝子発現分析に使用するための複雑な生物構造物からの遺伝子分子の単離
遺伝子発現の分析に使用するために動物のDNA, RNA, mRNA, rRNA又はtRNAのような遺伝分子の抽出及び単離のための方法及び装置が提供されている。本発明の方法及び装置は、特に遺伝分子レベル及び機能の高速、自動化分析に有用である。 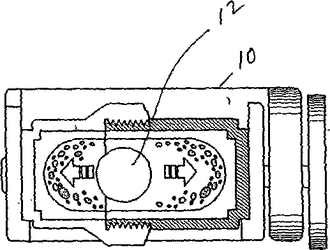 (もっと読む)
(もっと読む)
小型で高速な試料スクリーニング装置
【課題】動物細胞等の数十マイクロメータサイズの微細細胞を対象とした、信頼性が高く、高効率にスクリーニングが行える薬効スクリーニング装置と方法の提供。
【解決手段】原子間力顕微鏡に用いられるカンチレバー式の針を薬効スクリーニング装置の電極針として用い、かつ、電極針に配線を形成して絶縁膜で覆い、電極針の先端から10マイクロメートル程度はなれた位置に開口を設けて、配線の一部を露出させること、さらに、複数の細胞を保持するマイクロチャンバを形成し、複数の電極針を備えて、前記細胞に対応する位置に電極針を配した構造とすることによって解決できる。
(もっと読む)
血管新生において差次的に発現するESM−1遺伝子、そのアンタゴニスト、および、それらを使用する方法
本発明は、血管形成および発癌において発現が調節される、核酸およびそのコードされるポリペプチドであるESM−1に関する。本発明はまた、前記ポリペプチドに対する特異性を有する抗体に関する。本発明はまた、アンチセンス分子に関する。本発明はさらに、このような生物学的効果を必要としている哺乳動物における血管形成を治療または調節するのに有用な方法に関する。 (もっと読む)
表面電位測定型センサー装置
【課題】表面電位計測用の微小電極を用いた簡便にかつ超高感度に被検体中の多成分をセンシングできる表面電位測定型分子センサー装置を提供する。
【解決手段】
参照電位測定部位と、一種類もしくは複数種のホスト分子がターゲット分子を認識したとき、電位変化をシグナルとして発生させるセンシングユニットと、基板上に結合させるための結合ユニットからなるナノセンサーを基板表面に吸着させたセンサー膜部位、および、電位をモニターするための配線網部位の3要素部位をシリコン基板上に複数配線集積した集積センサー部と、シグナルをコントローラーに送るための被覆導線部と、それを接続するためのアダプター部と、それらがつながる計測コントローラー部からなる表面電位測定型センサー装置。
(もっと読む)
強化された特性を持つ変性ポリペプチドを発生させるためのルックスルー変異誘発
所定のアミノ酸を、ポリペプチドの事前選択された領域(またはいくつかの異なる領域)内の選択された一組の位置のそれぞれおよび全ての位置に導入して、ポリペプチド類似体のライブラリーを生成する、変異誘発の方法を開示する。この方法は、あるアミノ酸が、タンパク質の構造および機能で極めて重要な役割を演ずるという前提に基づいており、したがって、ポリペプチド内の非機能的アミノ酸残基(「コールドスポット」)またはその部分から、機能的アミノ酸残基(「ホットスポット」)を特定し区別することが可能である。ライブラリーは、所望のポリペプチド類似体のみ含有しかつスクリーニングに適切なサイズのものを生成することができる。このライブラリーを使用して、ポリペプチドの構造および機能における特定のアミノ酸の役割を研究することができ、また抗体や抗体断片、単鎖抗体、酵素、およびリガンドなどの、新しくまたは改善されたポリペプチドを開発することができる。 (もっと読む)
偽陽性結果を低下させる方法
【課題】検出に必要な試薬を生物学的分子から汚染除去し、および/または生物学的分子を含まない試薬を維持する、試料中の生物学的分子の検出のための方法および化合物を提供すること。
【解決手段】試料中の生物学的分子を検出するために必要な試薬中に潜在的に存在する生物学的分子の検出は回避する、試料中の生物学的分子の検出方法であって、
a)生物学的分子を潜在的に含む試料を提供する工程、
b)固相の表面にカップリングされた結合部を提供する工程、
c)生物学的分子を検出するために必要な試薬を提供する工程、
d)試料へ試薬を添加する工程、
e)試料中の生物学的分子を検出する工程、
を含み、工程c)において、又は工程d)において、又は工程c)及びd)において、試薬中に潜在的に存在する生物学的分子が固相の表面にカップリングされた結合部へ結合する条件下で試薬が結合部と物理的に接触している、方法。
(もっと読む)
半導体に固定化された酵素を具備するバイオセンサー及び方法
【課題】半導体に固定化された酵素を具備するバイオセンサー及び方法
【解決手段】本発明は、試験試料中の薬剤の存在及び/又は濃度を検出するための、官能性を持たせた半導体要素を用いる方法及びデバイスを提供する。本発明のデバイスは、(i)電子供与体の存在下において励起され得る半導体物質を含むか、又はそれと結合された表面を有する本体、前記半導体物質は、前記本体内で電流を発生することができる;及び、(ii)基質の存在下において、前記電子供与体を産する反応を触媒する、前記半導体物質に結合された酵素;を具備する。 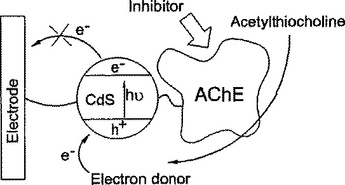 (もっと読む)
(もっと読む)
バブルを利用するハイブリダイゼーション方法および容器
【課題】 微小反応液を効率よく攪拌し、プローブ担体の測定において、基板表面に固定されたプローブDNAに対するターゲットDNAのハイブリダイゼーション効率を向上させるハイブリダイゼーション方法および容器を提供すること。
【解決手段】 微小反応容器内の反応液を攪拌する方法であって、微小反応容器中に設けられた微小ヒータを連続的にパルス加熱し、発生したバブルの膨張、凝縮により反応液を攪拌しながら、ハイブリダイゼーション方法および容器。
(もっと読む)
酵素電極、センサ、燃料電池、電気化学反応装置
【課題】 高密度で酵素を担持可能であり、かつ電流密度の向上を図ることができる酵素電極を提供すること。
【解決手段】 酵素と、酵素との電子の受け渡しを行うための第1のメディエータを少なくとも一種類と、第1のメディエータとの電子の受け渡しを行うための第2のメディエータを少なくとも一種類と、を担体を介して前記第1のメディエータ及び前記第2のメディエータの少なくとも一方との電子の受け渡しを行うための導電性部材に固定して、センサ、燃料電池、電気化学反応装置などの電極として有用である酵素電極を得る。
(もっと読む)
汎用タグアッセイ
本発明開示は、検出プローブを持つ汎用検出子が、標的に対応する識別子タグを持つタグ付き分子と共にインキュベートされ、相補的検出プローブへの識別子タグのハイブリダイゼーションが、アッセイ対象物中に、対応する標的が存在することを示すという、汎用タグアッセイのための方法および組成物を提供する。特に、本発明開示は、標的ヌクレオチド配列に対応する識別子タグを持つタグ付き分子を生成させる標的依存的操作によって、試料中の標的ヌクレオチド配列を検出するための方法および組成物を提供する。この方法では、検出プローブを持つ汎用検出子と共にタグ付き分子をインキュベートすることによって、相補的な検出プローブへの識別子タグのハイブリダイゼーションが可能になり、それによって、各識別子タグに対応する標的ヌクレオチド配列の存在が示される。好ましい実施形態には、一塩基多型(SNP)、対立遺伝子変異体、およびスプライス変異体を含む変異体配列を検出するための汎用タグアッセイの使用が含まれる。好ましい実施形態には、さらに、汎用検出子(好ましくは金電極または炭素電極を持つ汎用チップ)上に固定化された検出プローブへのタグ付きDNAまたはRNA分子のハイブリダイゼーションを検出するためのルテニウムアンペロメトリーの使用が含まれる。 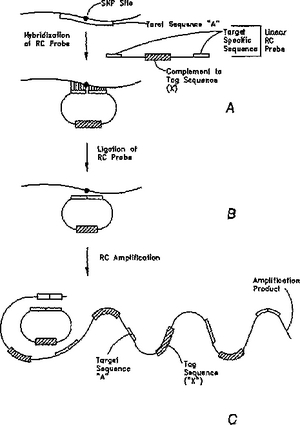 (もっと読む)
(もっと読む)
分子の実効サイズ決定法、基板への分子の付着方法および分子検出デバイス
【課題】 固体表面に付着する分子の付着密度をコントロールでき、このことにより、固体表面に付着した分子の溶液中での構造や挙動を明らかにでき、また、固体表面に付着した分子を用いるデバイスの高信頼性化や高感度化を実現できる技術を提供する。
【解決手段】 電荷を有する分子を基板に付着させるに際し、その分子を含んだ溶液に電解質を共存させ、電解質によるスクリーニング効果を調整すること、および、溶液中の分子の実効サイズを考慮することにより、分子の付着密度をコントロールする。電解質と電荷を有する分子とを含む溶液中の電荷を有する分子の実効サイズを、電解質によるスクリーニング効果から推定することもできる。
(もっと読む)
mRNAの絶対量を測定する方法及びシステム
【課題】 本発明は、mRNAの絶対量を測定する方法及びシステム、特に、cDNAマイクロアレイ上のmRNAの絶対量を測定する方法及びシステムの提供を目的とする。
【解決手段】 下記工程及び各手段が提供される:マイクロアレイを用意する;このマイクロアレイ上に少なくとも一組の連続稀釈コントロールスポットを用意する;既知の濃度の対応するコントロールcDNAとハイブリダイゼーションを行う;前記ハイブリダイゼーションから参照データを導き出し、前記参照データを用いて、使用した1以上のサンプルにおけるmRNAの絶対量を計算する。 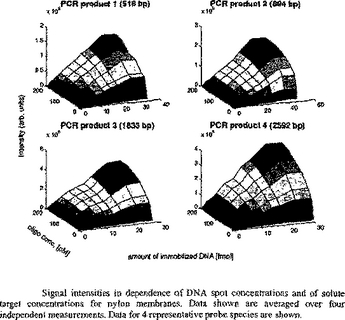 (もっと読む)
(もっと読む)
ランゲルハンス島の膵ベータ細胞に特異的なタンパク質およびその適用
本発明は、ランゲルハンス島の膵ベータ細胞において特異的に発現されるZnT-8タンパク質、インシュリンの成熟およびエキソサイトーシスに関係する該タンパク質をエンコードするポリヌクレオチド、ならびに例えばベータ細胞の選別および研究、および糖尿病および高インシュリン症に作用する医薬のスクリーニングのためのその適用に関する。 (もっと読む)
高次構造に基づくプローブ核酸塩基配列決定方法とDNAマイクロアレイ
【課題】 対象遺伝子の二次構造などの高次構造を考慮に入れることにより、二本鎖形成の確実性、配列特異性を高めたオリゴヌクレオチドを設計するための方法とそのオリゴヌクレオチドをプローブとして搭載したDNAマイクロアレイ。DNAマイクロアレイの感度、再現性、対象遺伝子の識別能力を向上させる。
【解決手段】 対象遺伝子配列の二次構造などの高次構造から、自己相補性による二本鎖を形成するステム領域と一本鎖のループ領域を予測し、ループ領域近辺の配列類似性と実験条件を評価し、オリゴヌクレオチドのハイブリダイゼージョンに適した領域を絞り込み、プローブを設計する。図2に示すようなループ領域の配列はmRNAのファミリー配列で異なっていることがしばしばあり、識別可能となる。更に一本鎖であるため、相補配列となるプローブとのハイブリダイズ能力がステム領域よりも高く、感度、再現性の向上が見込める。
(もっと読む)
洗浄装置
【課題】本発明は、細胞を運搬している細胞運搬マイクロカプセルを洗浄するための洗浄装置(1)に関する。
【解決手段】細胞運搬マイクロカプセルが、製品容器(2)において、冷蔵用バッファ溶液または凍結用バッファ溶液中に保存されている。細胞運搬マイクロカプセルを洗浄するための洗浄用溶液を貯蔵するため、貯蔵容器(6)が設けられている。貯蔵容器(6)が、製品容器(2)へと接続されている。さらに製品容器(2)は、廃棄物容器(10)へと接続されている。細胞運搬マイクロカプセルを洗浄するとき、細胞運搬マイクロカプセルを洗浄すべく洗浄用溶液が貯蔵容器(6)から製品容器(2)へと移され、その後に廃棄物容器へと移される。洗浄済みの細胞運搬マイクロカプセルを、さらなる使用のためにカートリッジへと移すことができる。
(もっと読む)
蛍光ポリマーと消光剤−連結鎖−リガンド・バイオコンジュゲートとを使用するバイオセンシング法
ビオチン化蛍光ポリマーとビオチン結合タンパク質との複合体および該蛍光ポリマー複合体でコートされた固体支持体が述べられる。この複合体は生物学的認識事象(たとえば、核酸ハイブリダイゼーション反応または酵素誘導ポリペプチド開裂)の検出センサとして使用することができる。この複合体の作製方法ならびに試料中の標的検体の存在および/または量を検出するためのこの複合体の使用方法も述べられる。標的検体は酵素(たとえば、β−セクレターゼ)または核酸(たとえば、1本鎖または2本鎖核酸)であってよい。  (もっと読む)
(もっと読む)
EGFR陽性癌の遺伝子発現プロファイリング
本発明は、EGFR陽性の癌に関連する予後判定マーカーに関する。特に、本発明は、EGFRを発現する癌のパラフィン包埋された固定組織サンプルにおける、遺伝子発現の分子的特徴付けに基づく予後判定法に関する。この方法は、患者がEGFRインヒビターによる処置によく反応する可能性があるかどうかを、医師が予測することを可能にする。本発明の1つの方法は、予後判定法であり、(a)患者から得られたEGFR発現性癌細胞を含むサンプルを、CD44v3;CD44v6;DR5;GRO1;KRT17;およびLAMC2からなる群から選択される少なくとも一遺伝子のRNA転写物またはそれらの産物の発現レベルの定量分析に供する工程、ならびに(b)該遺伝子もしくはそれらの産物の正規化された発現レベルが規定の発現閾値より高く上昇した場合、該患者を、EGFRインヒビターによる処置に抵抗性を示す可能性があると同定する工程を包含する。  (もっと読む)
(もっと読む)
心筋前駆細胞の単離方法及び単離用デバイス
【課題】 心筋前駆細胞に特有な表面マーカーの提供、並びに当該表面マーカーを用いた、心筋前駆細胞の単離方法及びその為のデバイス及び心筋前駆細胞の体内導入用デバイスの提供。
【解決手段】 中胚葉細胞を含有する細胞集団についてCD44、Flk1およびPDGFRαからなる群より選択される少なくとも1種の蛋白質の発現を解析する工程、及びCD44、Flk1およびPDGFRαからなる群より選択される少なくとも1種を発現している細胞を回収する工程を含む、中胚葉細胞を含有する細胞集団から心筋前駆細胞を単離する方法、及び当該方法を用いるデバイス。
(もっと読む)
核酸配列検出
本出願は、核酸プローブ24が付着した電極22を備える支持体104を用いる標的核酸配列を検出するためのシステムおよび方法を開示している。核酸標的26および非共有結合光電気化学的標識30がこのプローブ24と接触される。この非共有結合光電気化学的標識30は、好ましくは、二本鎖核酸に結合する。この混合物を照射することは、電極22で光電流を生成する。核酸プローブ要素のアレイを備える支持体104もまた開示される。 (もっと読む)
1,481 - 1,500 / 1,741
[ Back to top ]



