Fターム[4C054CC02]の内容
水添ピリジン系化合物 (12,675) | 1位の置換基 (2,124) | 非置換炭化水素基により置換 (395)
Fターム[4C054CC02]に分類される特許
161 - 180 / 395
麻酔薬
一実施態様において、本発明は、式(I):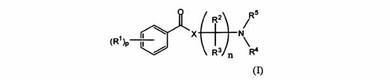
の新規な化合物及びそのプロドラッグ、塩、水和物、溶媒和物そして窒素酸化物を提供する。本発明はまた、これら化合物を含む医薬組成物及び該化合物の合成方法および医療上の治療における使用方法も提供する。  (もっと読む)
(もっと読む)
塩の製造のための新規な方法
本発明は、医薬化合物またはそれらの中間体の塩酸塩、臭化水素酸塩またはヨウ化水素酸塩の製造および結晶化のための新規な方法であり、塩基またはその酸付加塩を溶媒中でハロゲン化トリアルキルシリルと反応させる方法を提供する。 (もっと読む)
β−グルコセレブロシダーゼの活性増強による神経学的疾患の治療方法
野生型β-グルコセレブロシダーゼの安定性を増強する方法を提供する。中枢神経系におけるβ-グルコセレブロシダーゼの発現又は活性の増強が有用と考えられる、神経学的疾患を有する個体の治療及び/又は予防の方法を提供する。この方法は、β-グルコセレブロシダーゼ用の薬理学的シャペロンの有効量を投与することを含み、但し、個体は、β-グルコセレブロシダーゼをコードする遺伝子に変異を有さないことを条件とする。さらに、特異的な薬理学的シャペロンとして同定され、インビボで中枢神経系においてβ-グルコセレブロシダーゼの活性を増強することが示されるβ-グルコセレブロシダーゼインヒビターを提供する。 (もっと読む)
ニューロキニンアンタゴニストとしてのピペリジン誘導体
【課題】ニューロキニンレセプターのアンタゴニストとして有用な新規化合物を提供すること。
【解決手段】下式の化合物が提供される。ここでi、j=1〜2、n=0〜3、n'=1〜3であり;AおよびA’は、Hまたは一緒になって=O、=Sなどであり;XはO、CO、C(R, R1)など;R2、R3は、H、ハロゲン、置換されていてもよいアルキルなどの種々の所定の基であり、ここでR1は所定のアルキルである。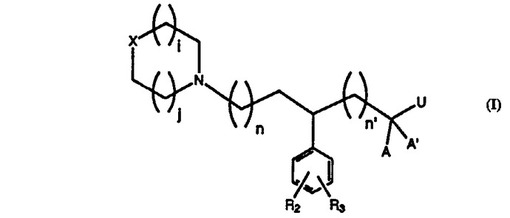 (もっと読む)
(もっと読む)
ビフェニル誘導体及びC型肝炎の治療におけるそれらの使用
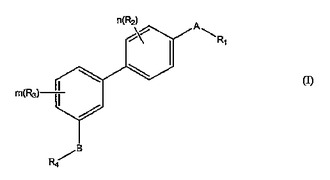
式(I)の化合物はHCVに対して活性であることが発見され、式中、R1は部分、−A1−L1−A1’、−A1−L1−A1’−A1’’又は−A1−L1−A1’−Y1−A1’’であり;A及びBは同一であるか又は異なっており、そして各々直接結合又は−CO−NR’−、−NR’−CO−、−NR’−CO−NR’’−、−NR’−S(O)2−、−S(O)2−NR’−又は−NR’−部分を表し、式中、R’及びR’’は同一であるか又は異なっており、そして各々水素又はC1〜C4アルキルを表し;R2及びR3は同一であるか又は異なっており、そして各々C1〜C4アルキル、C1〜C4アルコキシ、C1〜C4アルキルチオ、C1〜C4ハロアルキル、C1〜C4ハロアルコキシ、ハロゲン、ヒドロキシ、チオ、−NR’R’’、−SO2−R’’’、−NR’−COR’’’又はCO2R’’’を表し、式中、R’及びR’’は、同一であるか又は異なっており、そして水素又はC1〜C4アルキルを表し、及びR’’’はC1〜C4アルキルを表し;n及びmは同一であるか又は異なっており、そして各々0、1又は2を表し;R4は、C1〜C6アルキル又はC1〜C6ハロアルキル基又は部分、−A4、−A4−A4’、−L4−A4、−A4−L4−A4’、−A4−Het4−L4−Het4’−L4’又は−L4−Het4−L4’であり、各A1、A4、A1’、A1’’及びA4’は同一であるか又は異なっており、そしてフェニル、5〜10員ヘテロアリール、5〜10員ヘテロシクリル又はC3〜C6カルボシクリル部分を表し;各L1及びL4は同一であるか又は異なっており、そしてC1〜C4アルキレン又はC1〜C4ヒドロキシアルキレン基を表し;Y1は、−CO−NR’−、−CO−(C1〜C4アルキレン)−、−CO−(C1〜C4アルキレン)−NR’−、−NR’−CO−、−CO−、−O−CO−又は−CO−O−を表し、式中、R’は水素又はC1〜C4アルキルであり;L4’は水素又はC1〜C4アルキル基を表し;Het4及びHet4’は同一であるか又は異なっており、そして−O−、−S−又は−NR’−を表し、式中、R’は水素又はC1〜C4アルキル基であり;R1及びR4中のフェニル、ヘテロアリール、ヘテロシクリル及びカルボシクリル部分は、置換されていないか、又は(a)−CO2R’、−SO2NR’’R’’、−S(O)2−R’、−CONR’’R’’、−COR’’’、−CO−CO−OR’’’、−CO−(C1〜C4アルキレン)−OR’’、−CO−(C1〜C4アルキレン)−NR’’R’’、−CO−(C1〜C4アルキレン)−NR’’−CO−R’’’、−CO−(C1〜C4アルキレン)−CO−NR’’R’’、−CO−(C1〜C4アルキレン)−SO2−R’’’、−CO−(C1〜C4アルキレン)−O−(C1〜C4アルキレン)−OR’’、−CO−(C1〜C4アルキレン)−O−(C1〜C4アルキレン)−NR’’R’’、−CO−(C1〜C4アルキレン)−NR’’−(C1〜C4アルキレン)−OR’’、−CO−(C1〜C4アルキレン)−NR’’−(C1〜C4アルキレン)−NR’’R’’、−SO2−(C1〜C4アルキレン)−OR’’、−NR’’−SO2−R’’’、−(C1〜C4アルキレン)−CO−(C1〜C4アルキレン)−CO等から選択される単一の未置換の置換基等より置換されている。
 (もっと読む)
(もっと読む)
β−アラニン化合物、ピペリドン化合物及びアミノピペリジン化合物の製造方法
【課題】 従来製法に比べて、温和な条件で製造できる工業的に優位なβ−アラニン化合物の製造法、そうして得られたβ−アラニン化合物を原料とするピペリドン化合物の製造法並びにシアン化水素の発生しない工業的に安全な還元剤を用いたアミノピペリジン化合物の製造法を提供すること。
【解決手段】 アルキルアミン化合物をアクリル酸エステルと反応させてβ−アラニン化合物を製造するにあたり、カルボン酸の存在下で反応することを特徴とするβ−アラニン化合物の製造法、こうして得られたβ−アラニン化合物を塩基の存在下で環化縮合させた後、次いで環化縮合生成物を酸性条件下で加水分解脱炭酸反応せしめることを特徴とするピペリドン化合物の製造法、並びに水素化触媒の存在下で、ピペリドン化合物をアンモニア及び水素と還元アミノ化反応せしめることを特徴とするアミノピペリジン化合物の製造法。
(もっと読む)
ドネペジル経皮吸収型製剤
【課題】副作用を軽減せしめ、かつ充分な治療効果を発揮するドネペジル類含有経皮吸収型製剤。
【解決手段】TypeBの結晶形ドネペジルを含むドネペジル及び/又はその塩を粘着剤総重量当たり9質量%〜50質量%含む経皮吸収型製剤。本発明の経皮吸収製剤(特に非水系の粘着剤層に含有させたもの)を用いることにより、ドネペジル及び/又はその塩の皮膚透過性が極めて良好で、かつ製剤中の薬物安定性も良好であり、しかも局所刺激や副作用の極めて少ない経皮吸収型製剤を得ることができる。
(もっと読む)
置換されたテトラサイクリン化合物を用いて、遺伝子または遺伝子産物の発現を調節する方法
本発明は、テトラサイクリンオペレーター系に作動可能に連結された核酸の発現の調節のための置換されたテトラサイクリン化合物の使用に、少なくとも一部は関する。本発明は、細胞中で遺伝子発現を調節するために原核生物のTetリプレッサー/オペレーター/インデューサー系の構成要素を利用する調節系において用いられる化合物に関する。本発明の方法で特徴づけられるような特定の置換されたテトラサイクリン化合物の使用は、例えば、テトラサイクリンおよびドキシサイクリンについての結果に比較した場合、用量応答結果の改善をもたらす。従って、本発明の特定の方法によって、細胞中での遺伝子発現の調節において、Tetリプレッサー/インデューサー系の制御を強化することが可能になる。 (もっと読む)
ムスカリンアンタゴニスト
【課題】ムスカリンアンタゴニストを提供すること。
【解決手段】式(I)
の1,4二置換ピペリジン化合物のアミド誘導体またはその薬学的に受容可能な塩、エステルもしくは溶媒化合物(ここで、R1は、必要に応じて置換されたシクロアルキル、シクロアルキルアルキル、アリール、アリールアルキルまたはヘテロアリールであり;R2は、H、アルキルまたは必要に応じて置換されたシクロアルキル、シクロアルキルアルキル、ヘテロシクロアルキル、架橋シクロアルキルもしくは架橋ヘテロシクロアルキルであり;R3は、アルキルまたは−CH2OHであり;そしてR4はHまたはアルキルである)は、アルツハイマー病のような認知障害を処置するために有用なムスカリンアンタゴニストである。薬学的組成物および調製方法もまた開示される。
(もっと読む)
ケラチン繊維の成長を誘導及び/又は刺激するため、並びに/あるいはそれらの損失を予防するための薬剤としての4−アミノピペリジン誘導体の使用
【課題】脱毛症を排除又は低減する組成物、特に毛髪の成長を誘導又は刺激する組成物の提供。
【解決手段】下記式(I):
[式中、Alk1及びAlk2は、互いに独立に、直鎖状の飽和C1〜C10若しくは不飽和C2〜C10、又は分枝状の飽和若しくは不飽和C3〜C10アルキレン基(二価の基)を意味し;Ar1及びAr2は、フェニル基を意味し;Rは、水素原子、又は飽和若しくは不飽和の、直鎖状C1〜C10若しくは分枝状C3〜C10アルキル基を意味し;R1及びR2は、互いに独立に、直鎖状の飽和C1〜C7若しくは不飽和C2〜C7、又は分枝状若しくは環状の、飽和若しくは不飽和C3〜C7アルキル基を意味する]で表される4−アミノピペリジン誘導体、並びにその塩、光学異性体、及び溶媒和物の少なくとも1種を使用する。
(もっと読む)
アルツハイマー病を治療するためのピペリジン及び関連化合物
式(I)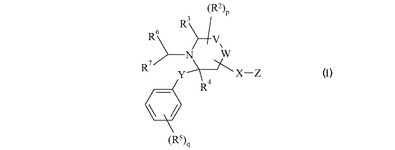
を有する化合物はγ−セクレターゼのモジュレーターであり、よってアルツハイマー病の治療において有用である。 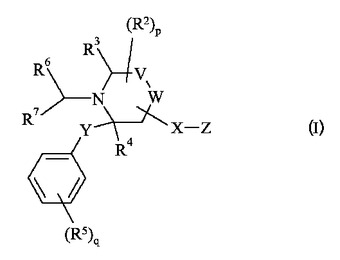 (もっと読む)
(もっと読む)
眼圧降下剤としてのアブノーマル・カンナビジオール化合物
本発明は、式I: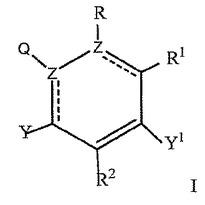
[式中、Y、Q、Z、R、R1およびR2は明細書中に定義する通りである]
で示される化合物を緑内障または高眼圧の処置に充分な量で個体の眼に適用することを含んで成る緑内障または高眼圧の処置方法を提供する。本発明はさらに、前記化合物を含有する医薬組成物、例えば眼用組成物をも包含する。 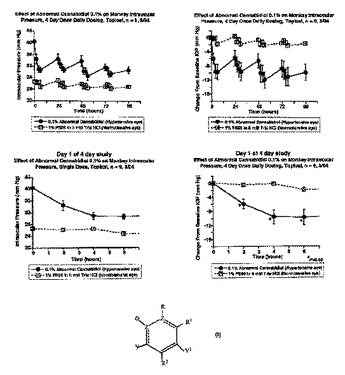 (もっと読む)
(もっと読む)
例えば慢性気管支閉塞、喘息および過活動膀胱の処置に有用な、ムスカリンM3受容体アンタゴニスト活性を有する環状アミノアルコールの新規アルキルエステル
本発明は、式(I)
【化1】
〔式中、R1、R2、R3、R4、R5およびXは明細書において定義の通りである。〕
の化合物、それらの製造方法、それらを含む医薬組成物、医薬組成物の製造方法および治療におけるそれらの使用を提供する。  (もっと読む)
(もっと読む)
ピペリジンMCHアンタゴニストおよび肥満の処置におけるそれらの使用
【課題】メラニン濃縮ホルモン(MCH)に対するアンタゴニストを提供すること。
【解決手段】
構造式(I)で表される化合物あるいはそれらの薬学的に受容可能な塩、エステルまたは溶媒和物を開示し、そして、この化合物を含む薬学的組成物ならびに摂食障害および糖尿病の処置におけるこの化合物の使用方法を開示する。本発明はまた、摂食障害(例えば、肥満および過食症)ならびに糖尿病の処置を必要とする哺乳動物に、有効量の式(I)の化合物を投与する工程を含む、摂食障害および糖尿病の処置方法に関する。本発明の別の局面は、薬学的に受容可能なキャリアと組み合わせて式(I)の化合物を含む、摂食障害および肥満の処置のための薬学的組成物である。
(もっと読む)
ロピバカイン塩酸塩無水物およびその調製
本発明は、安定な無水ロピバカイン塩酸塩を調製するための方法であって、当該方法は、ロピバカイン塩基からロピバカイン塩酸塩を調製することを含み、ロピバカイン塩基は、95%以上のキラル純度を有して提供され、当該単離は、イソプロパノールおよび塩酸塩の使用を含み、水フリーの条件下で行われる方法に関する。ロピバカイン塩基は、相間移動触媒の存在下で、L-ピペコリン酸2,6-キシリジド塩酸塩をN-プロピル化することにより高いキラル純度で提供され得る。更に本発明は、上記方法により得られる安定な無水ロピバカイン塩酸塩に関する。 (もっと読む)
塩酸ドネペジルの調製に有用な中間体およびその新規な多形の改善された合成および調製
本発明は、2−(1−ベンジルピペリジン−4−イルメチリデン)−5,6−ジメトキシインダン−1−オン(塩酸ドネペジルの合成において主要な中間体)、本主要中間体の結晶多形を調製するプロセス、および塩酸ドネペジルを生成するためのそれらの使用に関する。特に、本発明は、中間体2−(1−ベンジルピペリジン−4−イルメチリデン)−5,6−ジメトキシインダン−1−オンの生成方法を提供する。本プロセスは、水性溶媒に水酸化カリウムを使用して、5,6−ジメトキシインダン−1−オンを1−ベンジルピペリジン−4−カルバルデヒドと反応させることを含む。水性溶媒は、有機溶媒と水の混合物であってよい。有機溶媒が水と混和しない場合は、反応を相間移動触媒の存在下において行うことができる。  (もっと読む)
(もっと読む)
抗シワ化粧品組成物
【課題】シワ、特に表情シワを平滑化するまたは消すための有効な化合物および該化合物を含有する化粧品または皮膚科学的組成物の提供。
【解決手段】式(I)
[式中:−Alk1及びAlk2は、互いに独立に、直鎖状飽和C1−C10アルキレン基などを表し;−Ar1は、−F、−CF3などで任意に置換されてもよいフェニル基を表し;−Ar2は、−F、−CF3などで任意に置換されてもよいフェニル基を表し;−Rは、水素原子またはC3−C10アルキル基などを表す。]で表される4−アミノピペリジン誘導体および該化合物を含有する化粧品または皮膚科学的組成物。
(もっと読む)
改善された色品質を有するN−アルキルラクタムの製造方法
N−アルキルラクタムに0.01〜10質量%のC1〜10のアルコール、または0.01〜10質量%のC1〜10のアルコールを遊離する化合物を添加する、改善された色品質を有するN−アルキルラクタムの製造方法である。少なくとも99.0質量%のN−アルキルラクタムと、100〜5000質量ppmの範囲のC1〜10のアルコール、または100〜5000質量ppmの範囲のC1〜10のアルコールを遊離する、アセタール、アミナールまたはオルトエステルを含む混合物である。 (もっと読む)
新規化合物およびその製造法
本発明は(S)−2’[2−1−(メチル−2−ピペリジル)エチル]シンナムアニリド(I)またはその塩もしくは医薬的に許容されるプロドラッグの合成法に関する。
【化1】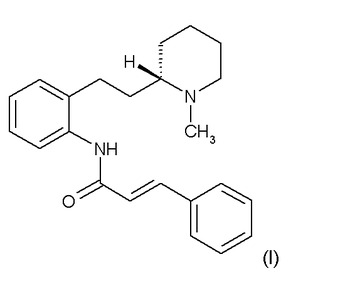
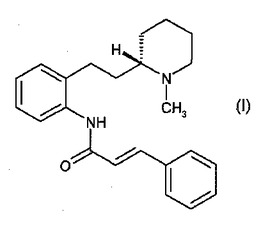 (もっと読む)
(もっと読む)
ベンゼンスルホン酸塩および2−[2−(1−アルキル−2−ピペリジル)エチル]シンナムアニリドを合成するための中間体としてのそれらの使用
本発明は、式(I)の塩およびそれらを製造するための方法に関する(式中、Xは有機または無機部分であり、nは0、1、2、3または4であり;そしてR*およびRbはそれぞれ独立してH、OH、C1、C2、C3もしくはC4アルキル、C1、C2、C3もしくはC4ハロアルキル、C1、C2、C3もしくはC4アルコキシ、C1、C2、C3もしくはC4アルケニルから選択されるか、または両方がNO2部分を形成するための酸素であり;そしてR1はC1、C2、C3またはC4アルキルであり;そしてYおよびZは両方が炭素であり;そして
破線−−−−−は飽和または不飽和結合を示す)。式(I)の塩はシンナムアニリド(Y)を形成するための方法における中間体となり得る(R8はH、OH、C1、C2、C3またはC4アルキルから選択され;そしてR1はC1、C2、C3またはC4アルキルである)。
【化1】
 (もっと読む)
(もっと読む)
161 - 180 / 395
[ Back to top ]

