Fターム[4C054FF01]の内容
水添ピリジン系化合物 (12,675) | P−位の置換基 (3,383) | 非置換 (532)
Fターム[4C054FF01]に分類される特許
201 - 220 / 532
ビスアミド亜鉛塩基
一般式(I)の化合物を提供する。
(R1R2N)2−Zn・aMgX12・bLiX2 (I)
R1およびR2は、それぞれ独立して、置換もしくは非置換の、直鎖もしくは分岐鎖状のアルキル、アルケニル、アルキニル、またはそれらのシリル誘導体、および置換もしくは非置換のアリールもしくはヘテロアリールから選択され、
R1およびR2は、共に環状構造を形成することができ、または、R1および/もしくはR2は、重合体構造の一部となることができ、
X12は、二価陰イオンまたは互いに独立した2つの一価陰イオンであり、
X2は、一価陰イオンであり、
a>0であり、
b>0である。
前記亜鉛アミド塩基は、とりわけ、芳香族の脱プロトン化およびメタル化に用いられる。
(もっと読む)
フルオレン、アントラセン、キサンテン、ジベンゾスベロン、及びアクリジンの誘導体、並びに、それらの使用
抗癌剤及び抗腫瘍剤として作用し、とりわけ、Wnt/β−カテニンシグナル経路の活性を変調して癌細胞のような細胞中に存在するβ−カテニンのレベルを低下させるのに有用であり、又は癌細胞などの細胞系における遺伝子発現レベルを変調する薬剤として機能するフルオレン、アントラセン、キサンテン、ジベンゾスベロン、及びアクリジンのジスルホンアミド誘導体、並びに、それらの塩を含む同様なヘテロ環構造を有する薬剤が開示され、併せて、こうした薬剤を調製する方法、及びこうした薬剤を活性成分として含む薬学的組成物、及び治療薬としてこれらを使用する方法が開示される。 (もっと読む)
環状アルキレンイミンの製造方法
【課題】簡便な製造装置を使用して任意の生産に対応が可能な環状アルキレンイミン、及び重水素化された環状アルキレンイミンの製造方法を提供する。
【解決手段】軽水又は重水溶液中でルテニウム系触媒の存在下に、主鎖を形成しているアルキレン基の炭素数が4〜6であるα,ω−ジアミノアルカンを環化反応させる環状アルキレンイミンの製造方法、及び、重水溶液中でルテニウム系触媒の存在下に、主鎖を構成するアルキレン基の炭素数が4〜6であるα,ω−ジアミノアルカンを環化反応させて得られる、重水素化された環状アルキレンイミンが、複素環の主鎖を形成している炭素原子に結合している、水素原子と重水素原子中の重水素原子の割合([重水素原子(原子数)/(水素原子+重水素原子)(原子数)]×100(%))が50%以上であることを特徴とする、環状アルキレンイミンの製造方法。
(もっと読む)
置換アミドの医薬用途
11β-ヒドロキシステロイド・デヒドロゲナーゼ1型(11βHSD1)の活性を調節するための置換アミドの使用、及び医薬組成物としてのそれらの化合物の使用を説明する。また、新規クラスの置換アミド、治療法におけるそれらの使用、その化合物を含んでなる医薬組成物、並びに医薬品の製造におけるそれらの使用も説明する。本発明の化合物は、11βHSD1の活性の調節因子であり、且つ、より特異的な阻害剤であるので、活性グルココルチコイドの細胞内濃度の低下が望ましい様々な医学的障害の治療に有用であり得る。 (もっと読む)
置換されたアミド誘導体
本発明は 、式(I)で表わされる置換されたアミド誘導体、その製造方法、この化合物を含有する医薬並びにブラジキニン−B1Rアンタゴニストとして、及び特に痛みの状態の治療へのその使用に関する。
【化1】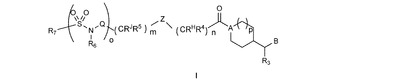
 (もっと読む)
(もっと読む)
置換されたスルホンアミド誘導体
本発明は、置換されたスルホンアミド誘導体、その製造方法、前記化合物を含有する医薬品及び医薬品を製造するための置換されたスルホンアミド誘導体の使用に関する。 (もっと読む)
核内受容体結合剤
本発明は、新規種類の選択的エストロゲン受容体モジュレーター(SERM)に関する。本SERM化合物は、癌、例えば前立腺癌および乳癌、骨粗しょう症、ホルモン関連疾患のぼせまたは血管運動症状、神経障害、心血管疾患ならびに肥満の予防および治療をはじめとする様々な疾患および状態の予防および/または治療に関する用途に利用することができる。 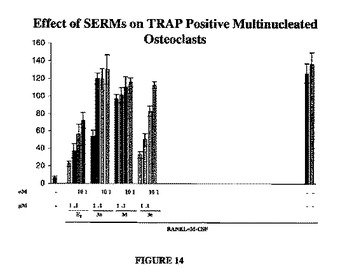 (もっと読む)
(もっと読む)
光塩基発生剤、感光性樹脂組成物、物品、及びネガ型パターン形成方法
【課題】400nm以上の波長領域に、光反応活性を有する新規な光塩基発生剤を提供する。また、高感度で、高分子前駆体の種類を問わず大きな溶解性コントラストを得られる感光性樹脂組成物を提供する。
【解決手段】下記式(1A)〜(1C)で表わされる光塩基発生剤、及び当該光塩基発生剤と高分子前駆体を含有する、感光性樹脂組成物である。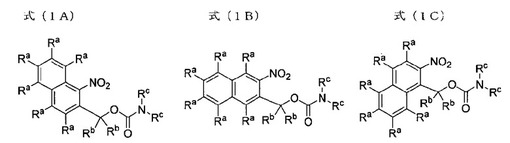
(式中、RaとRbは、それぞれ独立に、水素原子、ハロゲン原子、ヒドロキシル基、メルカプト基、ニトロ基、シリル基、シラノール基、もしくは1価の有機基を示す。Rcは、それぞれ独立に、水素原子、もしくは1価の有機基を示す。但し、Rcの少なくとも1つは、1価の有機基である。)
(もっと読む)
ヒストンデアセチラーゼ阻害剤
本発明は、ヒストンデアセチラーゼを阻害するための化合物に関する。より詳細には、本発明は、式(I)の化合物、並びにそのN−オキシド、水和物、溶媒和物、医薬として許容できる塩、プロドラッグ及び錯体、並びにそのラセミ及びスカレミック混合物、ジアステレオマー及びエナンチオマーを提供し、式中、基L、M、X及びYは、本明細書で定義された通りである。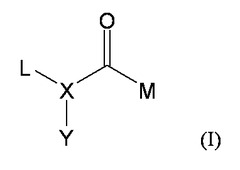
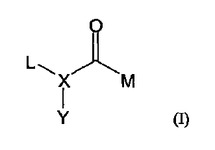 (もっと読む)
(もっと読む)
新規光学活性環状アミノ酸およびその製造方法
【課題】医農薬の合成中間体として有用な、新規な環状アミノ酸、及びその中間体を提供する。
【解決手段】下記一般式(1)で示される光学活性環状アミノ酸。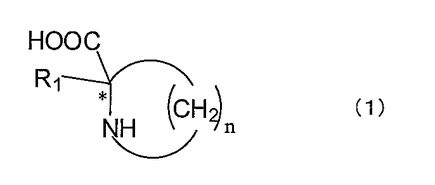
(式中、R1はイソプロピル基、炭素数4〜10の直鎖、分岐若しくは環式のアルキル基、炭素数6〜14の芳香族基で置換されたエチル基、ヘテロアルキル基で置換されていても良い炭素数6の芳香族基で置換されたメチル基、ヘテロ原子を含む炭素数2〜10の直鎖等であり、特にイソプロピル基、s−ブチル基、4−エトキシフェニルメチル基、2−メチルチオエチル基が好ましく、nは1〜6 の整数、* は不斉炭素を示す。)
(もっと読む)
ラクタム置換ジカルボン酸およびそれらの使用
本発明は、新規のラクタム置換ジカルボン酸誘導体、それらの製造方法、疾患の処置および/または予防におけるそれらの使用に関する。本発明は、また、疾患の処置および/または予防用の、特に心血管障害の処置および/または予防用の医薬の製造における該物質の使用に関する。 (もっと読む)
α,α−ジ置換環状含窒素化合物の製造方法
【課題】α位が置換されている環状含窒素化合物の置換基が導入されている側のα位にさらに置換基を導入すること。
【解決手段】窒素がシアノ基で保護されたα−置換環状含窒素化合物を、有機溶媒中で電極酸化して、窒素がシアノ基で保護されたα,α−ジ置換環状含窒素化合物を製造する方法。
(もっと読む)
8−[{1−(3,5−ビス−(トリフルオロメチル)フェニル)−エトキシ}メチル]−8−フェニル−1,7−ジアザ−スピロ[4.5]デカン−2−オン化合物の合成のための方法および中間体
本出願は、式27a−スルホン酸塩化合物を酢酸の存在下で亜鉛と反応させるステップを含む、8−({1−(3,5−ビス−(トリフルオロメチル)フェニル)−エトキシ)−メチル}−8−フェニル−1,7−ジアザ−スピロ[4.5]デカン−2−オンの合成方法を開示する。この方法は、(a)式IIIの保護エナミンをニトロ化剤と反応させて対応する保護ニトロ−エナミンを生成させ、続いてその生成物を還元して式IVの保護ピペリジンとするステップと、(b)ステップ「a」からの式IVの保護ピペリジンを、パラジウム触媒の存在下で水素と反応させることによって脱保護して式Vの化合物を生成させるステップと、などを含む。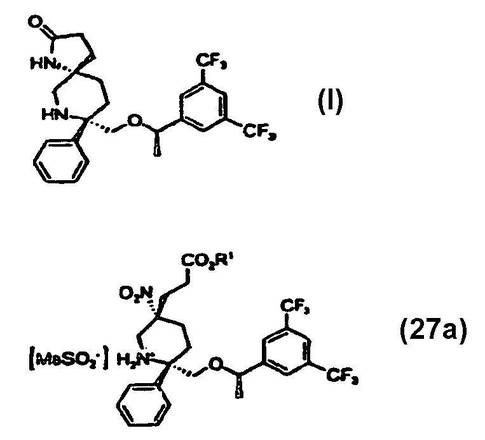
 (もっと読む)
(もっと読む)
フェブリフジン及びイソフェブリフジンの新規製造方法
【課題】熱帯性マラリア原虫に対して極めて強い活性を有するフェブリフジン(3−[3−(3−ヒドロキシ−2−ピペリジニル)−2−オキソプロピル]−4(3H)−キナゾリノン)及びイソフェブリフジンの新規な合成方法であり、全ての段階において、水性溶媒中で行う全合成ルートによる製造方法の提供。
【解決手段】(R)−(+)−2,2−ジメチル−1,3−ジオキソラン−4−カルボキサアルデヒドを出発物質として数段階の工程により(3’S)−1−[2’−(3’−ベンジルオキシ)−1’−(tert−ブトキシカルボニル)−ピペリジノ]−3−ヒドロキシ−2−プロパノンを得、これを4−ヒドロキシキナゾリンと反応させて、目的物の保護体を得る。これを6N塩酸と加熱処理することによりフェブリフジンが得られる。
(もっと読む)
ピペコリン酸の立体選択的なエステル化方法
【課題】ピペコリン酸を高い収率で立体選択的にエステル化できる方法を確立し,医薬品の合成原料や中間体として有用な光学活性ピペコリン酸やその誘導体を工業的に提供できるようにする。
【解決手段】ピペコリン酸の窒素部位に置換基を導入してN−置換ピペコリン酸に変換した後,アルコールを含む有機溶媒中,立体選択性を有する生体触媒を用いてエステル化する。これによって,高い収率で光学活性N−置換ピペコリン酸エステルを得ることができるようになり,医薬品の合成原料や中間体として有用な光学活性ピペコリン酸やその誘導体を経済的に製造し提供することが可能となる。
(もっと読む)
光学活性ピペコリン酸またはその誘導体の製造方法。
【課題】ピペコリン酸から,医薬品の合成原料や中間体として有用な光学活性ピペコリン酸や光学活性ピペコリン酸誘導体を工業的に有利に製造する方法を提供する。
【解決手段】ピペコリン酸をN−置換ピペコリン酸に変換した後,アルコールを含む有機溶媒中で立体選択性を有する生体触媒を用いてエステル化する。次いで,アルカリで中和し光学活性N−置換ピペコリン酸エステルと光学活性ピペコリン酸塩となした後,有機溶媒/水系における分配特性を利用して両光学活性体を分離する。このようにして得られた光学活性N−置換ピペコリン酸エステルと光学活性N−ピペコリン酸塩の各々を加水分解や脱保護処理することによって,医薬品の合成原料や中間体として有用な光学活性N−置換ピペコリン酸エステル,光学活性N−置換ピペコリン酸,光学活性ピペコリン酸エステル,光学活性ピペコリン酸を経済的に製造し提供することが可能となる。
(もっと読む)
炎症の治療において有用なピペリジノン類
式 (I)
[式中、R1、R2、R3、R4、R5、R6、R7、R8、m、n、qおよびrは、明細書において定義された意味を有する。]の化合物、およびその薬事的に許容される誘導体類が提供される。これらの化合物は、炎症に関連する疾患及び症状の治療に有用である。  (もっと読む)
(もっと読む)
芳香族性化合物の位置選択的置換方法
【課題】芳香族性化合物のオルト位又は隣接位への置換基導入を可能にする銅アート錯体を提供する。
【解決手段】下記の式I:
【化1】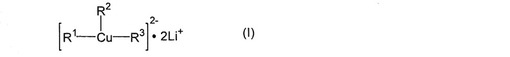
(式中、R1は、置換又は未置換の、アルキル、アルケニル、ジアルキルアミノ、アリール、アリールアルキル、トリアルキルシリルアルキル、5〜7員複素環、或いは5〜7員環状二級アミン基を表し、R2は、置換又は未置換の、ジアルキルアミノ又は前記環状二級アミン基を表し、R3は、シアノ、置換又は未置換の、アルキル、アルケニル、ジアルキルアミ基、又は前記環状二級アミン基を表す)によって表される銅アート錯体、並びにこの錯体を用いて芳香族性化合物に位置選択的に置換基を導入するための方法。
(もっと読む)
新規プロドラッグ
本発明は、新規な式−Iのプロドラッグまたはその塩、調製プロセスおよびその使用について記載する。 (もっと読む)
炎症の治療において有用なピペリジノン類
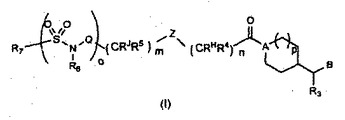
式 (I)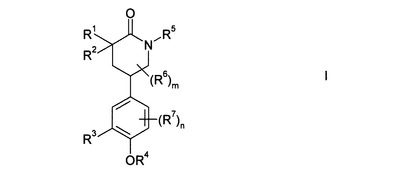
[式中、R1、R2、R3、R4、R5、R6、R7、mおよびnは、明細書において定義された意味を有する。]の化合物、およびその薬事的に許容される誘導体類が提供される。これらの化合物は、炎症に関連する疾患及び症状の治療に有用である。 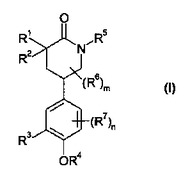 (もっと読む)
(もっと読む)
201 - 220 / 532
[ Back to top ]

