Fターム[4H045AA30]の内容
Fターム[4H045AA30]に分類される特許
221 - 240 / 12,187
ヒト抗体及びタンパク質
【課題】低免疫原性を示す抗体を含む合成タンパク質を提供する。
【解決手段】ヒト用複合抗体を提供し、具体的には、一又はそれ以上のT細胞エピトープを除去するように修飾された抗体を提供する。修飾抗体又は前記修飾抗体の抗原結合フラグメントにおいて、前記修飾抗体又は抗原結合フラグメントの重鎖及び軽鎖可変領域が、各々1又はそれ以上の他の抗体又は抗原結合フラグメントからのアミノ酸配列の2又はそれ以上のセグメントから成り、前記セグメントが全てCDRsでもなくフレームワーク領域でもないことを特徴とする修飾抗体又は前記修飾抗体の抗原結合フラグメント。このようなタンパク質を生成する方法。
(もっと読む)
予防又は治療目的のためのMHCクラスI拘束性エピトープに対する免疫応答を誘発し、増強し、維持する方法
【課題】好ましくはMHCクラスI拘束性エピトープに対する免疫応答を誘発し、増強し、持続するための方法及び組成物。
【解決手段】実施の形態は、好ましくはMHCクラスI拘束性エピトープに対する免疫応答を誘発し、増強し、持続するための方法及び組成物に関する。この方法及び組成物は、予防又は治療目的のために用いられ得る。
(もっと読む)
ワクチン用のヒト白血球抗原(HLA)クラスIまたはII分子に結合する腫瘍関連ペプチドの新規組成物
【課題】抗癌ワクチン組成物として、白血球抗原(HLA)クラスIまたはII分子に結合する腫瘍関連ペプチド、癌、特に腎臓癌や脳腫瘍、特定の神経膠腫、特に膠芽腫に対して抗腫瘍免疫応答を誘発するワクチン組成物に関して、当該組成物の凍結乾燥品(lyophilisate)の溶解性の強化及び湿潤強化を施した安全で有効な新規ペプチド組成物の提供。
【解決手段】マンニトール及びポロキサマー188を含有し、ここで、該ペプチド:マンニトール:ポロキサマー188の重量比は1:5:1.5から1:8:2.2を含む範囲であり、あるいは、マンニトール及びTween 80(登録商標)を含有し、ここで、該ペプチド:マンニトール:Tween 80(登録商標)の重量比は、1:2:1.5から1:8:2.2を含む範囲である新規ペプチド組成物。
(もっと読む)
NKG2Aに対するモノクローナル抗体
【課題】 免疫障害、特に、自己免疫または炎症性障害を処置する方法、ならびにそのような障害を処置するための治療ストラテジーにおける使用のための抗体および他の化合物を生成する方法を提供すること。
【解決手段】 障害の病因に寄与する樹状細胞の溶解をもたらすNK細胞上のNKG2A受容体の刺激を防止する抗体を見いだした。
(もっと読む)
イオン性複合体
【課題】リンペプチド/リンタンパク質によって安定化された無定形リン酸カルシウムおよび/または無定形リン酸フッ化カルシウムの超増量複合体を提供すること。
【解決手段】本発明は、リンペプチドまたはリンタンパク質(PP)によって安定化された無定形リン酸カルシウムまたは無定形リン酸フッ化カルシウムの複合体であって、PP1モル当たりのカルシウムが約30モルよりも高いカルシウムイオン含量を有する複合体を提供する。
(もっと読む)
関節リウマチに対する抗IL−6受容体抗体療法の有効性の予測方法
【課題】従来法よりも高い感度で、関節リウマチに対する抗IL-6受容体抗体療法の有効性を予測する方法を提供する。
【解決手段】関節リウマチに対する抗ヒトIL-6受容体阻害性抗体による治療の有効性を予測するための方法であって、(1)対象関節リウマチ患者から単離された末梢血単核球における、薬効マーカー遺伝子群から選択される少なくとも1つの遺伝子の発現レベルを測定すること、並びに、(2)(1)において測定した発現レベルと、関節リウマチに対する抗ヒトIL-6受容体阻害性抗体による治療の有効性とを相関付けることを含む。
(もっと読む)
肝保護剤、医薬組成物、食品、細胞等の保護方法、および細胞等保護用組成物
【課題】肝保護効果を有する肝保護剤およびその化合物を含有する組成物の提供。特に、天然起源の物質を含有し、経口投与可能な肝保護剤の提供。
【解決手段】N末端からβ−アラニン、オルニチン、オルニチンの順でペプチド結合したトリペプチドか、または、該トリペプチドの医薬的あるいは食品的に許容される塩を含有する肝保護剤。医薬的医薬的あるいは食品的に許容される塩を包含する。たとえば、塩酸、硫酸、硝酸、リン酸、酢酸、プロピオン酸、グリコール酸、クエン酸、酒石酸、コハク酸、グルコン酸、乳酸、マロン酸等との酸付加塩を挙げることができ、好ましくは塩酸等との塩であり、これらの塩は公知の方法により、遊離の該トリペプチドから製造でき、あるいは相互に変換することができる。この肝保護剤を医薬品組成物や食品に含有せしめる。
(もっと読む)
抗PCSK9抗体を用いた処置
【課題】低頻度で低用量のPCSK9拮抗抗体が、ヒト患者における高コレステロール血症および関連するCVDの発生率を低下させるために有効となるかどうか、また、そうであれば、どのような投薬レジメンがそのようなin vivoの有効性に必要であるかを明確にすること。
【解決手段】本発明は、血漿中の低密度リポタンパク質粒子の著しい上昇によって特徴づけられる障害に罹りやすい、またはそれと診断されたヒト患者を、PCSK9拮抗抗体単独でまたはスタチンと組み合わせて処置するための用量に関する。
(もっと読む)
抗Gaussiaルシフェラーゼ抗体およびその産生細胞
【課題】Gaussiaルシフェラーゼの発光機能の阻害活性を有する抗Gaussiaルシフェラーゼモノクローナル抗体を提供する。
【解決手段】Gaussiaルシフェラーゼの発光機能の阻害活性を有し、かつGaussiaルシフェラーゼを特異的に認識する抗Gaussiaルシフェラーゼモノクローナル抗体もしくはその機能性断片であって、前記機能性断片が、少なくともCDR1領域の特定の配列,CDR2領域の特定の配列,CDR3領域の特定の配列を含む軽鎖可変領域又は、重鎖可変領域を含むことを特徴とする。
(もっと読む)
抗ヒスチジンタグ抗体
【課題】検出感度及び特異性の高い抗ヒスチジンタグ抗体、該抗ヒスチジンタグ抗体をコードする遺伝子、ヒスチジンタグ融合ポリペプチドを高感度で検出できる検出方法・検出キット、及び、ヒスチジンタグ融合ポリペプチドを高効率で精製できる精製方法・精製キットの開発
【解決手段】特定のアミノ酸配列を有する重鎖可変領、及び特定のアミノ酸配列を有する軽鎖可変領域を備えた抗ヒスチジンタグ抗体、特定のアミノ酸配列と90%以上の配列同一性のアミノ酸配列を有する重鎖可変領域、及び特定のアミノ酸配列と90%以上の配列同一性のアミノ酸配列を有する軽鎖可変領域を備え、ヒスチジンタグに特異的に結合する抗ヒスチジンタグ抗体、該抗ヒスチジンタグ抗体をコードする抗ヒスチジンタグ抗体遺伝子、該抗ヒスチジンタグ抗体を用いたヒスチジンタグ融合ポリペプチドの検出方法・検出キット、ヒスチジンタグ融合ポリペプチドの精製方法・精製キットの提供
(もっと読む)
ワクチン組成物
【課題】新規ワクチン組成物の提供。
【解決手段】本発明は免疫防御作用のある、無害の、小児用に適したグラム陰性菌ブレブワクチンに関連する。ブレブ製造材料となるグラム陰性菌株の例はN. meningitidis、M. catarrhalis及びH. influenzaeなどである。本発明のブレブは、細菌染色体に対する1以上の遺伝子操作、たとえば防御抗原の発現増進、免疫支配的非防御抗原の発現抑制、LPSのリピドA部分の無害化などによる改善を図っている。
(もっと読む)
エルシニアSPP.ポリペプチド及び使用方法
【課題】本発明は、1又は複数のポリペプチドを含むエルシニア・エンテロコリチカを治療又は予防するための組成物、並びに当該ポリペプチドの製造方法及び使用方法を提供する。
【解決手段】組成物は、少なくとも2の単離ポリペプチドであって、各ポリペプチドは、83kDa、77kDa、又は66kDaの分子量を有する単離ポリペプチドを含み、そして少なくとも2の単離ポリペプチドであって、各ポリペプチドが40kDa、38kDa、又は37kDaの分子量を有する、単離ポリペプチドを含む。
(もっと読む)
アミノ酸41〜46に結合するモノクローナル抗体を用いたproBNPの検出方法
【課題】N末端proBNPの測定のための、および/またはN末端proBNPの臨床的に関連のある断片または亜集団のための、より特異的なアッセイを提供すること。
【解決手段】非修飾proBNPに特異的に結合する抗体であって、該抗体は、10ng/ml〜150ng/mlのN末端(1-76)非修飾proBNPを有する心不全患者試料において測定した非修飾proBNPの値に関して、直線回帰分析により決定した場合、少なくともr=0.95またはそれより大きいr値で、ハイブリドーマ細胞株MAB 1.21.3(DSM ACC2650)により産生される抗体と相関し、該非修飾proBNPに特異的に結合する抗体は、非修飾proBNPに対して少なくとも107L/molの結合親和性を有する、抗体。
(もっと読む)
MANSC1蛋白質に結合し、抗癌活性を有する抗体
【課題】優れた抗癌活性を有する新規抗体および該抗体を有効成分とする癌の治療または診断のための薬剤を提供すること
【解決手段】SST-REX法を利用して、癌細胞株由来のcDNAライブラリーから細胞表面に発現あるいは細胞から分泌される蛋白質をコードするcDNAを選抜し、選抜したcDNAがコードする蛋白質に対するモノクローナル抗体を作製して、in vitroおよびin vivoにおける抗癌活性を検討した結果、MANSC1蛋白質に結合し、優れた抗癌活性を有するモノクローナル抗体を見出した。さらに、MANSC1蛋白質における、この抗体におけるエピトープを含む領域を同定すると共に、この抗体の軽鎖および重鎖の可変領域の構造を決定することに成功した。
(もっと読む)
昆虫及びクモの防除のためのRNAi
【課題】昆虫及び/又はクモの防除のための非化合物に基づく新しいアプローチを提供する。
【解決手段】昆虫及び/又はクモ害虫の個体数を効果的に制御することができるRNAiのための標的ヌクレオチド配列及びアミノ酸配列。また、昆虫にRNAiを仲介するための二本鎖RNA領域を含むRNA構築物、DNA構築物、発現ベクター、宿主細胞、及びRNAiを用いて昆虫及び/又はクモを防除するための組成物。昆虫及び/又はクモの個体数の制御におけるその構築物、ベクター、宿主細胞、及び組成物の使用、並びにRNAiに基づき昆虫及び/又はクモ害虫を防除する方法における使用に適したキット。
(もっと読む)
ヒト凝固第VII因子ポリペプチド
【課題】血液凝固活性を有する新規のヒト凝固第VIIa因子ポリペプチド、並びに該ポリペプチドをコードするポリヌクレオチドコンストラクト、該ポリヌクレオチドを含み発現するベクター及び宿主細胞、薬剤的組成物、使用及び治療方法の提供。
【解決手段】野生型のアミノ酸配列と比較して一又は複数の置換を含み、ヒトの野生型と比較して、インビボ半減期の増加した機能を表し、また、内在性インヒビターによる不活性化に対する耐性が増加している第VIIa因子ポリペプチド。
(もっと読む)
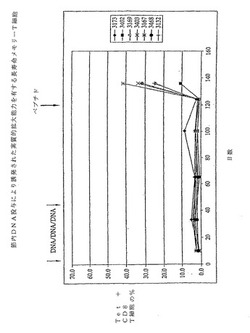
アデノ随伴ウイルス(AAV)配列の検出および/もしくは同定方法ならびにそれにより同定される新規配列の単離方法
【課題】組織もしくは細胞から得られたDNAのサンプル中のAAV配列の検出および単離方法、及び、本方法により同定されるAAV配列およびこれらの方法を使用して構築されるベクターを提供する。
【解決手段】核に侵入しならびにヘルパーウイルスの共感染の非存在下で細胞DNA中に組込み、そして潜在性感染を確立するアデノ随伴ウイルス(AAV)の能力を利用する方法。ヒトおよび非ヒト霊長類起源の組織ならびに他の供給源からのDNAからのAAVの配列の検出、同定および/もしくは単離のためのポリメラーゼ連鎖反応(PCR)に基づく戦略。有利には、他の組込まれたウイルスおよび非ウイルス配列の検出、同定および/もしくは単離。
(もっと読む)
融合タンパク質の自己タンパク質分解切断による組換えタンパク質の産生
【課題】 対象異種ポリペプチドの組換え産生のための方法であって、
(i)融合ポリペプチドをコードする核酸分子を含む発現ベクターで形質転換された宿主細胞を培養すること、ここで、該融合ポリペプチドは、ペスチウイルスの天然型オートプロテアーゼNproの少なくとも1つのシステイン残基が別のアミノ酸残基で置換されているペスチウイルスのオートプロテアーゼNproの誘導体と、異種ポリペプチドであり、第一のポリペプチドと、その第一のポリペプチドのC末端において、第一のポリペプチドの自己タンパク質分解活性によりその融合タンパク質から第二のポリペプチドが切断され得るように連結されている、第二のポリペプチドとを含み、該培養は融合ポリペプチドを発現させ、対応する細胞質封入体を形成させる条件下で行う、
(ii)該宿主細胞から該封入体を単離すること、
(iii)単離した封入体を可溶化すること、
(iv)該融合ポリペプチドから対象異種ポリペプチドの自己タンパク質分解切断を誘導すること、および
(v)切断された対象異種ポリペプチドを単離すること
を含む方法を提供すること。
【解決手段】 低いpIを有し、溶解度が高められた、ペスチウイルスの天然型オートプロテアーゼNproのある種の誘導体が広範な条件で使用に好適であることを見いだした。
(もっと読む)
オートタキシンアイソフォーム特異的抗体および検出方法
【課題】オートタキシンの測定方法であって、特定のアイソフォームの有無を検出可能な測定方法を提供すること。
【解決手段】オートタキシンを認識する抗体であって、Val−Glu−Pro−Lysからなるアミノ酸配列を含むオートタキシンを特異的に認識する抗体、および前記抗体を用いたオートタキシンの測定方法および測定試薬により前記課題を解決する。
(もっと読む)
リン酸化ペプチド、硬組織および/または異所性石灰化抑制剤、抗体ならびに硬組織および/または異所性石灰化促進剤
【課題】MEPE由来のASARMペプチドの石灰化抑制作用活性部位を利用する、硬組織および/または異所性石灰化抑制作用を有するリン酸化ペプチド、硬組織および/または異所性石灰化抑制剤、硬組織および/または異所性石灰化促進作用を有する抗体、ならびに、硬組織および/または異所性石灰化促進剤を提供する。
【解決手段】リン酸化ペプチドは、MEPEに由来するASARMペプチドの全部または一部のアミノ酸配列を含有し、当該アミノ酸配列における少なくとも二つ以上のアミノ酸残基がリン酸化されたセリンであり、かつ硬組織石灰化および/または異所性石灰化を抑制する作用を有することを特徴とする。抗体は、当該リン酸化ペプチドの活性中心である、リン酸化されたセリンを認識することを特徴とする。
(もっと読む)
221 - 240 / 12,187
[ Back to top ]