Fターム[4H045BA18]の内容
Fターム[4H045BA18]に分類される特許
341 - 360 / 719
アテローム性動脈硬化症を改善する経口投与ペプチド
【課題】本発明は、アテローム性硬化症の1つまたは2つ以上の症状を改善する新規なペ
プチドを提供する。
【解決手段】前記ペプチドは少なくとも1つのクラスA両親媒性らせんおよび少なくとも
1つのD−アミノ酸を含む。前記ペプチドは高度に安定であり、経口ルートにより容易に
投与することができる。“D”アミノ酸残基とともに製剤化されるか、および/または保護アミノ末端およびカルボキシル末端を有する、クラスA両親媒性らせんを含むペプチドは、生物に経口投与することが可能で、容易に取り込まれ、血清に送られて効果的に1つまたは2つ以上のアテローム性硬化症の症状を緩和する。
(もっと読む)
SETを調節する方法およびその使用
本発明は、SETとApoEペプチド誘導体などの結合剤とを接触させることによって、SET活性を調節する方法を提供する。本発明の一実施形態において、炎症性病態または神経性病態の治療のために、SET活性を調節することができる医薬品組成物を患者に投与する。本発明の別の実施形態において、ApoE誘導体のSETへの結合と競合できるか、または該結合を阻害できる結合剤をスクリーニングすることによって、炎症性病態または神経性病態の治療に有効な化合物を同定する。 (もっと読む)
アジュバント療法およびネオアジュバント療法のためのVEGF特異的アンタゴニストと初期ステージ腫瘍の治療
抗VEGF特異的アンタゴニストを用いた良性、前癌性又は非転移性の腫瘍の治療方法を本明細書中に開示する。また、抗VEGF特異的アンタゴニストを用いた良性、前癌性又は非転移性の腫瘍を発症するリスクにある被検体の治療方法を開示する。また、抗VEGF特異的アンタゴニストを用いた腫瘍の再発の治療又は予防方法、並びにネオアジュバント(術前補助)およびアジュバント(補助)癌療法におけるVEGF特異的アンタゴニストの使用を開示する。 (もっと読む)
造影剤
本発明は、プロテオグリカンに対して親和性を有する新規化合物及びかかる化合物を含む医薬品組成物を提供する。かかる化合物は、正に帯電した部分に結合したアミノ酸系のコア単位を含んでいる。かかる化合物はさらにインビボイメージングで検出可能な1以上のイメージング部分を含んでいるので、ヘパラン硫酸プロテオグリカンのようなプロテオグリカンのイメージングのための診断用造影剤として有用である。 (もっと読む)
コイルドコイル構造を有するリポペプチドのヘリックスバンドルおよび合成ウイルス様粒子
本発明は、コイルドコイルドメインを含むペプチド鎖と、該ペプチド鎖に共有結合で連結された、長いアルキルまたはアルケニル鎖を含む脂質部分と、ペプチド鎖に任意選択で連結された抗原とにより構成されるリポペプチドビルディングブロック;ならびに凝集によって形成されたリポペプチドヘリックスバンドルおよび合成ウイルス様粒子に関する。これらのバンドルおよび粒子の、ナノメートル規模の大きさおよび形状、水性の生理学的条件下における安定性、化学組成、B細胞エピトープおよびT細胞エピトープを組込む実現性、ならびに化学合成による生産は、該バンドルおよび粒子をワクチン送達手段として非常に適したものにしている。  (もっと読む)
(もっと読む)
ペプチド化合物PYY3−36の存否の確認方法
【課題】本発明は、ペプチド化合物PYY3−36の存否を簡便に、且つ、精度良く確認する方法を提供する。
【解決手段】被検薬剤中において、下記アミノ酸配列
H−Ile−Lys−Pro−Glu−Ala−Pro−Gly−Glu−Asp−Ala−Ser−Pro−Glu−Glu−Leu−Asn−Arg−Tyr−Tyr−Ala−Ser−Leu−Arg−His−Tyr−Leu−Asn−Leu−Val−Thr−Arg−Gln−Arg−Tyr−X
(アミノ酸配列中、XはOH、又はカルボン酸保護基を示す)
で表されるペプチド化合物PYY3−36の存否を確認する方法であって、
(1)前記被検薬剤及びキューカービチュリル[7]を溶媒とともに混合することにより溶液を調製する工程、及び
(2)工程(1)で得られた溶液を熱分析する工程
を含む、ペプチド化合物PYY3−36の存否の確認方法。
(もっと読む)
長期持続性抗新脈管形成ペプチド
【課題】新脈管形成に関する疾患の処置のための長期間の作用を有する改変クリングル5ペプチドを提供すること。
【解決手段】本発明によって、改変抗新脈管形成ペプチドが提供され、このペプチドは、血液成分のアミノ基、ヒドロキシル基、またはチオール基と反応して、安定な共有結合を形成する反応性基を有する。別の実施形態において、このペプチドはクリングル5ペプチドである。本発明の別の実施形態は、抗新脈管形成ペプチドのインビボ半減期を延長するための方法であって、この方法は、以下:反応性基をこのペプチドに結合し、そしてこの反応性基を血液成分の官能基と反応させて共有結合を形成する工程、それによって、この抗新脈管形成ペプチドのみのインビボ半減期よりも長いインビボ半減期を有する安定なインビボ結合体を形成する工程を包含する。
(もっと読む)
選択的グルカゴン様ペプチド−2(GLP−2)類似体
h[Gly2]GLP−2に比較して1つ以上の置換を含み、かつ増大した小腸/結腸および胃/結腸選択性の特性を有し得るGLP−2類似体を開示する。さらに詳細には、ここに開示する好ましいGLP−2類似体は、野生型GLP−2配列の位置(11、16、20、24)および/または(28)の1つ以上の位置における置換を、位置(2)および(3、5、7)のうち1つ以上の位置、および(10)におけるさらなる置換、および/または(31)ないし(33)のうち1つ以上のアミノ酸の欠失および/またはN−末端またはC−末端安定化ペプチド配列の付加との組み合わせにおいて含む。この類似体は、胃および腸関連疾患の予防または治療、および化学療法の副作用の寛解に特に有用である。 (もっと読む)
リン酸化−脱リン酸化反応検出用基質群およびそれを用いた検出方法
【課題】プロテインキナーゼまたはプロテインホスファターゼの反応性を簡便に測定可能な手段の提供。
【解決手段】プロテインキナーゼの天然に存在する基質に含まれるアミノ酸配列中のセリン残基をスレオニン残基に置換してなる人工ペプチド基質を少なくとも1種含有するプロテインキナーゼの基質群、前記基質群を固定してなるペプチドアレイ、前記ペプチドアレイおよび抗リン酸化スレオニン抗体を用いることを特徴とする、リン酸化および/または脱リン酸化反応を検出する方法、前記ペプチドアレイおよび抗リン酸化スレオニン抗体を用いることを特徴とする、プロテインキナーゼおよび/またはプロテインホスファターゼの活性化および/または不活化に基づく疾患の診断方法、ならびに前記ペプチドアレイおよび抗リン酸化スレオニン抗体を用いることを特徴とする、プロテインキナーゼまたはプロテインホスファターゼ活性を変動させる被検物質のスクリーニング方法。
(もっと読む)
生体応答性ポリマー
本発明は、生体活性物質をデリバリーするための生分解性ポリマーに関する。このポリマーは、ペプチダーゼ酵素による選択的加水分解に対して感受性のポリアミドリンカーを介して共有結合している生体活性物質を少なくとも1つ含む。ポリアミドリンカーが加水分解されると、インビボで生体活性物質が放出される。 (もっと読む)
新規なω−コノトキシン
【解決手段】
本発明は、一般式Iで表されるω−コノトキシンペプチドのシステイン残基2番及び3番の間の二次ループにおいて、11番及び/または12番アミノ酸残基をそれぞれIle及びAlaが位置するようにω-コノトキシンペプチドを製造する段階を含む、ω-コノトキシンペプチドのN-タイプカルシウムチャネルに対する結合可逆性を増加させる方法に関する。また、本発明は、N-タイプカルシウムチャネルに対する遮断活性及び特異性、そしてN-タイプカルシウムチャネルに対して著しく増加された結合可逆性を有する、優れた特性を有した新規ω−コノトキシンペプチド及び薬剤学的組成物に関する。
(もっと読む)
アミノ酸残基又はペプチド残基を有する化合物、及びその製造方法
【課題】本発明の目的は、様々な化合物や保持担体に結合可能であり、アミノ酸又はオリゴペプチドを有する側鎖が主鎖に結合した構造の新規化合物を提供することである。
【解決手段】以下の一般式(1)で示される化合物を提供する。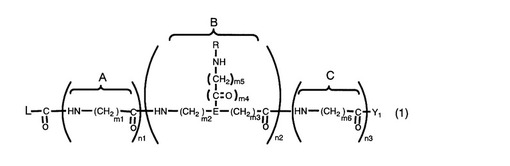
[式(1)中、n1は0〜10の整数、n2は1〜50の整数、及びn3は1〜10の整数を示し;m1は0〜100の整数、m2は0〜100の整数、m3は0〜100の整数、m4は0又は1の整数、m5は0〜100の整数、及びm6は0〜100の整数を示し;Y1は、水酸基又はアミノ基を示し;Eは、N又はCHを示し;Rは、アミノ酸残基、又は2〜100個のアミノ酸残基からなるペプチド残基を示し;Lは、ペプチド結合、ジスルフィド結合又はビオチンアビジン結合を形成可能な官能基(但し、アミノ基を除く)がリンカーを介して結合しているアミノ基を示す。]
(もっと読む)
アミノ酸伸長したインスリン
アミノ酸オリゴマーに結合したインスリンは、満足のいく特性を有する。 (もっと読む)
ウイルス感染の長期持続性融合ペプチドインヒビター
【課題】存在する抗ウイルスペプチドおよび/または抗膜融合性ペプチドの半減期を延長すること、および、これらのペプチドのインビボでのより長い期間の作用を提供することを、本発明の課題とする。
【解決手段】改変された抗ウイルスペプチドであって、抗ウイルス活性を示すペプチド、および、安定な共有結合を形成するように血液成分上のチオール基と反応性のマレイミド基を含む、改変されたペプチド、そのようなペプチドを含む結合体および組成物を提供することによって、上記課題は解決された。
(もっと読む)
ピロリ菌感染を治療するための新規の方法
本発明は、アミノ酸配列を含むポリペプチドであって、ポリペプチドのアミノ酸配列が、配列番号1に対応するアミノ酸配列を含むHPGGTの領域の一続きの連続アミノ酸配列と少なくとも80%同一であり、そのような領域が、(a)配列番号1に従ったアミノ酸配列のアミノ酸位置150〜200、又は(b)配列番号1に従ったアミノ酸配列のアミノ酸位置410〜480によって規定され、及びポリペプチドが、HPGGTの触媒活性を阻害することができる免疫応答を惹起するのに適する、前記ポリペプチドに関する。 (もっと読む)
PTH受容体モジュレーターとしてのペグ化PTHおよびその使用
哺乳動物における骨粗鬆症を含む骨量減少疾患の処置および予防のための薬理学的組成物および方法が、提供される。 (もっと読む)
細胞接着インヒビター
【課題】細胞接着および細胞接着媒介性の病理の阻害および予防に対して有用である新規の化合物の提供。
【解決手段】細胞接着および細胞接着媒介性の病理の阻害および予防に対して有用な、超遅発型抗原−4(VLA−4)に対するリガンドの結合を阻害する新規な半ペプチド化合物。および、これらの化合物を包含する薬学的処方物ならびに細胞接着および細胞接着媒介性の病理の阻害および予防に対してこれらの化合物を使用する方法。
(もっと読む)
改善された性質を有する再構成サーファクタント
本発明は、脂質担体、ネイティブなサーファクタントタンパク質SP−Cのポリペプチドアナログ、およびネイティブなサーファクタントタンパク質SP−Bのポリペプチドアナログを含む再構成サーファクタントに関するものである。本発明は、その薬学的組成物に、ならびにRDSおよび他の呼吸器障害の処置または予防のためのその使用にもまた関するものである。 (もっと読む)
N末端で置換されたグレリン類似体
本発明は、GHS受容体において活性な、より大きな安定性をもつ、下記の式によるグレリンのペプチジル類似体:(R2)-A1-A2-A3-A4-A5-A6-A7-A8-A9-A10-A11-A12-A13-A14-A15-A16-A17-A18-A19-A20-A21-A22-A23-A24-A25-A26-A27-A28-R1[式中のA1〜A2、R1およびR2の定義は明細書中に示され、ただし、N末端アミノ酸はInp、1−Apeおよび4−Apeよりなる群から選択しなければならない]、その医薬的に許容できる塩、ならびに有効量の前記化合物を含む医薬組成物、ならびにその療法用途および療法以外の用途を含む。 (もっと読む)
糖尿病発症を予防または遅延させるためのゾヌリンのペプチドアンタゴニストの使用方法
【課題】ゾヌリンのペプチドアンタゴニストを用いて糖尿病発症を予防または遅延させる方法を提供すること。
【解決手段】糖尿病発症を予防または遅延させる方法であって、該方法は、糖尿病発症を予防または遅延させる必要のある被験体に、薬学的に有効量のゾヌリンのペプチドアンタゴニストを投与する工程を包含し、ここで該ペプチドアンタゴニストは、閉鎖帯毒素レセプターに結合するが、哺乳動物の接着結合の開きを薬学的に修飾しない、方法。
(もっと読む)
341 - 360 / 719
[ Back to top ]



