Fターム[4H045GA45]の内容
Fターム[4H045GA45]に分類される特許
21 - 40 / 104
高濃度フィブロインゲルの製造方法
【課題】人体組織との適合性に優れ保湿性、付着性、展性が高いシルクプロテインの特性を発揮できる10重量%以上の高濃度フィブロインゲルを提供する。
【解決手段】高濃度非結晶性フィブロインゲルは、タンパク質に変性を齎す化学物質や長時間処理を行うことなく、従来に無いシルクプロテインの特性を醸し出す高濃度フィブロインゲルの製造を可能にした。さらに加圧蒸気滅菌処理に耐え、化粧料のみならず医療用等へ用途を広げた。
(もっと読む)
シャペロニン−目的タンパク質複合体及びその製造方法
【課題】単離・精製された膜受容体を活性保持した状態で安定化することができ、膜受容体の取扱いを容易にする技術を提供する。
【解決手段】2個以上のシャペロニンサブユニットが直列に連結されてなるシャペロニン連結体と、当該シャペロニン連結体に対して非共有結合的に結合している目的タンパク質とを含み、前記シャペロニンサブユニットがリング状に配置されてなるリング状構造体を形成可能であると共に当該リング状構造体の内部に前記目的タンパク質を格納可能なシャペロニン−目的タンパク質複合体であって、前記目的タンパク質は、動物細胞内で発現させた膜受容体であることを特徴とするシャペロニン−目的タンパク質複合体が提供される。シャペロニン連結体と目的タンパク質とをタグを介して結合することもできる。
(もっと読む)
改良された抗体分子を含有する製剤
本発明の目的は、改良された抗体分子を含有する製剤を提供することである。ヒト化抗IL-6レセプターIgG1抗体であるトシリズマブの可変領域および定常領域のアミノ酸配列を改変することで、抗原中和能を増強させつつ、薬物動態を向上させることで投与頻度を少なくし持続的に治療効果を発揮し、且つ、免疫原性、安全性、物理化学的性質(安定性および均一性)を向上し、トシリズマブより優れた第2世代の分子からなる製剤を提供することである。本製剤は、安定剤として好ましくはアルギニンを含有し、溶液または固体の形状で提供される。 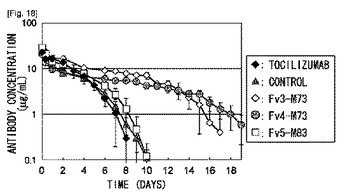 (もっと読む)
(もっと読む)
活性因子を凍結乾燥するための方法
【課題】溶液を凍結乾燥するための方法を提供すること。
【解決手段】容器内において、活性薬剤の溶液(50)を凍結乾燥するためのプロセスが提供される。活性薬剤の溶液は、容器内に入れられ、この容器は、カバープレート(60)で覆われ、凍結乾燥装置内に配置される。凍結乾燥は、放射か、対流か、もしくはその両方によって乾燥するように行われ得る。このプロセスによって作製されるデバイス(活性薬剤−プラスチック投与デバイス(例えば、シリンジ(20))であり、凍結乾燥ケークの形態で活性薬剤を含む)、およびこのような投与デバイスのアレイも、また提供される。
(もっと読む)
タンパク質結晶およびイオン性ポリマーの複合体
【課題】種々のタンパク質結晶の徐放性組成物を開発すること。
【解決手段】本発明は、タンパク質結晶とイオンポリマーとの複合体、およびそのような複合体を含んで成る組成物に関する。本発明はさらに、これらの複合体および組成物を製造する方法も提供する。本発明はさらに、タンパク質に基づく療法の持続放出を必要とするかまたはそれによって改善される疾患を有する個体の治療法も提供する。種々のタンパク質結晶の徐放性組成物を開発するために、本発明は、タンパク質の両性性質を利用する。また、本発明は、薬物療法の持続放出を必要とするかまたはそれによって改善される疾患状態の治療法を提供する。
(もっと読む)
タンパク質の熱安定化方法および熱安定化されたタンパク質溶液
【課題】安価な方法で、また幅広い温度領域で、さらに幅広いタンパク質に対して熱安定化を行うことのできるタンパク質の熱安定化法を提供する。
【解決手段】タンパク質を含有する溶液に、不活性雰囲気において炭化された、有機物の炭化物を粉砕することにより得られた非晶質炭素微粒子を添加する。非晶質炭素微粒子は、例えば木材、竹などの有機物を不活性雰囲気において所定の温度で順次温度を上げて加熱し、前記雰囲気中及び有機物中の炭素以外の所期成分を、500℃以下の温度において分解温度の低いものから順次熱分解させて個別的に遊離させて製造された炭化物を粉砕することにより製造されたものであり、粒径1nm以下のような炭素超微粒子の集合体からなっている。
(もっと読む)
タンパク質の安定化剤
【課題】(1)病原体汚染の可能性が低い、(2)発光タンパク質の安定化に効果的である、(3)凍結乾燥した場合であってもタンパク質の活性への影響を最小化できる、といった効果を有する優れたタンパク質の安定化剤を提供する。
【解決手段】魚類由来のペプチドを含有するタンパク質の安定化剤。魚類由来のペプチドが、魚類由来のコラーゲンもしくはゼラチンを加水分解して得られたペプチドである、該安定化剤。タンパク質がカルシウム結合型発光タンパク質である、該安定化剤。
(もっと読む)
高濃度の低粘度懸濁液
本発明は、1又は2以上のタンパク質若しくはペプチドを含む1若しくは2以上のサブミクロン又はミクロンサイズの非結晶性粒子を含有する、薬学的に許容される溶媒を用いた高濃度の低粘度懸濁液も提供する。任意選択により、少なくとも20mg/mlの濃度と、振盪又は撹拌により懸濁可能な2〜100センチポアズの溶液粘度とを有する高濃度の低粘度懸濁液を形成するための、前記薬学的に許容される溶媒中の1又は2以上の添加物であって、送達時に前記1若しくは2以上のサブミクロン又はミクロンサイズのペプチドが溶解しておりペプチド凝集体を形成しないために、21〜27ゲージの針により注射可能な添加物。 (もっと読む)
水溶性絹フィブロイン粉末の製造方法
【課題】溶解性がよく、長期保存が可能で、高濃度の絹フィブロイン溶液に調整可能な水溶性絹フィブロイン粉末の製造方法を提供する。
【課題を解決するための手段】本発明に係る絹フィブロイン粉末の製造方法は、絹原料を溶解して絹フィブロイン溶液とする工程と、この絹フィブロイン溶液を限外濾過膜により濾過し、不溶性成分を除去する工程と、絹フィブロイン溶液を脱塩する脱塩工程と、不溶性成分を除去し、脱塩した絹フィブロイン溶液を乾燥し粉末化する工程を含むことを特徴とする。
(もっと読む)
インシュリンの再折りたたみ方法
本発明は、システイン架橋が正確に結合したインシュリン前駆体、そのアナログまたは誘導体を入手する方法に関する。本方法は、システインまたは塩酸システインおよび1つ以上のカオトロピズム促進剤を含む水溶液または緩衝液にインシュリン前駆体、インシュリンアナログまたは誘導体を可溶化する工程を含む。可溶化させた混合物に希釈剤を添加すること(リバース希釈)によって、前記可溶化された前駆体は再び折り畳まれる。さらにまた、可溶化された前駆体(前駆体濃度は0.65g/リットルよりも高い)の再折畳みは、場合によって約5−40%(v/v)の1つ以上のアルコール性溶媒または非プロトン性溶媒を含む希釈剤で反応混合物を希釈することによってもまた実施することができる。 (もっと読む)
糖尿病の処置に有用な組成物
【課題】空腹時低血糖を引き起こすことなく、長期間、コントロールされた様式でインスリンを放出するインスリン製剤が必要とされている。
【解決手段】本発明は、代謝障害、特に糖尿病を処置するためのタンパク質治療薬として有用な、超分子インスリンアセンブリーおよび超分子エキセンディン-4アセンブリーを提供する。本発明で開示する超分子アセンブリーは、不溶性かつ凝集したオリゴマーのタンパク質からなる。本発明は、超分子アセンブリーを含む薬剤組成物も提供する。
(もっと読む)
心筋トロポニンT含有水溶液及びこの製造方法
【課題】心筋トロポニンT溶液を標準液とする場合、従来の凍結乾燥による方法では、保存安定性は良いが使用時に水を加えなければならないため操作が煩雑となり、結果として標準液中の抗原濃度に誤差を生じやすい。また、牛血清アルブミンや動物血清などのタンパク質を添加しても、溶液中での心筋トロポニンTの安定性が悪く、長期間の保存安定性を確保することが困難である。
【解決手段】pHが6.0〜8.5である心筋トロポニンTを含む水溶液(A)を30℃〜50℃で72時間〜240時間加熱処理して得られる心筋トロポニンT含有水溶液(B)。
(もっと読む)
タンパク質及びポリペプチドを安定化する方法
小さい群の突然変異型を産生するために、所定のアミノ酸をタンパク質又はポリペプチドの選択位置に導入する、上記タンパク質及びポリペプチドを修飾、特に安定化する方法。この方法は、或る特定のアミノ酸がタンパク質又はポリペプチドの安定性に重要な役割を果たすという前提に基づいている。それから、生成された突然変異型は、安定性及び/又は機能、例えば親和性に関してさらに解析することができる。さらに、適当な突然変異型を組み合わせて、さらに最適なタンパク質又はポリペプチドを得ることができる。また、安定化した例示的なポリペプチド、並びに不安定化した又は安定化したタンパク質又はポリペプチドを同定及び/又は解析するのに好適な方法が提供される。この方法を、タンパク質の構造及び機能における特定のアミノ酸の役割を研究するのに、並びに新規の又は改善した、例えば安定化したタンパク質及びポリペプチド、例えば抗体及び単一可変ドメインを開発するのに使用することができる。 (もっと読む)
ペプチド修飾の方法
本発明は次の事項に関する。式(I)のC末端キャッピング基をペプチドまたはペプチドミメティックに組み込むことを含む、ペプチドまたはペプチドミメティックのトリプシンによる分解に対する耐性を向上させる方法:X−Y−Z(I)、式中、XはN原子であり、N、OおよびSから選択される2個までのヘテロ原子が組み込まれていてもよい、分岐したまたは分岐していないC1〜C10アルキルまたはアリール基により置換されていてもよい;Yは、−Ra−Rb−、−Ra−Rb−Rb−および−Rb−Rb−Ra−から選ばれる基を表し、RaはC、O、SまたはNであり、RbはCである;RaおよびRbの各々は、C1〜C4アルキル基により置換されていても、非置換であってもよい;Zは、各々5個もしくは6個の非水素原子の環状基を1〜3個含み、2個以上の環状基の各々は融合していてもよく、1個以上の環状基は置換されていてもよい基である;Z部分には最高15個の非水素原子が組み込まれていてもよい;そして、YとZとの間の結合は、YのRaもしくはRbとZの環状基のうちの一つの非水素原子との間の共有結合である。 (もっと読む)
精製されたP−糖タンパク質を安定化させるための方法
精製されたP−糖タンパク質(P−gp)を作製するための方法が提供される。この方法は、i)細胞膜から得られるP−gpおよび他のタンパク質の混合物を可溶化すること;
ii)不溶物を遠心分離によって除くこと;iii)P−gpおよび他のタンパク質の混合物を精製カラムに入れること;ならびにiv)精製カラムに少なくとも1つの洗浄緩衝液を流して、望まれないタンパク質を除き、その後、少なくとも1つの溶出緩衝液を流して、P−gpを回収することを含み、前記緩衝液の1つまたは複数が二糖類を含有する。
(もっと読む)
タンパク質含有水溶液安定化剤及びタンパク質含有水溶液の安定化方法
【課題】診断・検査薬、医薬品として広く利用される酵素、組み換えタンパク質、糖タンパク質、ペプチドなどの水溶液中のタンパク質を安定化し、製造工程および保存期間中にタンパク質の生理活性を長期的に低下させないタンパク質安定化剤、及び安定化方法の提供。
【解決手段】タンパク質を含んでなる水溶液の安定化剤であって、下記一般式(1)で表される化合物(A)及び/又はその塩(B)を含んでなるタンパク質含有水溶液の安定化剤。[式1]
[一般化学式(1)中、有機基Xは、エステル基又はN−アルキルアミド基;有機基Yは、N−アルカノイルアミド基又はイミノ基を表す。]
(もっと読む)
プロテアーゼに対して安定しているペグ化インスリンアナログ
プロテアーゼに対する耐性を示す新規のペグ化されたインスリンアナログは、効果的に、肺又は口腔に投与することができる。インスリンアナログはB25H及びA14E又はA14Hを含む。B29Kでペグ化されている。  (もっと読む)
(もっと読む)
抗体処方
本発明は、標準処方(30mMクエン酸塩、100mM NaCl、pH6.5など)に比べてより安定であるせん断および温度安定性抗体処方に関する。本発明のせん断および温度安定性抗体処方は、応力条件に曝される場合に沈殿の減少を示すが、標準処方は、凝集していた。そのDSC(示差走査熱量計)プロファイルに見られるように、熱力学的に2種の処方は類似しているので、この結果は予測不可能であった。 (もっと読む)
蛋白質を含む液状組成物中における蛋白質の安定化方法
【課題】蛋白質を含む液状組成物中における蛋白質の優れた安定化方法を提供する。
【解決手段】(1)水溶性高分子化合物と(2)アミノ酸又はその誘導体及び/又は無機塩を液状組成物中に共存させることを特徴とし、水溶性高分子化合物がポリエチレングリコール、ポリビニルアルコール、ポリアクリルアミド、ポリビニルピロリドンから選ばれる少なくとも1種類であり、水溶性高分子化合物の重量平均分子量が200〜50000であり、水溶性高分子化合物の濃度が10mg/ml〜250mg/mlであることを特徴とする蛋白質を含む液状組成物中における蛋白質の優れた安定化方法。
(もっと読む)
アポフェリチン
【課題】産生宿主関連成分あるいはその他の夾雑成分を含まず、着色が充分に抑えられたアポフェリチン及びその製造方法を提供する。
【解決手段】
金属イオンを含有しない緩衝液、及び金属イオンを含有しない塩を用いて、キレート剤共存下にてフェリチン含有試料又はフェリチン産生宿主の培養液からアポフェリチンを精製することにより、産生宿主関連成分あるいはその他の夾雑成分を含まず、着色が充分に抑えられ、かつ含有する金属が特定値以下のアポフェリチンを得る。
(もっと読む)
21 - 40 / 104
[ Back to top ]