Fターム[2G041FA13]の内容
その他の電気的手段による材料の調査、分析 (22,023) | 検出対象 (2,606) | 非金属 (2,002) | 有機 (1,818) | 高分子 (1,425) | 生体物質 (1,377) | 単に配列を確定するためのもの (98)
Fターム[2G041FA13]に分類される特許
61 - 80 / 98
迅速かつ定量的なプロテオーム解析および関連した方法
【課題】プロテオーム解析のための迅速で、効率的でかつ費用効率的な方法の提供。
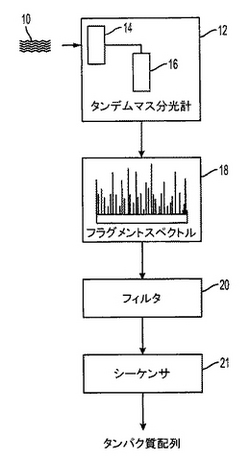
【解決手段】ポリペプチドを同定する方法であって、以下:(a)ポリペプチドの集団由来の親ポリペプチドのサブセットの質量と該親ポリペプチドのサブセットのフラグメントの質量を同時に決定する工程;(b)注釈されたポリペプチドインデックスと該決定された質量を比較する工程;および(c)該決定された質量を有する該注釈されたポリペプチドインデックスの1つ以上のポリペプチドを同定する工程、を包含する方法など。
(もっと読む)
アルツハイマー病についてのバイオマーカーとしての神経分泌タンパク質VGFのフラグメント
本発明は、患者のアルツハイマー病状態を認定するのにおいて有用な神経分泌タンパク質VGFペプチドを提供する。詳細には、このペプチドおよびその改変型は、被験体サンプルをアルツハイマー病または非アルツハイマー病として分類するために用いられ得る。このペプチドバイオマーカーは、SELDI質量分析法によって検出され得る。本発明によって、ある被験体におけるアルツハイマー病状態を認定するための方法が提供され、この方法は、(a)該被験体由来の生物学的サンプルにおいて少なくともVGFペプチド−1を測定する工程と、(b)この測定値とアルツハイマー病状態とを関連付ける工程とを、包含する。  (もっと読む)
(もっと読む)
分画を用いる化学分析の方法および装置
化学物質を分析する方法(100)は、混成サンプルを、各々が様々の濃度比ではあるが2つのポリペプチドの部分を含む少なくとも2つのサンプル部分に分画し、消化し、およびサンプル部分(110)の各々でLC/MSを行い、およびLC/MSを介して観察される前駆体イオンを、LC/MSで提供される強度データに応じてこれらの対応のポリペプチドと関連させる(170)ことを含む。両方のサンプル部分で実質的に類似の強度比を有する前駆体イオンの集合が、同じポリペプチドと関連していることが決定される。  (もっと読む)
(もっと読む)
ナトリウム利尿ペプチドに関連したポリペプチド、並びにこれらの同定および使用法
本発明は、関心対象の所望のポリペプチドに対する抗体と結合するポリペプチドの同定および使用に関する。ナトリウム利尿ペプチドおよびこれらの前駆体、特にBNPを一例として使用し、本発明は、生体試料中、最も好ましくは血液由来試料中に産生される、BNPに対する抗体に結合する多くのナトリウム利尿ペプチド断片を記載する。このような断片の産生は、なかでも組織内へのナトリウム利尿ペプチドの放出を誘発する事象の開始と試料を入手または解析する時間との間の経過時間;試料獲得と試料を解析した時間との間の経過時間;問題の組織試料のタイプ;貯蔵条件;存在するタンパク質分解酵素の量などの関数でありうる持続的なプロセスであることから、正確な予後または診断の結果を提供するために、1つまたは複数のナトリウム利尿ペプチドのためのアッセイ法をデザインするとき、およびこのようなアッセイ法を行うときの両方においてこのような断片を使用してもよい。 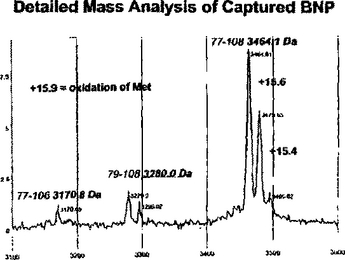 (もっと読む)
(もっと読む)
品質スペクトルの自動検出
【課題】品質スペクトルを自動的に検出すること。
【解決手段】本出願は、マスフラグメントスペクトルの一部にアクセスし、このスペクトルのピーク対の差異に応じたベクトルを構築し、このベクトルに応じたスペクトルを選択するシステム及び/又は方法を提供する。
(もっと読む)
内部標準ペプチドを用いて生体由来試料に含まれる標的タンパク質を定量する方法
【課題】
複数のタンパク質の混合物である生体由来試料に含まれる標的タンパク質を検出・同定し、定量するための、新規タンパク質定量法を提供する。
【解決手段】
標的タンパク質に対するペプチドを合成し、安定同位体で標識した後、内部標準として生体由来試料に既知量を添加する。その後、プロテアーゼにてタンパク質をペプチドへ消化して、液体クロマトグラフィーを用いてペプチドの分離を行い、質量分析計で分析を行なう。既知量の内部標準ペプチドとタンパク質由来ペプチドのシグナル面積を比較することで、定量を行なう。
(もっと読む)
生物薬剤の免疫原性に関するエピトープの同定のための方法
【課題】本発明は、生物薬剤の免疫原性に関するエピトープの同定のための方法を提供することを課題とする。
【解決手段】本発明は、以下の工程を含む免疫原性に関与するペプチドを同定するための方法に関する:a)0.1〜5μgの分子を提供する数の抗原提示受容体(APR)を発現する細胞を提供する工程、b)(a)からの細胞を免疫原性ペプチドの供与源と接触させる工程、c)細胞からAPR分子-免疫原性ペプチド複合体を単離する工程、d)APR分子から会合したペプチドを溶出する工程、e)免疫原性ペプチドを同定する工程、f)エピトープとして同定された免疫原性ペプチドを検証する工程。
(もっと読む)
オリゴ糖の同定方法、オリゴ糖の配列分析方法
【課題】 本発明は、上記事情に鑑みなされたものであって、その目的は、正確かつ容易にオリゴ糖の種類を同定できるオリゴ糖の同定方法を提供することである。
また、本発明の別の目的は、N−アセチルヘパロサン由来のオリゴ糖において、糖修飾基に関する情報が得られるオリゴ糖の配列分析方法を提供することである。
【解決手段】 本発明に係る同定方法は、N−アセチルヘキソサミンとウロン酸との交互繰り返し構造を有する被検オリゴ糖の質量分析のn乗スペクトル(nは2以上の整数)を用いて被検オリゴ糖の同定を行う。また、本発明に係る配列分析方法は、N−アセチルヘパロサン由来の被検オリゴ糖の質量分析のn乗スペクトル(nは2以上の整数)を用いて前記被検オリゴ糖における修飾基情報を得る。
(もっと読む)
ケラタン硫酸由来オリゴ糖の同定方法
【課題】 ケラタン硫酸から得られるオリゴ糖を微量試料で正確かつ迅速に同定する方法を提供すること。
【解決手段】 ケラタン硫酸由来の被検オリゴ糖をエレクトロスプレー・イオン化(ESI)法でイオン化して多段階質量分析(MSn分析)することにより糖鎖配列の解析を行うケラタン硫酸由来のオリゴ糖の同定方法であって、
前記被検オリゴ糖のMS1分析を行い、分子量関連イオンのスペクトルデータを得る工程と、前記MS1分析で得られた分子量関連イオンのMS2分析を行い、0,2Arイオンのスペクトルデータを得る工程と、前記MS2分析で得られた0,2ArイオンのMS3分析を行い、2,4Arイオンのスペクトルデータを得る工程と、前記MS3分析で得られた2,4ArイオンのMS4分析を行う工程と、を含み、
前記2,4ArイオンのMS4分析により得られたスペクトルデータから前記糖鎖配列の解析を行うことを特徴とするケラタン硫酸由来のオリゴ糖の同定方法。
(もっと読む)
還元性物質を用いるタンパク質又はペプチドの構造解析手法
【課題】質量分析測定試料となるタンパク質又はペプチドがジスルフィド結合を有するものであっても、その一次構造解析を迅速且つ容易に行うことができる方法を提供する。
【解決手段】MSの2乗以上の分析が可能なMALDI(マトリックス支援レーザー脱離イオン化)質量分析装置により、マトリックスとしてジスルフィド結合に対して還元性を示す物質を用いて、タンパク質又はペプチドのMS分析を行い、前記MS分析で得られた分子量関連イオンをプリカーサイオンとしてMSn分析を行い、タンパク質又はペプチドのアミノ酸配列情報を得る、タンパク質又はペプチドの構造解析手法。
(もっと読む)
インビボにおける神経系由来生体分子の代謝測定方法
本発明は、アルツハイマー病といった神経性及び神経変性疾患又は障害の臨床疾患進行の初期又は脳障害及び臨床症状の発症前における診断、観察、及び治療効果の評価の方法に関する。被験者の中枢神経系(CNS)内で産生される生体分子のインビボでの代謝の測定方法が提供される。 (もっと読む)
心臓血管障害に関連する分泌ポリペプチド種
本発明は心臓血管障害を有する患者の血漿において高レベルで循環するヒト分泌ポリペプチドを開示する。本発明はまた診断、予後診断および薬物開発のためのポリペプチド、これらをコードするポリヌクレオチド、およびこれらのポリペプチドに特異的な抗体をも提供する。  (もっと読む)
(もっと読む)
質量分析プリカーサーイオンの選択
本発明は、質量分析計でフラグメント化するためのサンプルポリペプチドのプリカーサーイオンを選択する方法、サンプルポリペプチドに対する少なくとも1つの推定アミノ酸配列を決定する方法、それらに用いられる装置およびコンピュータプログラムに関する。 (もっと読む)
複合した混合物中のタンパク質またはタンパク質機能の迅速定量分析
【課題】従来の技術に固有の制限を克服するproteome分析において使用され得る方法および試薬を提供する。
【解決手段】自動化LC/MS/MSシステムであって、以下: (a)キャピラリーHPLCと流体接続するオートサンプラー (b)該キャピラリーHPLCと流体接続するエレクトロスプレーイオン化三連四重極MS/MS装置;および (c)該オートサンプラー、キャピラリーHPLCおよびMS/MS装置と電気接続する装置制御およびデータ分析システムを備える、システム。
(もっと読む)
質量分析法を用いたアミノ酸配列同定方法
【課題】計算処理の効率化を図り、精度の高いアミノ酸配列同定方法を提供する。
【解決手段】 マススペクトルを入力する入力手段と、プレカーサーの質量より考えられるアミノ酸組合せを算出し、アミノ酸の理論質量値と、上記入力手段から入力したマススペクトルのうち特定のマススペクトルの質量電荷比から算出される実測質量値との差を算出し、算出した差のなかで所定の範囲内にあるものを同定し、同定した差を算出するのに使用したN個のアミノ酸をd+1〜d+N番目のアミノ酸の候補アミノ酸とする候補アミノ酸検索手段と、アミノ酸の組合せに従いながらアミノ酸同定候補を絞り込み、各候補アミノ酸に関してイオン強度より算出した正規化相対イオン強度とアミノ酸巻の切れやすさの確率を評価関数に用いてそれぞれ評価値を演算する評価値演算手段と、評価値を用いてペプチド断片におけるアミノ酸配列を同定する同定手段とを備えるアミノ酸配列同定装置。
(もっと読む)
タンパク質データの分析
【解決課題】 偽陽性判定の恐れが無い、タンパク質データの判定方法を提供する。
【解決手段】 タンパク質試料の質量分析の実測値をメモリに記憶し、演算装置が前記実測値とデータベースとに基づいてタンパク質の同定を行うデータ処理方法において、前記演算装置は、前記実測値と理論値との検量線を試料の測定の都度作成し、この検量線に基づいて前記実測値から得られるピークリストを較正し、較正されたピークリストとデータベースとを照合して、前記タンパク質を同定する。
(もっと読む)
アミノ末端およびカルボキシル末端の同時的配列分析
本発明は、質量分析によってカルボキシルおよびアミノ末端のアミノ酸配列を導き出すことによって、ポリペプチドを特定するための新規方法に関する。本法は、電子移動解離誘発陰イオンによって、高度に荷電したペプチド前駆体イオン(例えば、z>4)を解離する工程、次いで、これらの試薬を除去し、第2のプロトン移動誘発陽イオン型を導入する工程を含む。ETD産物を主に+1電荷状態に変換して高度に荷電したcおよびz-型断片を低減し、アミノおよびカルボキシル末端の配列をそれぞれ明らかにするために簡単に解釈することが可能な一連のcおよびz-型断片イオンを含むm/zスペクトルを生成するように、第2のPTR反応持続時間を調節する。 (もっと読む)
バインディングザイムアレイ及びハイスループットプロテオミクス方法
異なる生物試料間のポリペプチド変動存在又は不存在の同定方法及び異なる生物試料中の1以上のポリペプチドの変動を速やかに同定するためのハイスループットスクリーニングの対応する作成方法を本明細書で提供する。具体的には、例えば、ホスホリル部分が付着されたポリペプチドの存在又は不存在などの生物試料中の特定のポリペプチド上の翻訳後修飾における変動を同定することができる。これらの方法では、触媒不活性化酵素(すなわち、バインディングザイム)を基質特異的結合タンパク質として利用する。これらのバインディングザイムは生物試料中の1つ以上の基質と結合することができ、結合基質はある試料を別のものと区別するためのマーカーとして働くことができる。これらの方法は、それらの同定のための基質の単離、試料中の基質の検出、並びに医療用医薬品の発見及び開発にも有用である。 (もっと読む)
アミノ酸配列パターン・マッチング
試料内パターン一致、群内パターン一致、ならびにさらなる分析またはデータ・マイニングを目的とするワード・マッチングを決定することが可能な種々のフィルターおよび逐次フィルターを用いることによって、複数のアミノ酸でのパターン一致を突き止める方法。フィルターとして、スコアリング・スキーム、MS/MSにかけられる共通イオンの配列と走査回数との比較、およびパターン一致候補を得るための娘イオン減法を用いることが挙げられる。  (もっと読む)
(もっと読む)
化学試薬を利用したアスパラギン酸位置で蛋白質開裂
本発明は質量分析法で特定試料に含まれているポリペプチドの同定方法に関するものである。さらに詳しく、本発明はプロテオミック分析のための試料の製造法に関するものである:特定開裂規則(N-末端、またはC-末端のアスパラギン酸での開裂)で蛋白質をペプチドに断片化する方法を提供し、前記ペプチドは質量分析器で分析するのに適している。 (もっと読む)
61 - 80 / 98
[ Back to top ]