Fターム[4H045FA52]の内容
ペプチド又は蛋白質 (143,989) | 製造方法 (18,984) | 化学合成によるもの (4,727) | 化学修飾によるもの(ペプチド結合の切断、形成以外のもの) (684) | アミノ酸側鎖の修飾 (137)
Fターム[4H045FA52]に分類される特許
121 - 137 / 137
HIVgp41由来ペプチドの部位特異的化学修飾
HIV gp41由来ペプチドを部位特異的に化学修飾するための方法を提供する。この方法では、合成の間に、HIV gp41由来ペプチドの1つ以上のアミン基が化学的保護剤によってブロックされるように選択され、また1つ以上のアミン基が無保護となるように選択されて、アミン反応性官能基と反応するように遊離のままである。得られたHIV gp41由来ペプチドは、HIV gp41由来ペプチドの1つ以上の遊離(無保護)アミン基にポリマーを共有結合させることにより、HIV gp41由来ペプチドとポリマーからなる実質的に均一なコンジュゲートを製造するために使用することができる。 (もっと読む)
カスパーゼインヒビターおよびそれらの使用
本発明は、式(I)の化合物を提供する:ここで、変数は、本明細書中で定義したとおりである。本発明はまた、式(I)の化合物を調製する方法、それらの中間体、これらの化合物を含有する薬学的組成物、ならびにこれらの化合物および組成物を使用する方法を提供する。本発明はまた、カスパーゼを阻害するためにこのような化合物および組成物を使用する方法を提供する。これらの化合物は、選択的なカスパーゼ−1/カスパーゼ−8インヒビターとして、特に有用である。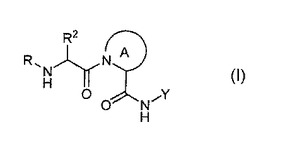
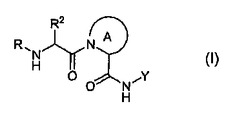 (もっと読む)
(もっと読む)
骨形成蛋白−2の正のモジュレーター
【解決課題】 骨形成蛋白活性のモジュレーターである化合物を開示する。
【解決手段】 化合物は非成長因子ヘパリン結合領域、リンカー及び骨形成蛋白受容体に特異的に結合する配列を有する合成のペプチドである。骨患部、変性間接疾患の治療における、及び、骨形成の増強のために本発明の化合物を使用し得る。
(もっと読む)
糖尿病、インスリン抵抗性、及び肥満症の治療のためのGIPペプチド・アナログ
当該発明は、胃抑制ペプチド(GIP)の拮抗薬であるペプチド・アナログを提供する。GIP1-42をベースとする前記ペプチドは、酵素であるジペプチジル・ペプチダーゼ IV(DPP IV)による分解への高い抵抗性を持つ置換及び/又は修飾を含む。本発明は、N末端で修飾したGIPの製法及び糖尿病の治療のための前記ペプチド・アナログの使用方法も同様に提供する。 (もっと読む)
化学修飾されたヒト成長ホルモン受容体アンタゴニスト結合体
本発明は、単一のポリエチレングリコール部分をN末端に結合させることによって調製された、化学修飾されたヒト成長ホルモン(hGH)受容体アンタゴニストを提供する。本発明による化学修飾されたタンパク質では、ペグ化の不均一性が減少しており、さらに結合親和性も増大している可能性がある。
【図1】
 (もっと読む)
(もっと読む)
ペプチドのO結合型グリコシル化
本発明は、野生型ペプチドには存在しないO結合型グリコシル化部位を含むポリペプチドを提供する。本発明のポリペプチドには、水溶性ポリマー、生体分子の治療薬などの化学種が、完全なO結合型グリコシル残基を介してポリペプチドに共有結合している複合糖質が含まれる。また、本発明および方法のペプチドを作製する方法、それらのペプチドを含有する医薬組成物、ならびに、所望の応答を実現するのに十分な量の本発明のペプチドを投与することによって哺乳動物の疾患を治療、改善、または予防する方法も提供される。 (もっと読む)
分岐ペプチド両親媒性物質、関連するエピトープ化合物およびその自己集合構造物
1つ以上のエピトープ配列に結合するためのペンダントアミノ基を提供する1つ以上の残基を組み込んだ分岐鎖状ペプチド両親媒性物質化合物、エピトープ提示を増強するためのこのような化合物および関連組成物。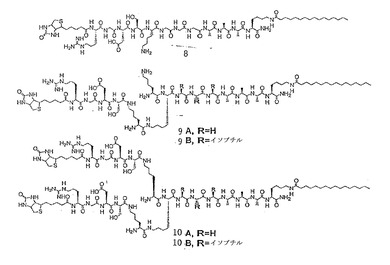
 (もっと読む)
(もっと読む)
免疫原性を低減した分子の取得方法
【課題】
【解決課題】本発明は、個体におけるペプチド、タンパク質またはタンパク質複合体の免疫原性を低減させる方法を提供する。
【解決手段】個体におけるペプチド、タンパク質またはタンパク質複合体の2アミノ酸間にインビボにおいて安定または不可逆な少なくとも1つの架橋を導入することを含み、この場合、少なくとも1つの架橋により、個体における該ペプチド、タンパク質またはタンパク質複合体の免疫原性が前記架橋を施されていない同一ペプチド、タンパク質またはタンパク質複合体に比較して低減される方法を提供する。
(もっと読む)
インターフェロンβ複合体
本発明は、高い生物活性を有するインターフェロンβとポリエチレングリコールとの複合体、及びこれを高効率で製造するための方法に関する。すなわち、本発明は、糖単位の数が5以下の少糖類及び単糖類、これらの糖アルコール、並びに炭素数2乃至6の多価アルコールから成る群より選ばれる少なくとも1種の添加剤存在下で、インターフェロンβとポリエチレングリコールとを結合させることを特徴とするインターフェロンβ複合体の製造方法、及び該方法によって製造される、インターフェロンβのアミノ酸配列の19番目、あるいは134番目のリジンに特異的にポリエチレングリコールが結合したインターフェロンβ複合体に関する。 (もっと読む)
新規のインスリン誘導体
【課題】新規のインスリン誘導体
【解決手段】本発明は、親インスリンのB鎖のN-末端アミノ酸残基のα-アミノ基又は該B鎖に存在するLys残基のε-アミノ基に結合した側鎖を有する、天然のインスリン又はそれらのアナログであるインスリン誘導体に関し、該側鎖は、下記一般式である
−W−X−Y−Z
ここで、W, X, Y 及び Z は、明細書で定義されたとおりである。
(もっと読む)
肺炎球菌表面付着因子Aタンパク質(PsaA)に関する結合メンバー
本発明は、肺炎連鎖球菌表面付着因子A(PsaA)タンパク質に特異的に結合することが可能な少なくとも1つの結合ドメインを含む結合メンバー、特に少なくとも2つの結合ドメインを有する結合メンバー、診断方法ならびに処置のための上記結合メンバーの使用、に関する。好ましい実施形態において、上記結合メンバーは、抗体(例えば、ヒト抗体、またはそのフラグメント)であり、それはまた、二重特異性抗体であり得る。上記結合メンバーは、連鎖球菌属、特に肺炎連鎖球菌に関する疾患および障害を予防および処置するための薬学的組成物での使用に適する。 (もっと読む)
タンパク質のジスルフィド結合形成およびグリコシル化の方法とそれに用いられる試薬
ジスルフィド結合を、特にタンパク質、ペプチドおよびアミノ酸において形成するための方法および試薬に関する。本発明の方法および試薬は、タンパク質、ペプチドおよびアミノ酸の制御されたグリコシル化に特に有用となる。本方法は、試薬または中間体としてチオスルフォネートまたはセレネニルスルフィドの化合物を使用する。セレネニルスルフィド基を含むタンパク質およびペプチドのあるものもまた、本発明の一部を形成する。 (もっと読む)
レラキシンスーパーファミリーペプチド類似体
レラキシンスーパーファミリータンパク質B鎖に基づくレラキシンスーパーファミリータンパク質の単量体環式ペプチド類似体およびその製造方法、ならびにそれを含む医薬組成物およびその利用方法について記載する。 (もっと読む)
皮膚の構造を改善するために美容上適用するためのトリペプチドおよびその誘導体
本発明は、一般式(I)[式中、R1は、H、−C(O)−R6、−SO2−R6または−C(O)−XR6を表し;R2およびR4は、互いに独立して、(CH2)n−NH2または(CH2)3−NHC(NH)NH2を表し;nは、1〜4に等しく;R3は、ヒドロキシルで場合により置換された、直鎖または分枝鎖C1〜C4アルキルを表し;R5およびR6は、互いに独立して、水素、場合により置換されたC1〜C24アルキル、場合により置換されたC2〜C24アルケニル、場合により置換されたフェニル、場合により置換されたフェニル−C1〜C4アルキル、または9−フルオレニルメチルを表し;Xは、酸素(−O−)または−NH−を表すか;あるいはX=OであるXR5は、α−トコフェロール、トコトリエノールまたはレチノールのエステルも表すが、同時に、R1およびR5が水素を表さず、Xが酸素を表さない]に相当する化合物、および美容上許容され得るその塩に関する。本発明は、一般式(I)の化合物の製造、および式(I)の少なくとも1種類の化合物を含有する美容活性組成物にも関する。 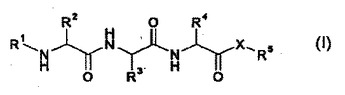 (もっと読む)
(もっと読む)
延長された生体内半減期を有するPEG−生理活性ポリペプチド同種二量体結合体及びその製造方法
【課題】 延長された生体内半減期を有するPEG−生理活性ポリペプチド同種二量体結合体及びその製造方法の提供。
【解決手段】 PEGリンカーと二分子の生理活性ポリペプチドを含み、前記二分子の生理活性ポリペプチドがPEGリンカーによって連結され、二分子の生理活性ポリペプチドの各々が一分子のPEGで修飾された、PEG−生理活性ポリペプチド同種二量体結合体は延長された血中半減期を有するポリペプチド薬物の開発に有用に用いられ得る。
(もっと読む)
ペプチドにおける標的特異的部位のノックアウト同定
本発明は、目的の標的に結合する既知親ポリペプチド内の二次構造の一次配列を決定する方法を含めた、ペプチドおよびタンパク質中の標的特異的部位の同定および決定の方法を提供する。本発明の1つの実施態様では、金属イオンに対する結合のために利用可能な窒素原子および硫黄原子を含有する基または擬態は、ペプチドまたはタンパク質の既知一次配列中の隣接残渣中で単独残渣の代わりに徐々に置換されるか、その間に挿入される。生じた配列は、金属イオンで複合され、それにより金属ペプチドを形成する。その後、生じた金属ペプチドは、目的の標的に関連した結合または官能性アッセイで使用され、そして、明らかであるか、または実質的に減少または変化した結合または官能性を生じる金属ペプチドは、このような結合または官能性に関与した一次配列を同定するために決定される。 (もっと読む)
ポリアミノ酸誘導体から成る核酸関連物質反応試薬
【課題】 核酸や核酸関連物質と相互作用してそれらの挙動や構造解析などに用いられる試薬を提供する。
【解決手段】 ポリペプチド結合を形成するアミノ基とカルボキシル基以外に側鎖に水酸基、カルボキシル基またはアミノ基から成る反応性官能基を有するアミノ酸を構成単位とし、前記アミノ酸側鎖の反応性官能基を介して、下記の式(I)で表わされるフェニルボロン酸基が結合されているポリアミノ酸誘導体から成る核酸関連物質反応試薬。式(I)中、Rは、アミノ酸側鎖の反応性官能基である水酸基、カルボキシル基またはアミノ基と反応して形成された原子団を表す。
【化1】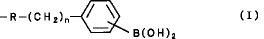 (もっと読む)
(もっと読む)
121 - 137 / 137
[ Back to top ]



