Fターム[4H045FA52]の内容
ペプチド又は蛋白質 (143,989) | 製造方法 (18,984) | 化学合成によるもの (4,727) | 化学修飾によるもの(ペプチド結合の切断、形成以外のもの) (684) | アミノ酸側鎖の修飾 (137)
Fターム[4H045FA52]に分類される特許
81 - 100 / 137
1型糖尿病の処置のための治療的ワクチン組成物
本発明は、1型糖尿病の処置および予防のための免疫原としての使用に適する修飾インスリンB鎖組成物を含む治療的ワクチン組成物に関する。 (もっと読む)
トロンビン受容体アンタゴニストとしての新規なヘテロアリールペプチド模倣物
本発明は、血栓症、再狭窄、高血圧症、心不全、不整脈、炎症、狭心症、発作、アテローム性動脈硬化症、虚血性症状、血管新生および関連障害、癌ならびに神経変性障害と関連する疾患の処置のためにトロンビン受容体アンタゴニストとして有用な新規なヘテロアリールペプチド模倣化合物に関する。本発明の置換されたヘテロアリールペプチド模倣物を含んでなる製薬学的組成物およびトロンビン受容体により媒介される症状を処置する方法もまた開示される。 (もっと読む)
ペプチドギャップ結合モジュレーター
本発明は、ギャップ結合により介される細胞間コミュニケーションを促進するジペプチドを開示する。本発明は、ギャップ結合細胞内コミュニケーション(GJIC)の障害に付随する疾患の治療における使用を含む広範な有用な用途を有する。 (もっと読む)
機能的糖ペプチドの合理的設計および合成
本発明は、少なくとも1つのアミノ酸残基にグルタミンを有する、生物学的活性を有する形態のペプチドのグルタミンが糖鎖で修飾されている、糖ペプチドを提供する。さらに本発明は、以下の工程:A)少なくとも1つのアミノ酸残基にグルタミンを含む、目的とするペプチドを提供する工程;およびB)該グルタミンに糖鎖を導入する工程、を包含する機能的糖ペプチドを調製する方法を提供する。これによって、生物学的活性を有意に増強または調節することが可能となる。 (もっと読む)
非標的部位のアミンが保護されたペプチド、その製造方法、及びこれを利用したPEGが特異的に接合されたペプチドの製造方法
本発明は、非標的部位のアミンが選択的に保護された合成ペプチド及びその製造方法とこれを利用して合成ペプチドの標的部位にPEGを特異的に接合する方法に関するものである。本発明により標的部位のアミンにPEGが特異的に結合したPEG接合ペプチドが非常に高い収率で得られる。  (もっと読む)
(もっと読む)
方法
炭水化物エステル、タンパク質エステル、タンパク質サブユニットエステル又はヒドロキシ酸エステルの1種類又は複数を生成する方法であって、リン脂質、リゾリン脂質、トリアシルグリセリド、ジグリセリド、糖脂質又はリゾ糖脂質からなる群の1種類又は複数から選択される脂質基質であるアシル供与体と、炭水化物、タンパク質、タンパク質サブユニット又はヒドロキシ酸からなる群の1種類又は複数から選択されるアシル受容体と、水とを混合して、5〜98%の水を含む高水分環境を作るステップと、脂質アシルトランスフェラーゼが以下の反応、すなわち、アルコール分解若しくはエステル転移の一方又は両方を触媒するように前記混合物を前記脂質アシルトランスフェラーゼと接触させるステップとを含む、方法。 (もっと読む)
抗感染性リポペプチド
本発明は、新規デプシペプチド化合物に関する。本発明は、これらの化合物の医薬組成物、および抗菌性化合物としてのこれらの化合物の使用方法にも関する。本発明は、これらの新規デプシペプチド化合物およびこれらの化合物の製造において用いる中間体の製造方法にも関する。 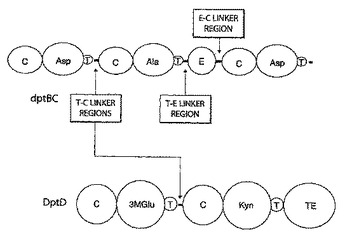 (もっと読む)
(もっと読む)
エリスロポエチン:エリスロポエチンの改造および複合糖質化
【課題】 貧血症、腎臓透析患者を治療するに有効なペプチドおよびその製造方法を提供する。
【解決手段】 一つもしくはそれ以上のグリコシル基をペプチドに付加もしくは除去すること、および/または修飾基をペプチドに付加する方法により、ペプチド分子を改造する。
(もっと読む)
ジポリマー・タンパク質コンジュゲートおよびその調製方法
本発明は、ジポリマー・タンパク質コンジュゲートおよびその調製方法に関する。さらに本発明は、そのようなジポリマー・タンパク質コンジュゲート、特にジPEG化タンパク質コンジュゲートの、疾患治療用の薬剤の製造のための使用に関する。 (もっと読む)
ポリエチレングリコール結合GLP−1化合物
本発明は、非ペグ化(unPEGylated)ペプチドと比べて、半減期が延長され、クリアランスが遅延化された生物活性ペプチドが得られる、少なくとも1個のポリエチレングリコール分子に共役結合したGLP-1化合物をまたはその誘導体提供する。これらのペグ化(PEGylated)GLP-1化合物および組成物は、糖尿病、肥満、過敏性腸症候群、ならびに血糖を低下させること、胃および/または腸運動性を抑制すること、および胃および/または腸内容排出を抑制すること、または食物摂取を抑制することが有益であるその他の健康状態の治療に有用である。 (もっと読む)
タンパク質の誘導体化及び結合のための活性化シアル酸誘導体
還元性末端及び/又は非還元性末端のシアル酸ユニットをN−ヒドロキシスクシンイミド(NHS)基に変換させて、PSAの誘導体を合成する。この誘導体を基質、例えばアミン基又はヒドラジン基を含有する基質と反応させてもよく、非架橋/架橋ポリシアル酸化化合物を形成する。基質は、例えば、治療に有用な薬物、ペプチド若しくはタンパク質、又はドラッグデリバリーシステムであってもよい。 (もっと読む)
シクロデキストリン担持微小管、その製造方法及びそれを用いたナノバイオ素子
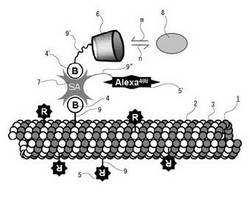
【課題】可逆的な包接能と運動機能を併せ持つ、シクロデキストリンで化学修飾された微小管及びその製造方法を提供する。また、物質の選択的回収、運搬及び徐放を行うナノバイオ素子を提供する。
【解決手段】少なくとも1つの一般式1で表わされるビオチン化シクロデキストリン、少なくとも1つのアビジン、及び少なくとも1つのビオチン化微小管を含むシクロデキストリン担持微小管。
一般式1
シクロデキストリン−Lin−ビオチン
(一般式1中、シクロデキストリンは、α、β又はγ−シクロデキストリンであり、Linは2価の連結基であり、シクロデキストリン及びLin間の結合、並びにLin及びビオチン間の結合はそれぞれ、共有結合であり、Linを介さずにシクロデキストリンとビオチンとが直接共有結合していてもよい。)
(もっと読む)
ポリエチレングリコール修飾インターフェロン組成物およびその使用方法
約30 kDの公称分子量を有する直鎖状ポリエチレングリコール(PEG)分子に結合したインターフェロンα(IFN-α)およびこれを含む組成物を提供する。本発明は、ウイルス感染症を本発明のPEG-修飾IFN-αで治療する方法をさらに提供する。 (もっと読む)
カスパーゼ活性化調節ペプチド
本発明はアポトーシス性細胞死を調節しえる小分子の構造を提供する。より具体的には、本構造はヒトα-フェトプロテイン(AFP)およびアルブミンのアポトーシス活性部位の構造に関する。この活性部位を模倣するペプチドは2つの配列Arg-Gly-AspおよびAsp-X-X-Asp(Xは任意のアミノ酸)を含む。これらの配列は広範囲の生物学的活性を生じさせるために同一の分子中に必要である。このペプチドはチトクロームc-媒介カスパーゼ活性化を阻害することによりアポトーシス経路を抑制するために使用することが出来る。従って、本ペプチドは酸化的ストレス、薬剤、サイトカイン、Fas-リガンド、α-フェトプロテインに使用することが出来、培養細胞、器官移植、免疫学的自己免疫疾患、ウイルス感染によって誘導される免疫不全症候群におけるアポトーシスの防止のために使用することが出来、化学療法および放射線療法後の細胞傷害性副作用を軽減するために使用することが出来る。 (もっと読む)
グリコシル化エンケファリン薬
二糖類によりグリコシル化されたエンケファリンペプチドは血液脳関門をとして輸送され、血流に導入された場合にモルヒネよりも優れた鎮痛効果を生じさせることが教示される。二糖類が付加してグリコシル化ペプチドは単糖または三糖類が付加した類似ペプチドよりも優れている。 (もっと読む)
インスリン誘導体
本発明は、親インスリン分子のB鎖のN-末端アミノ酸残基のα-アミノ基またはB鎖内に存在するLys残基のε-アミノ基のいずれかにアミド結合を介して結合した側鎖を有するインスリン誘導体であって、前記側鎖が、-NH2および-COOH;4〜22炭素原子を含む脂肪二酸基、少なくとも一つの遊離カルボン酸基または中性pHで負に帯電する基;および前記側鎖中の個々の成分をアミドまたはエーテル結合を介して一緒に連結させることが可能なリンカーであって遊離カルボン酸基を任意的に含むリンカーから選択された基をそれぞれ独立して含む、エチレングリコール、プロピレングリコールおよび/またはブチレングリコールの一以上の残基を含むインスリン誘導体に関する。 (もっと読む)
GLP−2化合物、製剤、及びそれらの使用
【課題】GLP−2化合物、製剤、及びそれらの使用
【解決手段】本発明は、持続的な作用プロファイルを有する新規ヒトグルカゴン様ペプチド2(GLP−2)ペプチド及びヒトグルカゴン様ペプチド-2誘導体に関し、並びに、そのようなペプチドをコードするポリヌクレオチド構築物、該ポリヌクレオチドを含み発現するベクター及び宿主細胞、薬学的組成物、使用及び治療方法に関する。  (もっと読む)
(もっと読む)
トリペプチドおよびテトラペプチドスルホン
トリペプチドおよびテトラペプチドスルホン、それを含む医薬組成物、その医薬的使用ならびにその製造。該化合物は、腫瘍細胞における化学療法剤の細胞毒性効果の増強、腫瘍細胞における選択的毒性付与、骨髄細胞におけるGM前駆体産生の亢進、骨髄分化の刺激、化学療法剤の骨髄抑制作用の緩和および骨髄における造血の調節に有用である。 (もっと読む)
トリペプチドおよびテトラペプチドチオエーテル
トリペプチドおよびテトラペプチドチオエーテル、それを含む医薬組成物、その医薬的使用ならびにその製造。該化合物は、腫瘍細胞における化学療法剤の細胞毒性効果の増強、腫瘍細胞における選択的毒性付与、骨髄細胞におけるGM前駆体産生の亢進、骨髄分化の刺激、化学療法剤の骨髄抑制作用の緩和および骨髄における造血の調節に有用である。 (もっと読む)
GEM−ジフルオロ化されたC−グリコペプチド及びその調製並びに生物学的物質の保存及び/又は凍結外科への使用
本発明は、化学式(I)を有するgem-ジフルオロ化されたC-グリコペプチド化合物に関し、ここにおいてNは1と5との間の整数であり、R4=H、AA1、AA1-AA2であり、R5=OH、AA1、AA1-AA2であり、AA1及びAA2は独立しており、非官能性側鎖を有するアミノ酸であり、R1、R2、R3は独立した基であり、それらの内の1つは化学式(II)に等しく、ここにおいてnは3と4との間の整数であり、Y、Y'は独立した基であり、ここでY、Y'=H、OR、N3、NR'R''、SR'''であり、ここでR=H、ベンジル基、トリメチルシリル基、tert-ブチルジメチルシリル基、tert-ブチルジフェニルシリル基、アセテート基であり、R'、R''=H基、アルキル基、アリル基、ベンジル基、トシレート基、C(=0)-アルキル基、C(=O)-Bn基であり、R'''=H基、アルキル基、アセテート基であり、R6は特にH基、CH3基、CH2OH基、CH2-グリコシド基、CH2-OGP基であり、ここでGPはアルキル基、ベンジル基、トリメチルシリル基、tert-ブチルジメチルシリル基、tertブチルジフェニルシリル基、アセテート基等の保護基であり、R7=OH、OGP'、NH2、N3、NHGP'、NGP'GP''であり、ここでGP'及びGP''はアルキル基、ベンジル基、トリメチルシリル基、tert-ブチルジメチルシリル基、tert-ブチルジフェニルシリル基、アセテート基等の保護基であるか否かであり、R8は水素原子H若しくは遊離型若しくは保護されたアルコール官能基である。これは特に生物学的物質の保存及び凍結外科に適用される。 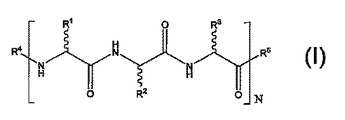 (もっと読む)
(もっと読む)
81 - 100 / 137
[ Back to top ]