Fターム[4H045GA23]の内容
ペプチド又は蛋白質 (143,989) | 分離・精製・安定化 (6,086) | 吸着によるもの (4,352) | クロマトグラフィー (4,156) | イオン交換クロマトグラフィー (616)
Fターム[4H045GA23]に分類される特許
61 - 80 / 616
成長因子タンパク質の精製方法
非免疫原性ポリマー結合体の調製のための凝集体非含有尿酸オキシダーゼ
【課題】尿酸分解活性を弱めずにウリカーゼ免疫原性を実質的に排除するポリ(アルキレングリコール)−ウリカーゼ結合体を提供する。
【解決手段】八量体より大きい凝集体を実質的に含有しない精製尿酸オキシダーゼ(ウリカーゼ)。ウリカーゼの精製方法であって、八量体より大きいウリカーゼ凝集体を分離する工程と、精製ウリカーゼからこのような凝集体を排除する工程とを包含する。及び前記分離工程が、イオン交換クロマトグラフィー、サイズ排除クロマトグラフィーおよび限外濾過からなる群から選択される。
(もっと読む)
植物培養における高マンノースタンパク質の製造
【課題】
リソソーム蓄積疾患の処置のための組成物を提供する。
【解決手段】
有効成分としての、高マンノース組み換えタンパク質を発現する植物細胞、及び医薬的に許容され得るキャリアを含む医薬組成物。
(もっと読む)
肥満および/または糖尿病を診断、モニタリング、および治療するための組成物、試薬、およびキット、ならびにその方法
【課題】肥満および/または糖尿病を診断、モニタリング、および治療するための組成物を提供する。
【解決手段】グレリン変異体2の配列を有する単離された核酸分子またはその相補物によりコードされる単離されたタンパク質、または配列GSSFLSPEHQRVQVRPPHKAPHを含むそのタンパク質フラグメントであって、グレリン変異体2とグレリン−WT(変異体)の元々の配列との間のヌクレオチドの変異を含む領域を含むグレリン変異体2の部分配列である核酸フラグメントによりコードされるアミノ酸配列であるタンパク質フラグメントからなる。
(もっと読む)
モノクローナル抗体を含む製剤の製造方法
【課題】高濃度モノクローナル抗体溶液の製造方法の提供。
【解決手段】モノクローナル抗体を含む製剤の製造方法であって、ウイルス除去工程は、モノクローナル抗体の産生時由来のウイルスと、安定化剤の産生時由来のウイルスを除去し、ウイルス除去工程のウイルス除去能力が、LRV≧4であって、ウイルス除去工程時のモノクローナル抗体の濃度が3.0〜10.0重量%の範囲であり、前記ウイルス除去工程に用いるウイルス除去膜に対する、溶液中に含まれるモノクローナル抗体の、濾過開始後0〜10分と、0〜3時間経過時の平均透過性が、いずれも1.0 ( kg / m2/ hour )以上であることを特徴とする、モノクローナル抗体を含む製剤の製造方法を提供する。
(もっと読む)
ペプチドが結合された、イノシン置換アンチセンスオリゴマー化合物および方法
【課題】治療的なオリゴマー−ペプチド結合体およびこの結合体を使用する方法の提供。
【解決手段】本願発明の治療的なオリゴマー−ペプチド結合体は、(a)実質的に荷電していないオリゴヌクレオチドアナログ化合物であって、化合物が結合することが意図される標的核酸領域において、4以上連続したシトシン塩基と相補的である塩基の列を含む塩基配列を有する、化合物、および(b)標的細胞への該化合物の取り込みを高めるのに効果的な、この化合物に結合されたアルギニンリッチペプチドを含む。この化合物中の塩基の列は、この塩基の列における連続したグアニン塩基の数を3個以下に制限するように列中に配置された少なくとも1個のイノシン塩基を含む。この結合体は、アルギニンリッチペプチドによって、化合物単独よりも大きな細胞取り込みを有し、そしてイノシンによるグアニン置換がない結合体よりも活性が実質的により大きいアンチセンス活性を有する。
(もっと読む)
8より上または5未満のpIを有するペプチドを産生するための方法
【課題】精製b型ナトリウム利尿ペプチドの産生方法
【解決手段】8より上または5未満のpIを有するペプチドを産生するための方法が記載される。ここで、このペプチドは、酸切断部位を介して融合パートナーに連結される融合タンパク質として発現される。このペプチドは、この融合パートナーから、カオトロープの非存在下で酸切断により放出される。この融合パートナーおよびその酸切断産物は、必要ならば、所望のペプチドの正味電荷とは有意に異なる正味の電荷を有して、このペプチドのイオン交換クロマトグラフィーによる単離を可能にする。
(もっと読む)
凝固因子VIIポリペプチド
【課題】新規なヒト凝固因子VIIポリペプチドを提供する。
【解決手段】TF非依存的活性が増加した因子VIIポリペプチド、即ち、野生型の因子VIIaと比較して同等かまたはより高い活性を示し、かつ組換え体の野生型ヒト因子VIIaと比較してより低い組織因子結合親和性を示す新規な凝固因子VIIポリペプチド。および前記ポリペプチドをコードするポリヌクレオチド構築物、前記ポリヌクレオチドを含みかつ発現させるベクターおよび宿主細胞、薬学的組成物、使用および治療方法。
(もっと読む)
ニューブラスチン(Neublastin)変異体
【課題】より低用量のタンパク質を使用する被験体の処置が可能であり、そして/またはより長い投与間隔が可能である変異体ニューブラスチンポリペプチドを提供すること。
【解決手段】選択されたアミノ酸残基に置換を有している変異体ニューブラスチン(Neublastin)ポリペプチドが開示される。1つ以上の選択されたアミノ酸残基での置換によっては、ヘパリンの結合が減少し、そして変異体ニューブラスチンポリペプチドの血清暴露が増大する。哺乳動物の疾患を処置し、RET受容体を活性化させるために変異体ニューブラスチンポリペプチドを使用する方法もまた開示される。
(もっと読む)
CD20抗体およびその使用
CD20は、B細胞の表面上で発現されるテトラスパニンファミリーの膜貫通タンパク質であり、末梢血ならびにリンパ系組織由来のB細胞上で見いだされる。CD20発現は、初期プレB細胞段階から形質細胞分化段階まで持続する。一方、造血幹細胞、プロB細胞、分化型形質細胞または非リンパ系組織上では見られない。正常なB細胞における発現に加えて、CD20は、非ホジキン(商標)リンパ腫(NHL)およびB細胞慢性リンパ性白血病(CLL)などのB細胞由来の悪性腫瘍で発現される。CD20発現細胞は、炎症をはじめとする他の疾患および障害に関与することが知られている。本発明は、優れた物理的および機能的特性を有する抗CD20抗体、形態および断片;免疫複合体、組成物、診断試薬、成長を阻害する方法、治療法、改善された抗体および細胞系;ならびにこれをコード化するポリヌクレオチド、ベクターおよび遺伝子構築物を含む。 (もっと読む)
単一ユニット抗体精製
本発明は、中間精製およびポリッシングの工程を少なくとも包含する、バイオリアクターにおいて生成されたタンパク質混合物からの抗体の精製のための方法に関し、当該中間精製およびポリッシング工程は、フロースルー様式での、インラインのアニオン交換クロマトグラフィー(AEX)処理および疎水性相互作用クロマトグラフィー(HIC)処理を含む。本発明はさらに、アニオン交換クロマトグラフィー部分および疎水性相互作用クロマトグラフィー部分の両方を連続的に連結して含む単一操作ユニットに関し、当該ユニットは、アニオン交換クロマトグラフィー部分の上流端において入口を含みかつ疎水性相互作用クロマトグラフィー部分の下流端において出口を含み、当該ユニットはまた、アニオン交換クロマトグラフィー部分と疎水性相互作用クロマトグラフィー部分との間にも入口を含む。 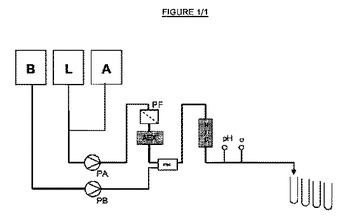 (もっと読む)
(もっと読む)
Val、LeuおよびIleのメチル基の特異的同位体標識化のための方法
本発明は、バリン、ロイシンおよびイソロイシンアミノ酸の特異的同位体標識化のための方法に関する。本発明の方法は、2−アルキル−2−ヒドロキシ−3−オキソブタン酸(2位のアルキル置換基は、エチルまたはメチルである)を使用する。本発明は、特にNMRによるタンパク質の分析に使用することができる。 (もっと読む)
薬理学的活性ペプチド/タンパク質の血清中半減期を上昇させるためのトランスサイレチンペプチド/タンパク質融合物の使用
【課題】トランスサイレチン(TTR)を生物学的活性物質との融合パートナーとして使用することにより、選択した生物学的活性物質の血清中半減期を上昇させるための手段を提供する。
【解決手段】TTR(又はTTR変異体)−生物学的活性物質融合物及びPEG−TTR(PEG−TTR変異体)−生物学的活性物質融合物の実質的に均質な製剤。製剤を製造する方法は、(a)TTRのアミノ酸配列内の特定アミノ酸位置にシステイン残基を工作して上記TTRの変異体を得る(b)上記システイン残基での上記TTR変異体にポリエチレングリコールを複合体化してPEG−TTRを得(c)上記PEG−TTRを対象ペプチドに融合してPEG−TTR−ペプチド融合物を得る(d)上記PEG−TTR−ペプチド融合物を単離する。
(もっと読む)
伸長α鎖を有するフィブリノーゲンが濃縮されたフィブリノーゲン調製物
本発明は、α伸長フィブリノーゲンが濃縮されたフィブリノーゲン調製物に関する。このような調製物を含む組成物は、典型的にはα伸長フィブリノーゲンを全く含まないか、またはごく少量含むHMW Fibに基づく調製物と比較して改善された凝固特性を示す。具体的には、α伸長フィブリノーゲンによって作成されるクロットのクロット形成時間、およびクロット強度は改善される。さらに、α伸長フィブリノーゲンのプラスミン媒介性の変性は、血漿由来のフィブリノーゲンに比較して低減される。 (もっと読む)
セリシン由来のポリペプチドおよび細胞増殖促進剤
【課題】細胞増殖や細胞機能を高めるのに有効な新たなセリシン由来成分を提供することにある。
【解決手段】本発明によるセリシン由来のポリペプチドは、繭糸から水を用いて抽出して得られたセリシンの水溶液を、陰イオン交換カラムと接触させ、非吸着画分を緩衝液Aとしてのトリス塩酸緩衝液で洗浄除去した後、陰イオン交換カラムに吸着した画分を、前記トリス塩酸緩衝液(緩衝液A)と、緩衝液Bとしての塩化ナトリウムを含むトリス塩酸緩衝液との容量比が7:3〜9:1の混合溶出液にて、溶出し回収することにより得られるものである。
(もっと読む)
大豆加工ストリームからKunitzトリプシンインヒビタータンパク質を回収する方法
加工ストリームから、少なくとも95重量%の総KTIタンパク質濃度を有するKTI生成物を回収し単離する方法が開示される。 (もっと読む)
大豆加工ストリームから単離される精製ボーマン・バークプロテアーゼインヒビタープロテイン
大豆加工ストリームから回収される精製ボーマン・バークプロテアーゼインヒビター(BBI)プロテインが開示され、ならびに大豆加工ストリームから精製BBIタンパク質を回収し単離する方法が開示される。 (もっと読む)
ボーマン・バークインヒビタープロテインを大豆加工ストリームから回収する方法
本発明は、特定される総BBIタンパク質濃度、および(例えばキモトリプシン阻害物質活性および内毒素含量をはじめとする)他のBBIの特性を有する、BBI生成物を精製する新規方法について記載する。 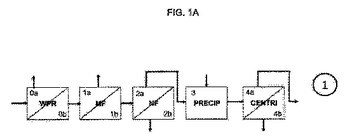 (もっと読む)
(もっと読む)
非機能性オリゴマーP2X7受容体に対する抗体
本発明は、プリン作動性受容体、前記受容体に結合する抗体およびその関連断片、前記抗体および断片の作製、および癌の検出および治療のための前記抗体および断片の使用に関する。特に、記載された抗体は生細胞により発現された非機能性P2X7受容体に特異的に結合する。 (もっと読む)
ポリペプチドを精製する方法
本発明は、イオン交換マトリックスへ結合される1つ又はそれ以上の不純物の量に対するイオン交換マトリックスへ結合される関心対象のポリペプチドの量を増加させることによって、関心対象のポリペプチドを精製するための改善された方法に関する。この効果は、イオン交換マトリックスの電荷と反対の電荷に起因してイオン交換マトリックスへも結合することによって、関心対象のポリペプチドの結合よりも多く不純物の結合を減少させる、化学化合物を方法に添加することによって達成される。 (もっと読む)
61 - 80 / 616
[ Back to top ]