Fターム[4H050BB25]の内容
第5−8族元素を含む化合物及びその製造 (19,778) | 反応媒体、分離・精製・回収用溶媒 (1,406) | 有機溶媒 (1,059) | 複素環式化合物 (128) | 異種原子として酸素のみを含有するもの (106)
Fターム[4H050BB25]に分類される特許
1 - 20 / 106
硬化性環状ホスファゼン系化合物およびこれらの製造方法
【課題】低い誘電率および誘電損失係数と高い熱安定性を有する硬化性環状ホスファゼン系化合物およびこれらの製造方法を提供する。
【解決手段】6つの置換位置を持っている環状ホスファゼン物質に2〜6つの硬化性反応基を導入し、残りの位置に様々な構造の置換基を導入する方法で硬化度や分子の分極化および自由体積などを調節することにより、低い誘電率および誘電損失係数と高い熱安定性および界面接着力を有する物質を製造することができる。
(もっと読む)
抗ウイルスヌクレオチド類似物としてのホスホネート基を有するピリミジン化合物
【課題】RNAまたはDNAウイルス(例えば、HIV、HBVまたはHSV)に対して抗ウイルス活性を有する新規化合物の提供。
【解決手段】式(I):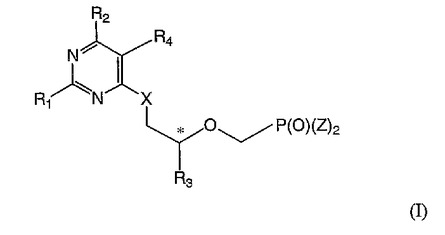
を有する新規化合物が提供されている:ここで、R1、R2、R3、R4、Z、Xおよび*は、本明細書中で定義されている。また、式(I)の化合物を使用する抗ウイルス方法およびそれを合成する方法が提供されている。他の目的は、イオン交換樹脂またはキラル媒体の調製で有用な化合物を提供することにある。さらに他の目的は、このような化合物を製造する中間体および方法を提供することにある。
(もっと読む)
ピリジルホスフィン化合物を有する金属錯体、及びアルキルメタクリレートの製造方法
【課題】従来の金属錯体を触媒とする製造方法では、メチルアセチレン等のアセチレン化合物を原料とした場合、パラジウム原子などの金属原子1モルあたり、アルキルメタクリレートの生成量が必ずしも十分満足できるものではなかった。
【解決手段】式(1)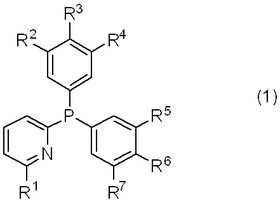
[式中、R1は直鎖アルキル基、アルコキシ基等を表す。R2、R4、R5及びR7はアルキル基等を表す。R3及びR6は水素原子、アルキル基、アルコキシ基等を表す。]
で示されるピリジルホスフィン化合物と周期表第10族に属する金属原子とを有することを特徴とする金属錯体。
(もっと読む)
リン酸エステルの合成
本発明は、リン酸エステルを製造する方法、および選択された化合物に関する。 (もっと読む)
ホスホリルクロライド及びグリコール又はポリグリコールのモノアルキルエーテルからリン酸エステルを製造する方法
ホスホリルクロライドと、少なくとも1つのモノ(アルキレングリコール)モノエーテル若しくはポリ(アルキレングリコール)モノエーテルとを、又は少なくとも1つのモノ(アルキレングリコール)モノエーテル若しくはポリ(アルキレングリコール)モノエーテルと少なくとも1つのアルキレングリコール若しくはポリアルキレングリコールの混合物とを、1モルのホスホリルクロライドにつき少なくとも3モルの、脂肪族窒素原子がない、ピリジニル化合物の存在下で反応させることにより、リン酸エステル化合物を調製する。 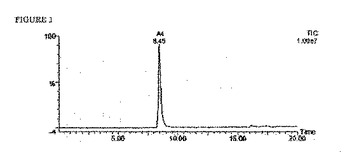 (もっと読む)
(もっと読む)
硬化性環状ホスファゼン系化合物およびこれらの製造方法
【課題】低い誘電率および誘電損失係数と高い熱安定性を有する硬化性環状ホスファゼン系化合物およびこれらの製造方法を提供する。
【解決手段】6つの置換位置を持っている環状ホスファゼン物質に2〜6つの硬化性反応基を導入し、残りの位置に様々な構造の置換基を導入する方法で硬化度や分子の分極化および自由体積などを調節することにより、低い誘電率および誘電損失係数と高い熱安定性および界面接着力を有する物質を製造することができる。
(もっと読む)
ポリカーボネート製造用エステル交換触媒、その製造方法及びポリカーボネートとその製造方法
【課題】水などの溶媒に溶解又は分散することなく、芳香族ジヒドロキシ化合物と炭酸ジエステルとの反応系にエステル交換触媒として直接導入して使用でき、透明性・色相に優れたポリカーボネート製造用エステル交換触媒の提供。
【解決手段】下記式(1)で表されるポリカーボネート製造用エステル交換触媒。
【化1】
(式(1)中、符号R1はフェノキシ基、フェニル基またはブトキシ基を表し、R2はフェニル基またはブチル基を表す。)
(もっと読む)
キラルな配位子
光学的に純粋又は光学的に非常に富化された、式(1)[ここで、R0は、C1−C12−アルキル(非置換であるか、又は1〜2個のC1−C4−アルコキシで置換されている);シクロペンチル又はシクロヘキシル(非置換であるか、又は1〜3個のC1−C4−アルキルもしくはC1−C4−アルコキシで置換されている);あるいはベンジル、フェニル又はナフチル(非置換であるか、又は1〜3個のC1−C4−アルキル、C1−C4−アルコキシ、C1−C4−フルオロアルキルもしくはC1−C4−フルオロアルコキシ、F又はClで置換されている)であるか、あるいは、R0は、−CR5R6OH又は−CR5R6OSi(C1−C8−アルキル)3(ここで、R5及びR6は、H、非置換C1−C12アルキル、置換C1−C12アルキル、非置換C4−C8シクロアルキル、置換C4−C8シクロアルキル、非置換アリール、置換アリールからなる群より独立して選択されるか、又はR5及びR6は、非置換5〜6員脂肪族炭素環又は置換5〜6員脂肪族炭素環を形成することができる)であり、各々R1及びR’1は、独立して、水素であるか、又はR0の意味を有し、R1、R’1及びR0は、同じであるか異なっていることができ、R2及びR3は、独立して、C−結合炭化水素基又はヘテロ炭化水素基であり、そして各々両方のR4は、C1−C6−アルキル、シクロペンチル、シクロヘキシル、フェニル、メチルフェニル、メチルベンジル又はベンジルであるか、あるいは両方のR4は一緒になって脂肪族C4−C6炭素環を形成する]のキラルな化合物。これらの配位子の金属錯体は、不斉付加反応、特に水素化のための、均一系触媒である。 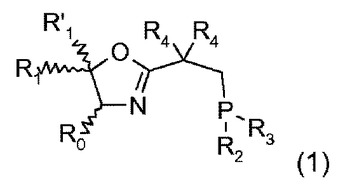 (もっと読む)
(もっと読む)
ジフルオロビス(オキサラト)リン酸リチウム溶液の製造方法
【課題】 本発明の目的は、非水電解液電池の性能向上に有効な添加剤となりへ、塩素化合物や遊離酸が少ないジフルオロビス(オキサラト)リン酸リチウム溶液を提供することである。
【解決手段】 非水溶媒中にヘキサフルオロリン酸リチウムとシュウ酸を1:1.90〜1:2.10のモル比の範囲で混合し、さらにこれに四塩化ケイ素をヘキサフルオロリン酸リチウムに対するモル比が1:0.95〜1:1.10の範囲で添加して反応させることを特徴とするジフルオロビス(オキサラト)リン酸リチウム溶液の製造方法を提供する。
(もっと読む)
ジアリールピリジルホスフィン化合物の製造方法
【課題】含硫黄官能基を有するホスフィン化合物を提供する。
【解決手段】下記の工程を含むジアリールピリジルホスフィン化合物の製造方法。A)ハロピリジン化合物を非プロトン性有機溶剤中で金属試薬と反応させて有機金属化合物を得る工程B)工程A)の反応混合物をハロゲン化ジアリールホスフィンと反応させ、ジアリールピリジルホスフィン化合物を含む反応混合物を得る工程C)工程B)の反応混合物を分離工程に供して粗ジアリールピリジルホスフィン化合物および非プロトン性有機溶剤を分離回収する工程D)工程C)の粗ジアリールピリジルホスフィン化合物に精製操作を施し、ジアリールピリジルホスフィン化合物を得る工程E)ハロゲン化ジアリールホスフィンを工程D)から回収する工程、およびF)工程C)で回収した非プロトン性有機溶剤及び/又は工程E)で回収したハロゲン化ジアリールホスフィンを工程A)又は工程B)へリサイクルする工程。
(もっと読む)
新規ホスフィンボラン化合物及びその製造方法並びに水素−ホスフィンボラン化合物の製造方法
【課題】光学活性ホスフィン配位子の製造に有用で、対掌体のいずれをも容易に製造可能な光学活性ホスフィンボラン化合物及びその製造方法を提供すること。
【解決手段】下記一般式(P−1)で表されるホスフィンボラン化合物。下記一般式(P−2)で表される水素−ホスフィンボラン化合物と下記一般式(3)で表される光学活性イソシアネート化合物とをカップリング反応に付す上記ホスフィンボラン化合物の製造方法。下記式中、R1及びR2は、それぞれ水素原子、炭化水素又は置換炭化水素基を示し、それらが存在することによりリン原子に不斉が生じるように選択してもよく又は不斉が生じないように選択してもよく、R3は不斉炭化水素基又は不斉炭化水素基を示す。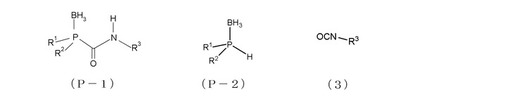 (もっと読む)
(もっと読む)
ビニレン類/ニトリル類を用いたモノカルボキシ官能化ジアルキルホスフィン酸、−エステル及び−塩の製造方法及びそれらの使用
本発明は、ビニレン類/ニトリル類を用いたモノカルボキシ官能化ジアルキルホスフィン酸、−エステル及び−塩の製造方法であって、
a)ホスフィン酸源(I)を触媒Aの存在下にオレフィン(IV)と反応させてアルキル亜ホスホン酸、それの塩またはエステル(II)とし、
b)こうして生じたアルキル亜ホスホン酸、それの塩またはエステル(II)を触媒Bの存在下に式(V)のアセチレン系化合物と反応させて、単官能化ジアルキルホスフィン酸誘導体(VI)とし、及び
c)こうして生じた単官能化ジアルキルホスフィン酸誘導体(VI)を触媒Cの存在下にシアン化水素源と反応させて、単官能化ジアルキルホスフィン酸誘導体(VII)とし、及び
d)こうして生じた単官能化ジアルキルホスフィン酸誘導体(VII)を触媒Dの存在下に反応させて、次式
【化1】
のモノカルボキシ官能化ジアルキルホスフィン酸誘導体(III)とし、ここで
R1、R2、R3、R4、R5、R6は同一かまたは異なりそして互いに独立して、中でも、H、C1−C18−アルキル、C6−C18−アリール、C6−C18−アラルキル、C6−C18−アルキルアリールを意味し、そしてX及びYは同一かまたは異なりそして互いに独立してH、C1−C18−アルキル、C6−C18−アリール、C6−C18−アラルキル、C6−C18−アルキルアリール、Mg、Ca、Al、Sb、Sn、Ge、Ti、Fe、Zr、Zn、Ce、Bi、Sr、Mn、Cu、Ni、Li、Na、K及び/またはプロトン化された窒素塩基を表し、触媒A、B及びCは、遷移金属、及び/または遷移金属化合物、及び/または遷移金属及び/または遷移金属化合物と少なくとも一つの配位子から構成される触媒系であり、そして触媒Dは酸または塩基である、ことを特徴とする上記方法に関するものである。  (もっと読む)
(もっと読む)
含リン化合物とその製造方法
【課題】立体障害のより小さい含リン化合物とその製造方法の提供。
【解決手段】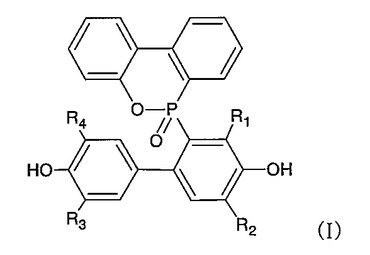
式中、R1、R2、R3とR4は、それぞれ独立して水素原子、ハロゲン原子、C1〜C8アルキル基、ハロゲン化アルキル基、又はアルコキシル基を示す。該含リン化合物は4,4'−ジヒドロキシ−ビフェノール基とリン原子との結合を利用して、ヒドロキシル基に対する含リンヘテロシクロ化合物分子の立体障害を防止することが可能となったので、後続する反応の反応性を向上させることができる。
(もっと読む)
ルテニウム−インデニリデンカルベン触媒の製造方法
本発明は(L)(L’)X2Ru(II)(アリール−インデニリデン)型のルテニウムインデニリデンカルベン触媒の製造方法に関する。本方法は、前駆体化合物Ru(PPh3)nX2(n=3−4)とプロパルギルアルコール誘導体とを、環状ジエーテル溶剤、例えば、1,4−ジオキサン中で80〜130℃の範囲の温度で且つ1〜60分の反応時間で反応させる工程を含む。場合により、追加の中性の電子供与配位子、例えば、PCy3、ホスバン配位子又はNHC配位子を、配位子交換のために反応混合物に添加する。本方法は、精製のための析出工程を含み、その後、生成物が単離される。ルテニウム−インデニリデンカルベン触媒は高純度で得られ、メタセシス反応(RCM、ROMP及びCM)のための触媒として使用され、且つ改質されたルテニウムカルベン触媒の合成のための前駆体として使用される。 (もっと読む)
アデホビルジピボキシルの改善された製造方法
本発明は、化学式1のアデホビルジピボキシルの改善された製造方法に関し、本発明による製造方法は、反応溶媒としてジメチルスルホキシドを使用することを特徴とし、当該ジメチルスルホキシドとトリエチルアミンの溶媒下で化学式2のアデホビルをクロロメチルピバレートと30℃〜50℃で反応させて、化学式1のアデホビルジピボキシルを製造する工程を含む。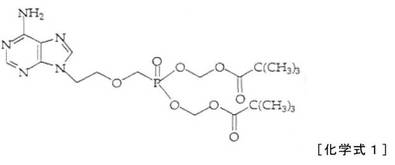
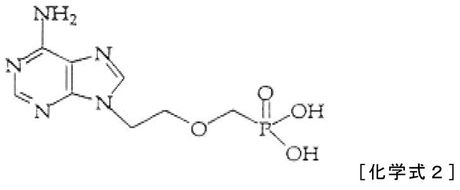
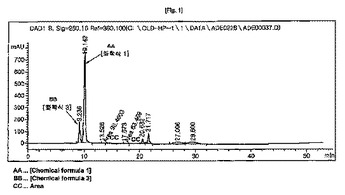 (もっと読む)
(もっと読む)
反応性基含有環状ホスファゼン化合物およびその製造方法
【課題】樹脂成形体の機械的特性を損なわずにその難燃性を効果的に高めることができ、しかも樹脂成形体の高温信頼性および誘電特性を損ないにくいホスファゼン化合物を実現する。
【解決手段】下記の式で表される反応性基含有環状ホスファゼン化合物。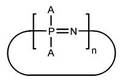
nは3〜15の整数を示す。Aの一例は、下記の式で示されるアクリロイルオキシ基置換フェニル基およびメタクリロイルオキシ基置換フェニル基からなる群から選ばれる基である。式(2)中、E1〜E5は、それぞれ独立して、少なくとも一つはアクリロイルオキシ基またはメタクリロイルオキシ基であり、かつ、少なくとも一つは炭素数1〜6のアルキル基、アルケニル基およびアリール基から選ばれる少なくとも一種の基であり、残りは水素原子を示す。)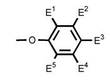
(もっと読む)
ジベンズ[c,e][1,2]−オキサホスホリン誘導体の製造方法、アミノジベンズ[c,e][1,2]−オキサホスホリン、及びその使用
【課題】リン原子上において窒素化合物で置換されている(6H)−ジベンズ[c,e][1,2]−オキサホスホリン誘導体の簡単で経済的な製造法、およびそれ自体の提供。
【解決手段】商業的に入手できるが比較的不活性な6H−ジベンズ[c,e][1,2]−オキサホスホリン−6−オキシド(II)とアミン(R4-NH2)とを反応させ、式(Iω)の(6H)−ジベンズ[c,e][1,2]−オキサホスホリン誘導体を合成する。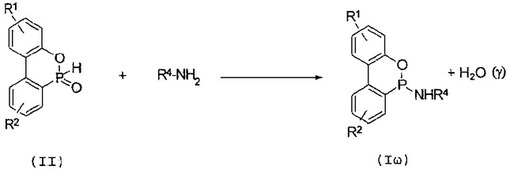
(式中、R1、R2は、同一か又は異なり、水素、又はアルキル基など、R4はアルキル基などを示す。)
(もっと読む)
ヒドロキシ基含有環状ホスファゼン化合物およびその製造方法
【課題】樹脂成形体の難燃性を高めることができ、しかも樹脂成形体の高温での機械的特性および信頼性を損ないにくいヒドロキシ基含有ホスファゼン化合物の提供。
【解決手段】下記式(1)で表されるヒドロキシ基含有環状ホスファゼン化合物。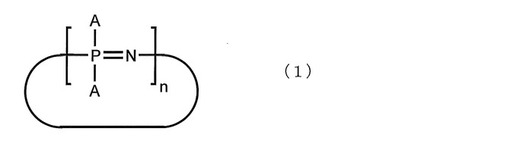
式(1)中、nは3〜8の整数を示し、Aは下記のA1基、A2基およびA3基からなる群から選ばれた基を示しかつ2n個のAのうちの少なくとも一つがA3基である。A1基:炭素数1〜6のアルキル基等で置換されていてもよい炭素数が1〜8のアルコキシ基。A2基:炭素数1〜6のアルキル基等で置換されていてもよい炭素数6〜20のアリールオキシ基。A3基:2−メチル−4−ヒドロキシ−フェニルオキシ基、3−メチル−4−ヒドロキシ−フェニルオキシ基および4−ヒドロキシ−3,5−ジメチル−フェニルオキシ基からなる群から選ばれる少なくとも一つの基。
(もっと読む)
リン化合物の製造方法及びアリル化合物誘導体の製造方法
【課題】 本発明の課題は、リン化合物の一種であるホスホロアミダイト化合物を、より簡便に且つ安全に製造でき、且つ工業的に有利なホスホロアミダイト化合物の合成法を提供することである。
【解決手段】 有機溶媒中で、ハロゲン化リン化合物、フェノール類、及び塩基を混合した後、得られた混合溶液に、アミン類を添加して、一般式(I)で表されるリン化合物を生成し、一般式(I)で表されるリン化合物を含有する反応液から、貧溶媒を用いて、一般式(I)で表されるリン化合物を取り出すリン化合物の製造方法。
(もっと読む)
糖ボラノホスフェート化合物及びその用途
【課題】効率的な糖1-リン酸化合物の製造方法を提供する。
【解決手段】下記の一般式(I):
(R1及びR2はアルキル基を示し;R〜O-は糖化合物残基を示す)で表される糖1-ボラノホスフェート化合物の製造方法であって、R〜OHで表される糖化合物と下記の一般式(II):
(X+は一価の陽イオンを示す)で表される化合物とを反応させる工程を含む方法。
(もっと読む)
1 - 20 / 106
[ Back to top ]