Fターム[2G041LA08]の内容
その他の電気的手段による材料の調査、分析 (22,023) | 信号処理 (1,307) | 定量測定 (529)
Fターム[2G041LA08]の下位に属するFターム
イオン強度軸補正 (39)
Fターム[2G041LA08]に分類される特許
101 - 120 / 490
小分子の同時的な定量および同定のための質量タグ試薬
質量タグを分析物にコンジュゲートし、タンデムマススペクトロメトリーフラグメンテーション(MS−MSまたはMS2)後に、質量タグのシグナチャーイオンが分析物に付着したまま残る、分子の同定方法および定量方法を提供する。シグナチャーイオンを失うのではなく、構造物の質量バランス部分を、タンデムマススペクトロメトリーフラグメンテーションの下で、電荷中性基として失わせることができる。このシグナチャーイオンを定量に用いることができ、さらなるフラグメンテーションによって、分析物の特徴を示し、かつ分析物の同定に有用なイオンシグナルを提供することもできる。いくつかの実施形態では、3回目のマススペクトロメトリーフラグメンテーション(MS3)から生成されたイオンシグナルを、例えば、検索表、ライブラリー、またはデータベースからの既知のマススペクトルと比較して、分析物の一義的な同定を提供することができる。 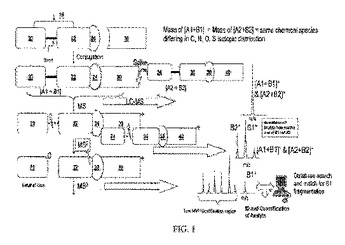 (もっと読む)
(もっと読む)
ビタミンD3、ビタミンD2、およびこれらの代謝体の定量分析
ビタミンD2、ビタミンD3、ならびにビタミンD2およびビタミンD3のモノヒドロキシおよびジヒドロキシ代謝体の定量は、分析物をマススペクトロメトリー(MS)タグ化試薬で標識し、かつ標識分析物のLC−MSMS分析を行なうことを含むことができる。標識分析物は、標識標準を含むことができ、かつ逆相カラムでの異なる保持時間、および異なる質量を有することができる。高エネルギー衝突下で、レポーター基を発生させることができる。各々のレポーター基について検出される強度またはピーク面積を定量に用いることができる。いくつかの実施形態では、ジエノフィルを含有する標識ディールス・アルダー試薬である1段階タグ化試薬を用いる。 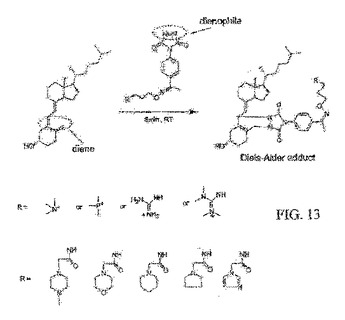 (もっと読む)
(もっと読む)
インスリン様増殖因子1受容体(IGF−1R)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にIGF−1Rタンパク質を定量するための特に好都合な、インスリン様増殖因子1受容体(IGF−1R)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、IGF−1Rタンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。IGF−1Rペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
インスリン受容体基質1(IRS1)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にIRS1タンパク質を定量するための特に好都合な、インスリン受容体基質1(IRS1)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、IRS1タンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。IRS1ペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
酸性およびシステインに富む分泌(SPARC)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にSPARCタンパク質を定量するための特に好都合な、酸性およびシステインに富む分泌(SPARC)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、SPARCタンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。SPARCペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
上皮成長因子受容体(EGFREGFR)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にEGFRタンパク質を定量するための特に好都合な、上皮成長因子受容体(EGFR)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、EGFRタンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。EGFRペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
前立腺癌の代謝学的プロファイリング
本発明は、癌マーカーに関するものである。特に本発明は、癌(例えば、前立腺癌または乳癌)において特異的に存在する代謝物および代謝物パネルを提供する。 (もっと読む)
プラズマローゲンの分析方法
【課題】本発明の目的は、プラズマローゲン分析における内部標準として用いることのできる新規化合物、及び前記化合物を用いる精確なプラズマローゲン分析方法を提供することである。
【解決手段】前記課題は、一般式(1)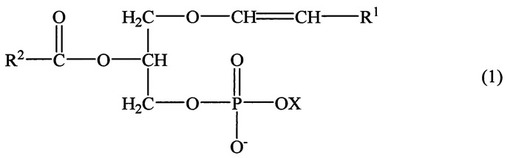
(式中、R1は、炭素数7、9、11、13、15、17、19、又は21のアルキル基であり、R2は、炭素数8〜21のアルキル基又はアルケニル基であり、Xは、CH2CH2N(CH3)3、又はCH2CH2NH2である)で表される化合物を、内部標準化合物として用いるプラズマローゲン分析方法によって解決することができる。
(もっと読む)
妊娠高血圧腎症の危険性の検出
例えば子癇、軽度妊娠高血圧腎症、慢性高血圧症、EPH妊娠中毒、妊娠性高血圧症、加重型妊娠高血圧腎症、ヘルプ症候群または腎症などを含む、妊婦の高血圧障害の危険性を早期に予測する方法。 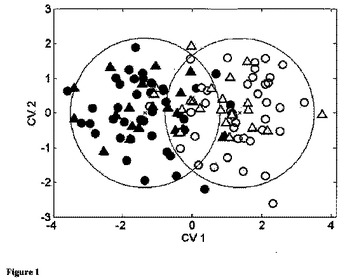 (もっと読む)
(もっと読む)
触媒生成方法およびシステム
触媒を生成する方法であって、この方法は、触媒粒子と溶媒とを混合し、それによって混合物を形成することと、混合物に対して粒度分布分析を行い、それによって粒度分布プロファイルを決定することと、粒度分布プロファイルが閾値未満である場合には、混合物の混合を反復することと、粒度分布プロファイルが閾値以上である場合には、混合物を遠心分離し、それによって上清と沈殿物とを形成することであって、上清は、触媒粒子と溶媒とを含む分散を含む、ことと、混合物をデカントし、上清を沈殿物から分離することと、分離された上清の粒子含有率を決定することと、触媒支持体の1つ以上の特性に基づいて、触媒支持体に適用される分散の体積を決定することと、分散の体積を触媒支持体に適用することによって、分散中の触媒粒子で触媒支持体を含浸することとを包含する。 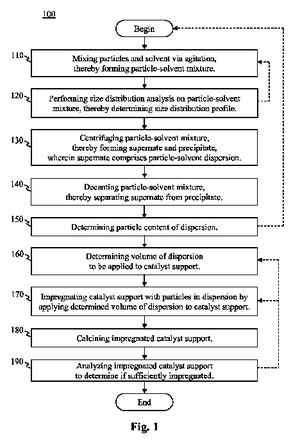 (もっと読む)
(もっと読む)
複合試料中のステロイド化合物の質量分析
本発明は、質量分析によるステロイド化合物の定量的測定に関する。特定の態様において、本発明は、質量分析による複数の試料からのステロイド化合物の定量的測定の方法に関する。 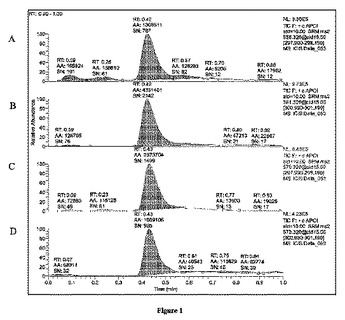 (もっと読む)
(もっと読む)
非誘導体化非代謝化ビタミンDの質量分析法による決定
本発明は、非代謝化ビタミンDの検出に関する。特定の態様では、本発明は、非誘導体化非代謝化ビタミンDを質量分析法により検出するための方法に関する。 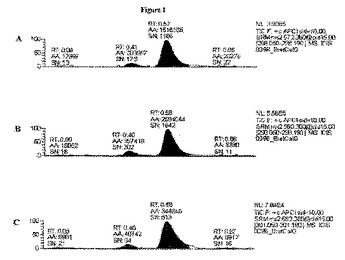 (もっと読む)
(もっと読む)
ペプチド末端の同定方法
【課題】蛋白質のアミノ末端およびカルボキシ末端を、網羅的かつ簡便に決定する方法の提供。
【解決手段】(a)対象ポリペプチド中の1種のアミノ酸残基のアミノ末端側又はカルボキシ末端側の一方で切断したペプチド断片群の取得工程;(b)対象ポリペプチドと同一のポリペプチド中に含まれるアミノ酸残基と同一のアミノ酸残基について、工程(a)で切断した末端と逆側の末端で切断したペプチド断片群の取得工程;(c)工程(a、b)で得た二つのペプチド断片群の質量分析スペクトルの取得工程;(d)工程(c)の質量分析スペクトルから、質量差のあるピークの組を抽出する工程;(e)工程(d)で抽出されたピークの組について、各ピークの質量差、又は、各ピークのフラグメントの質量分析結果から、ピークの組が、対象ポリペプチドのアミノ末端、又は、カルボキシ末端を含むポリペプチドであると判断する工程;により、ポリペプチド末端を同定する。
(もっと読む)
界面活性剤分析法
【課題】界面活性剤中の無機物イオン、とりわけ有機スルホン酸イオンの硫酸イオンの定量分析を高感度および高精度で行う手法を提供する。
【解決手段】有機スルホン酸塩などの界面活性剤中の無機物イオン、例えば、硫酸イオンの定量分析において、ESI(Electrospray Ionization)-MS(Mass Spectrometry)分析法を用い、メタノール・水混合溶液に試料を溶解し、内部標準添加法による所定濃度調製により無機物イオンを高感度および高精度分析法が可能となる。
(もっと読む)
フルオラス化シアル酸誘導体およびその分析方法
【課題】LC-MS/MS法で検出するフルオラス化シアル酸誘導体の検出方法を提供する。
【解決手段】一般式[I]: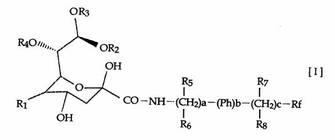
{式中、R1は、グリコリル基など、R2、R3及びR4は、水素原子など、aは1〜3の整数、bは0または1の整数、cは1〜3の整数、Rfは一般式[II]:
(式中、R9およびR10は、水素原子またはフッ素原子、dは4〜10の整数を意味する。)で表されるフルオロアルキル基を意味する。}で表されるフルオラス化シアル酸誘導体は、LC-MS/MS法で検出することができる。
(もっと読む)
液体クロマトグラフ質量分析装置
【課題】
本願発明の課題は、高速液体クロマトグラフ質量分析装置のイオン化部におけるコロナニードルが汚染された場合に、コロナニードルを補修する適切なタイミングを判断しユーザに通知することを可能にすると共に、ユーザが安全に補修作業を行うことを可能にする。
【解決手段】
補修タイミング判断部6は、クロマトグラム作成部5で作成されたクロマトグラムの形状に基づいて、コロナニードル8の汚染状態を判断する。補修タイミング判断部6が、コロナニードル8の補修が必要と判断した場合、その旨を通知部7と安全機構42に伝える。通知部7は、ユーザにコロナニードル8の補修が必要になった旨を伝える。安全機構42は、高圧電源41を制御し、コロナニードル8への印加電圧を低減させる。
(もっと読む)
心疾患マーカーとしての尿中トリアオシルセラミド(GB3)
本発明は、非ファブリー病の心疾患患者の尿中グロボトリアオシルセラミド(Gb3)レベルを判定する方法について記載する。Gb3レベルの判定により、心臓疾患のリスクを判定するスクリーニング方法を提供し、薬学的シャペロン又は他の薬剤を使用してGb3レベルを低減させることによって、心疾患の管理又は心疾患のリスクの軽減に対する代替的な治療の選択肢を提供することができるかもしれない。 (もっと読む)
胆道がんの新規バイオマーカー
【課題】胆道がんと関連する新規バイオマーカーの検出に、質量分析を使用する方法を提供する。
【解決手段】被験体における胆道がんと関連する異常量のバイオマーカーを検出する方法であって、a)質量分析を使用して該被験体由来の生物学的試料における約4204m/zのm/z値を有するプロトロンビンの断片の量を定量化すること、及びb)(a)において取得した定量化した値を閾値と比較することを含み、ここで該定量化した値が該閾値を上回る場合異常量の該バイオマーカーが該生物学的試料中に存在する、方法。
(もっと読む)
カテナ:漿液性癌幹細胞
本発明は、漿液性癌幹細胞(CSC)のクローン的に純粋な集団、CSCを製造及び培養する方法、並びにその使用に関する。CSCは、ヒアルロン酸とプロテオグリカンとのグリコカリックス被覆を有するカテナ(浮遊性細胞鎖)を形成する。この発見が、グリコカリックス形成の除去又は抑制を標的とすることにより漿液性癌及び卵巣癌を治療する方法であって、グリコカリックス阻害剤との併用による化学療法を用いた併用療法を含む上記方法の開発に至った。また、本発明は、これらのCSC、並びにその他漿液性癌細胞に対する効果的な化合物を同定するための薬物スクリーニングアッセイを提供する。カテナ遺伝子特性、タンパク質、及び表面抗原を使用する方法が、漿液性癌幹細胞の存在について患者試料を監視するために提供される。 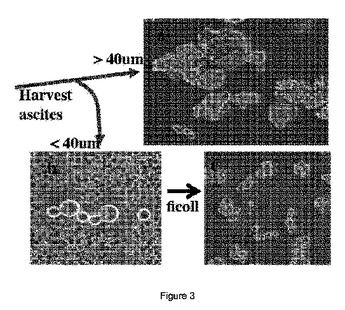 (もっと読む)
(もっと読む)
液体クロマトグラフィーを用いたビタミンUの精製および分析法
【課題】試料中に含まれるVUを精製および分析する方法の提供。
【解決手段】植物由来の試料中に含まれるビタミンU(VU)を液体クロマトグラフィーにより精製する方法であって、該液体クロマトグラフィーが親水性相互作用クロマトグラフィー用カラムを用いることを特徴とする。該親水性相互作用クロマトグラフィー用カラムが、エチレン架橋型親水性相互作用クロマトグラフィー用カラムであって、好ましい該親水性相互作用クロマトグラフィー用カラムは、XBridgeTMHILICカラムである。
(もっと読む)
101 - 120 / 490
[ Back to top ]



