Fターム[4B063QQ27]の内容
酵素、微生物を含む測定、試験 (178,766) | 検体,検出物 (39,509) | 酵素 (3,244) | 転移酵素 (880) | リン酸転移酵素(←キナーゼ) (617)
Fターム[4B063QQ27]の下位に属するFターム
DNA,RNAポリメラーゼ (125)
Fターム[4B063QQ27]に分類される特許
281 - 300 / 492
悪性腫瘍の性質の判定方法
【課題】 悪性腫瘍患者から採取した腫瘍細胞で発現している分子の分析結果に基づいて悪性腫瘍の性質を精度良く判定することのできる方法を提供すること。
【解決手段】 悪性腫瘍患者から採取した腫瘍細胞の第一のサイクリン依存性キナーゼ(第一CDK)の活性値及び発現量から得られる第一パラメータと、第二のサイクリン依存性キナーゼ(第二CDK)の活性値及び発現量から得られる第二パラメータとに基づいて得られる第三パラメータを、第一の閾値と比較する第一比較工程と、腫瘍細胞の増殖因子受容体の発現量から得られる第四パラメータを、第二の閾値と比較する第二比較工程と、第一比較結果及び第二比較結果に基づいて悪性腫瘍の性質を判定する工程と、を含む悪性腫瘍の性質の判定方法を提供する。
(もっと読む)
生体分子間の細胞内相互作用の検出方法
本発明は、蛍光ドナー/アクセプター対の2つのメンバー間の時分割蛍光エネルギー移動効果による、生物学的又は薬理学的刺激に応答して、生細胞における生体分子間の細胞内相互作用を検出する定量的な非顕微鏡的方法に関する。本発明は、分子のハイ-スループットスクリーニング及び細胞内シグナル伝達経路の検出に有用である。  (もっと読む)
(もっと読む)
クレアチンキナーゼ活性測定用試薬
【課題】CK(クレアチンキナーゼ)は、二つのサブユニットからなる二量体のリン酸化酵素であり、二種類のサブユニットの組み合せによって三種類のアイソザイムが存在する。心筋梗塞や筋ジストロフィーなどの疾患によって疾患の原因部位に存在するCKアイソザイムが血液中に逸脱するため、臨床検査において血清や血漿などの試料に含まれるCKの活性値は疾患を診断する際の重要な指標となる試薬溶液中のCK活性化剤の劣化を抑えることのできる物質を含有するCK活性測定用試薬を提供する。
【解決手段】アミノメタンスルホン酸と、CK活性化剤とを含有するCK活性測定用試薬を提供する。
(もっと読む)
血管透過性の阻害のための方法および組成物
本発明は、血管透過性を調節するための方法および組成物に関する。本発明は、血管透過性を上昇させることに関与するタンパク質およびシグナル伝達経路をブロックするための方法および組成物に関する。本発明は、PAKが血管外漏出を誘導するMLCKリン酸化を活性化する機序ならびにこの経路を調節するための組成物および方法を包含する。本発明は、血管透過性を調節する、特に血管透過性を阻害するための組成物および方法を対象とする。特に、本発明は、血管透過性の引き金を引くために重要なタンパク質の相互作用をブロックすることによって血管透過性を調節する方法を対象とする。 (もっと読む)
一般的キナーゼアッセイ法
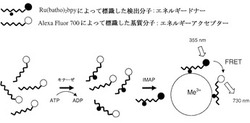
【課題】エネルギードナーとエネルギーアクセプターの間のエネルギー転移測定による、キナーゼまたはホスファターゼ活性を決定するためのより効率的な方法の提供。
【解決手段】三パートシステムに基づいて、キナーゼまたはホスファターゼ活性を決定する。リン酸化ペプチドに結合することができる結合パートナー(ビーズ上の金属イオン)、検出分子、および基質ペプチドを接触させる段階を含み、活性の測定は、検出分子および基質分子上に存在するエネルギードナー(Ru−発光団)ならびにエネルギーアクセプター(蛍光体)間のエネルギー転移を測定することによって達成される。
(もっと読む)
抗がん剤治療の有効性予測方法
【課題】 患者がためらうことなく抗がん剤治療に踏み切れるように、特定の抗がん剤治療が有効であることを高確率で予測できる抗がん剤治療の有効性予測方法を提供する。
【解決手段】 抗がん剤を少なくとも一度投与した生体から採取した腫瘍細胞のサイクリン依存性キナーゼ(第一CDK)の活性値、発現量、及び活性値と発現量との比からなる群より選択される少なくとも1つの第1パラメータと、該第1パラメータに対応する閾値とを比較する工程(第1比較工程);及び得られた比較結果(第1比較結果)に基づいて、前記生体に対する前記抗がん剤治療の有効性を予測する工程を含む。さらに第一CDKとは異なる第二CDK又はCDKインヒビターに係る第2パラメータと、該第2パラメータに対応する閾値とを比較し(第2比較工程)、第2比較結果に基づいて抗癌剤治療の有効性を予測してもよい。
(もっと読む)
グルコース輸送関連遺伝子、ポリペプチド、およびそれらの使用方法
グルコース輸送を調節するための方法および組成物を本明細書において提供する。 (もっと読む)
クレアチンキナーゼ活性測定用試薬
【課題】 試薬溶液中のSH化合物の劣化を防ぎ、且つ試薬自体の吸光度の上昇を抑えることのできるキレート剤を含有するCK活性測定用試薬を提供すること。
【解決手段】 シクロヘキシルジアミン四酢酸と、SH基を有する化合物とを含有するCK活性測定用試薬。シクロヘキシルジアミン四酢酸、グルコース−6−リン酸脱水素酵素、NAD(P)、ヘキソキナーゼ又はグルコキナーゼ、ADPを含有する第一試薬とクレアチンリン酸を含む第二試薬とからなるクレアチンキナーゼ活性測定用試薬キット。
(もっと読む)
ペプチドアレイ
【課題】ペプチドアレイを用いる測定系において、生体分子の非特異的な影響を受けることなく、結合シグナルを増幅させることにある。特に表面プラズモン(SPR)測定に用いてプロテインキナーゼによるリン酸化を検出する際に、信頼性の高いデータを得ることのできるペプチドアレイを得ることにある。
【解決手段】酵素反応の基質となるペプチドが基板上に固定化されてなるペプチドアレイであって、基板に固定化される部位と基質となるペプチドとの間に親水性化合物、好ましくはポリエチレングリコール(PEG)からなるスペーサー配列が挿入されることを特徴とする、特にSPRによるプロテインキナーゼによるリン酸化の検出に有用なペプチドアレイ。
(もっと読む)
チロシンキナーゼリン酸化の測定方法
キナーゼ阻害剤のキナーゼ特異性プロファイリングのための、キナーゼ阻害剤の存在下での前記キナーゼ阻害剤の非存在下と比較した1種または複数のチロシンキナーゼの自己リン酸化の測定のための方法、キットおよび組成物。  (もっと読む)
(もっと読む)
タンパク質相互作用と、抗がん剤、並びに抗がん剤のスクリーニング方法
【課題】DHPSの制御メカニズム及びん発症メカニズムの未解明だった部分を明らかにしすると共に、新規な抗がん剤を提供する。
【解決手段】ERKとDHPSとが相互作用すること、及び、ERKのリン酸化により、前記相互作用が抑制されることを新規に見出した。これらの事項から、(1)ERKがDHPSと相互作用し、DHPSの立体構造中に存在する酵素活性部位と球状構造との相互作用状態を保持することにより、DHPSの酵素活性(IF5Aのハイプシン化)を抑制する。(2)ERKがリン酸化された場合、ERKとDHPSとの相互作用が抑制され、DHPSの酵素活性部位と球状構造との相互作用状態が保持されないため、DHPSが酵素活性化し、IF5Aをハイプシン化するような作用メカニズムの存在が強く示唆された。DHPSの酵素活性部位と球状構造との相互作用状態を保持又は固定化する物質は抗がん剤として有用な可能性がある。
(もっと読む)
変異体SRCキナーゼポリペプチドを発現する個体の同定および治療方法
本明細書に記載する発明は、変異体SRCキナーゼタンパク質、およびそのような変異体SRCキナーゼタンパク質を発現する細胞が関連する疾患、例えば、癌の管理に有用な診断および治療法および組成物に関する。  (もっと読む)
(もっと読む)
抗がん剤治療の有効性予測方法
【課題】 患者がためらうことなく抗がん剤治療に踏み切れるように、特定の抗がん剤治療が有効であることを高確率で予測できる抗がん剤治療の有効性予測方法を提供する。
【解決手段】 患者から採取した腫瘍細胞のサイクリン依存性キナーゼの活性値、発現量、及び活性値と発現量の比からなる群より選択される少なくとも1つのパラメータと、選択されたパラメータに対応する閾値とを比較する工程;及び前記比較工程の結果に基づいて、前記患者の抗がん剤治療の有効性を予測する工程を含む方法である。複数のCDKについて、各パラメータと該当する閾値と比較し、それらの比較結果の組み合わせによって予測してもよい。閾値は、所定のがんに対して所定の抗がん剤が投与された抗がん剤治療結果と相関のあるパラメータについて、抗がん剤治療結果に基づいて設定されることが好ましい。
(もっと読む)
グルコース−6−リン酸脱水素酵素含有試薬及びグルコース−6−リン酸脱水素酵素安定化方法
【課題】 従来知られているG6PDHの安定化剤よりG6PDHの保存安定性を向上させることのできる安定化剤を含むG6PDH含有試薬を提供すること。
【解決手段】 グルコース−6−リン酸脱水素酵素(G6PDH)と、一般式(I)
【化1】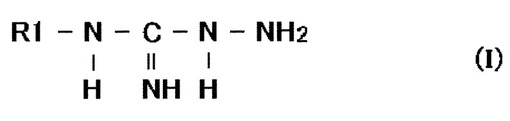
(式中、R1は水素、ハロゲン、ヒドロキシル、置換若しくは非置換低級アルキル、シクロアルキル、低級アルコキシ、低級アルケニル、置換若しくは非置換アラルキル、置換若しくは非置換アリール、置換若しくは非置換複素環基、低級アルカノイル、置換若しくは非置換アロイル、ピリジルカルボニル、低級アルコキシカルボニル、置換若しくは非置換アミノの何れかである)で表される安定化剤とを含有するG6PDH含有試薬。
(もっと読む)
キナーゼ活性測定方法及び試薬
【課題】メシル酸イマチニブが結合可能なキナーゼの活性値を正確に測定することが可能なキナーゼ活性測定方法及び試薬を提供すること。
【解決手段】メシル酸イマチニブが結合可能なキナーゼの活性を測定する方法であって、生体から採取したキナーゼを含む試料と、キナーゼの基質と、ATPとを接触させ、キナーゼの作用で前記基質にリン酸基を導入するリン酸化工程と、リン酸基を導入された基質に標識物質を結合させる工程と、基質に結合した標識物質の標識に基づいてキナーゼの活性を測定する工程と、を含むキナーゼ活性測定方法。
(もっと読む)
癌の治療のためのSMYD3トランスフェラーゼを調整する化合物の同定
本発明は、ポリペプチドのメチルトランスフェラーゼ活性を検出する方法およびメチルトランスフェラーゼ活性のモジュレーター、より具体的には、SMYD3による網膜芽細胞腫のメチル化のモジュレーターをスクリーニングする方法を特徴とする。さらに、本発明は、このように同定されたモジュレーターを用いて、結腸直腸癌、肝細胞癌、膀胱癌および/または乳癌を予防または治療するための方法または薬学的組成物を提供する。N末端短縮型SMYD3(aliasZNFN3A1)は、より高いメチル化活性を有する。Lys824は、SMYD3のRB1タンパク質上の好ましいメチル化部位である。 (もっと読む)
酵素と相互作用する新規化合物の同定法
本発明は、酵素または酵素−化合物複合体を特徴付けるための方法であって、固体担体上に固定化した少なくとも一つの広範囲性リガンドを活用して、酵素をタンパク質調製物から得て、そして、該酵素を質量分析によって特徴付ける、前記方法に関する。これらの方法は、非固定化化合物ライブラリのスクリーニング、リード化合物の選択性プロファイリング、および生細胞における作用機序研究に有用である。 (もっと読む)
HIV感染を阻害する化合物の同定法
本発明は、HIV感染を阻害する薬剤を同定するための新規方法を提供する。抗HIV剤を、PAK3分子のキナーゼ活性または発現を下方制御する能力に関して、試験化合物をスクリーニングすることにより同定する。そのようなPAK3モジュレーターを、さらに、HIV感染を阻害する活性に関して調べる。これらの新規抗HIV剤は、HIV感染およびHIV感染に関連した病気の予防または処置において有用である。  (もっと読む)
(もっと読む)
神経変性疾患に対する診断上及び治療上の標的PRKXタンパク質
本発明は、アルツハイマー病患者及びアルツハイマー病を進展させるリスクのある個体におけるPRKX遺伝子の調節不全及びそのタンパク質産物を開示する。この知見に基づき、本発明は、被験体のアルツハイマー病を診断及び予後判定するための方法、及び被験体がアルツハイマー病を進展させるリスクが増加しているかを決定するための方法を提供する。さらに、本発明は、アルツハイマー病及び関連する神経変性障害を治療及び予防するための、治療及び予防する方法であって、PRKX遺伝子及びその対応する遺伝子産物を用いる方法を提供する。神経変性疾患の調節剤のスクリーニング法もまた開示される。 (もっと読む)
双極性感情障害、統合失調症等の精神病性障害の予防・治療剤、そのスクリーニング方法、及び該疾患の発症リスクの判定方法
【課題】精神病性障害の治療薬、当該治療薬のスクリーニング方法、精神病性障害の診断方法等を提供すること。
【解決手段】CaMKIIαの発現又は機能を促進する物質を有効成分として含有してなる、精神病性障害の予防・治療剤。被検物質がCaMKIIαの発現又は機能を促進し得るか否かを評価し、CaMKIIαの発現又は機能を促進し得る物質を、精神病性障害を予防・治療し得る物質として選択することを含む、精神病性障害を予防・治療し得る物質のスクリーニング方法。生体試料におけるCaMKIIαの発現量又は機能を測定することを含む、精神病性障害の発症又は発症リスクの判定方法。CaMKIIα遺伝子における多型を検出することを含む、精神病性障害の発症リスクの判定方法。
(もっと読む)
281 - 300 / 492
[ Back to top ]