Fターム[4B063QQ27]の内容
酵素、微生物を含む測定、試験 (178,766) | 検体,検出物 (39,509) | 酵素 (3,244) | 転移酵素 (880) | リン酸転移酵素(←キナーゼ) (617)
Fターム[4B063QQ27]の下位に属するFターム
DNA,RNAポリメラーゼ (125)
Fターム[4B063QQ27]に分類される特許
221 - 240 / 492
δ−トコトリエノールによる膵臓癌の治療および予防
トコトリエノール類;すなわちγ−トコトリエノールおよびδ−トコトリエノールを使用して、膵臓癌などの新生物疾患を治療する方法が開示される。ヌードマウスに異種移植されたいくつかのヒト膵臓癌細胞株およびMIA−PACA2ヒト膵臓癌細胞を用いて、これらの化合物の抗腫瘍性効果がインビトロおよびインビボで示される。また、Ki−67およびp27などの代用エンドポイントバイオマーカーに対するそれらの効果を測定することによって潜在的な化学療法剤の効力を試験する方法が開示される。関連する化合物もまた、開示される。  (もっと読む)
(もっと読む)
医薬組合せ剤
本発明は、式(0):
【化1】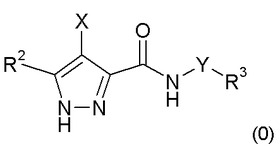
の副化合物と式(I'):
【化2】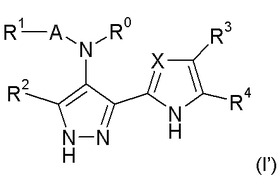
の化合物の組合せ剤を提供する。また包含されるのは、成分化合物の結晶形態、それらの製造方法および癌処置におけるそれらの使用である。 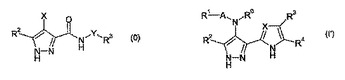 (もっと読む)
(もっと読む)
ZAP−70相互作用分子の同定およびZAP−70の精製のための方法
本発明は、第一の局面において、(a) リン酸化ZAP-70を含有するタンパク質調製物を提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、(c) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体を所与の化合物とともにインキュベーションする段階、および(d) 化合物が固定化アミノピリド-ピリミジンリガンド24からリン酸化ZAP-70を分離できるかどうかを判定する段階を含む、ZAP-70相互作用化合物の同定法を提供する。第二の局面において、本発明は、(a) リン酸化ZAP-70を含有するタンパク質調製物を提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、所与の化合物および固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、ならびに(c) 段階(b)において形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体を検出する段階を含む、ZAP-70相互作用化合物の同定法に関する。第三の局面において、本発明は、(a) リン酸化ZAP-70を含有するタンパク質調製物の二つのアリコートを提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24と一方のアリコートを接触させる段階、(c) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、所与の化合物および固体支持体に固定化されたアミノピリド-ピリミジンリガンド24ともう一方のアリコートを接触させる段階、ならびに(d) 段階(b)および(c)において形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の量を測定する段階を含む、ZAP-70相互作用化合物の同定法を提供する。第四の局面において、本発明は、(a) リン酸化ZAP-70を含有する少なくとも一つの細胞をそれぞれ含む二つのアリコートを提供する段階、(b) 一方のアリコートを所与の化合物とともにインキュベーションする段階、(c) それぞれのアリコートの細胞を収集する段階、(d) タンパク質調製物を得るために細胞を溶解させる段階、(e) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、ならびに(f) 段階(e)においてそれぞれのアリコートで形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の量を測定する段階を含む、ZAP-70相互作用化合物の同定法に関する。
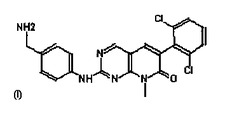 (もっと読む)
(もっと読む)
CDKI経路阻害剤の同定
本発明は、サイクリン依存性キナーゼ阻害剤(CDKI)経路の阻害に関する。より具体的には、本発明は、老化関連疾患および他のCDKI関連疾患の研究及び干渉のためにCDKI経路を阻害するための方法に関する。 (もっと読む)
ヒストン
各プローブ分子がヒストンタンパク質、アイソフォーム、変異体、またはその修飾体由来の配列を含む、少なくとも2つのプローブ分子で官能化された基板支持体を含むことを特徴とするヒストンマイクロアレイ。プローブ分子が異なるヒストンタンパク質由来の配列を含むことを特徴とするヒストンマイクロアレイ。本発明のヒストンマイクロアレイは、ヒストンおよび特定のヒストン修飾に対して特異性をもつ抗体のスクリーニングおよび評価法に利用できる。また、ヒストン修飾が、ヒストン修飾酵素および結合タンパク質の活性と結合に及ぼす影響のスクリーニングおよび評価法にも利用できる。 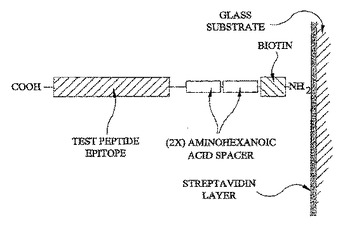 (もっと読む)
(もっと読む)
糖尿病治療薬のスクリーニング方法
【課題】 PDK4に対する特異的な阻害活性の有無を指標にし、当該活性を有する物質を選択するという、PDK4の機能の解明に基づく新規な糖尿病治療薬のスクリーニング方法を提供すること。
【解決手段】 本発明の糖尿病治療薬のスクリーニング方法は、PDK4に対する特異的な阻害活性の有無を指標にし、当該活性を有する物質を選択することを特徴とするものであり、具体的な方法としては、PDK4に対する阻害活性を有し、PDK1、PDK2、PDK3に対する阻害活性を有しない物質を選択する方法が挙げられる。
(もっと読む)
味覚物質同定のための機能的方法
T1R2/T1R3味覚受容体のT1R2モノマーを利用した、甘味応答のアゴニストおよび調節剤を同定するための機能的方法が提供される。 (もっと読む)
神経変性障害及びアルツハイマー病を治療するための、並びに正常な記憶を改善するための方法と組成物
本開示は、概して神経変性障害に関し、さらに詳しくはプレセニリン/Gタンパク質/c-src結合性ポリペプチドの群、並びにアルツハイマー病のシグナル伝達及び進行をモジュレートするための使用方法に関する。 (もっと読む)
肺癌の治療標的としてのNMU−GHSR1b/NTSR1発癌シグナル伝達経路
本発明は、患者由来の生体試料中のニューロメジンU(NMU)遺伝子の発現レベルを決定することによって肺癌の予後を評価するための方法およびキットに関する。本方法および本キットは、非小細胞肺癌(NSCLC)の予後の評価にとって特に望ましい。さらに本発明は、NMUタンパク質と、成長ホルモン分泌促進物質受容体1b(GHSR1b)およびニューロテンシン受容体1(NTSR1)のヘテロ二量体との結合を阻害する化合物を検出することによって、癌、特に肺癌の治療薬剤をスクリーニングする方法に関する。 (もっと読む)
リン酸化検出のためのペプチドアレイ
【課題】ペプチドアレイを用いる測定系において、生体分子の非特異的な影響を受けることなく、結合シグナルを増幅させることにある。特に表面プラズモン(SPR)測定に用いてプロテインキナーゼによるリン酸化を検出する際に、信頼性の高いデータを得ることのできる解析方法を提供する。
【解決手段】固定化されたペプチドのリン酸化を検出するためのアレイであって、該ペプチドの一方の末端がシステイン残基であり、かつアミノ酸配列の中にPEGのような親水性化合物が挿入されてなるペプチドが分子量500以下の架橋剤を介して基板上に固定化されることを特徴とするペプチドアレイ、ならびにペプチドアレイを用いたリン酸化検出方法。
(もっと読む)
膜アンドロゲン受容体(MAR)薬剤の検出
膜アンドロゲン受容体(mAR)を調節する薬剤を検出するための方法を開示する。一態様では、本発明は、リガンド結合するmARを検出及び随意的に同定する方法を提供する。本発明による一アッセイは、古典的細胞内アンドロゲン受容体(iAR又はAR)との結合に関連してmARを選択的に結合する薬剤を検出する。本発明は、mARを優先的に結合する化学物質に関する化学的ライブラリーをスクリーニングする方法を提供することを含む広範囲の有用な適用を有する。 (もっと読む)
薬物発見のための単一分子プラットホーム:抗癌剤および抗ウイルス剤の発見を含む薬物発見のための方法および装置
本出願は、単一分子薬物のスクリーニング、発見および確認のための方法および装置を開示する。これらの方法および装置により、ユーザーは、単一分子の観察を使用し、薬物候補が特定の疾患経路に関与する標的酵素に干渉するかどうか、およびどのように干渉するかを迅速に検出することが可能になる。本明細書に記載された方法および装置は、単一分子の操作および検出技術(例えば、光学的または磁気的ピンセット)を利用して、標的酵素-基質相互作用の特性動力学または「力学的特性」が薬物候補によって実質的に改変または調節されたかどうかを直接検出する。さらに、該方法および装置は、薬物候補の潜在的干渉機構を同定するために力学的特性の調節を分析するのに有用である。本発明の1つの局面において、本明細書に開示された方法および装置は、重合プロセスを阻害するか、さもなければ調節するかのいずれかである薬物候補の存在下での、ポリヌクレオチド基質に沿った個々のポリメラーゼ分子(例えば、DNAポリメラーゼ、RNAポリメラーゼ、および逆転写酵素)のリアルタイム動力学的力学的特性のモニタリングに関する。かかる薬物候補の同定および分析は、抗ウイルス剤、抗癌剤および抗生物質薬物の開発に重要である。 (もっと読む)
キナーゼ活性を求めるための方法、粒子及びキット
試料内のキナーゼ活性を求めるための方法、粒子、及びキットを提供する。本方法の実施形態には、蛍光粒子をアッセイに付することが含まれており、前記蛍光粒子は、1つ以上の蛍光物質を有する支持基質と、その支持基質の官能基を介して前記支持基質に結合されたペプチド基質とを含む。本方法には、更に、前記蛍光粒子をアッセイに付している間に前記ペプチド基質をリン酸化する工程と、前記蛍光粒子を処理する工程であって、そうすることで、前記ペプチド基質が脱リン酸化され、そして分極した二重結合が脱リン酸化部位で生じる工程とが含まれる。加えて、本発明は、前記分極した二重結合を介して前記蛍光粒子に、求核性末端基を有する蛍光レポーターを結合させることも含む。 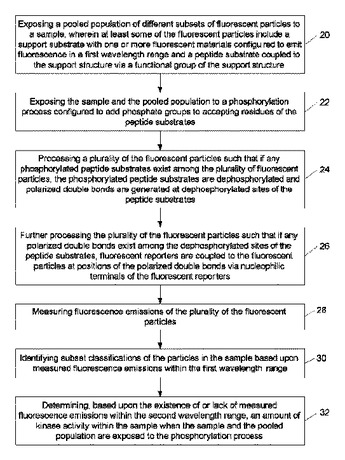 (もっと読む)
(もっと読む)
腫瘍の診断と軽減のための組成物と方法
本発明は、生物学的試料中におけるある種の腫瘍関連キナーゼポリペプチドの存在を決定する方法と、哺乳動物の腫瘍の診断及び治療に有用な組成物に関する。 (もっと読む)
アデノ随伴ウイルスファージ粒子に関する方法および組成物
本発明の態様は概して、発現の増強を達成するために、1つまたは複数のトランスジーンを腫瘍細胞などの標的細胞に、部位特異的な様式で送達する組成物および方法、ならびにそのような適用において有用なコンストラクトおよび組成物に向けられている。ある種の局面では、対象への処置の適用または対象に対する診断手順の前に、治療的核酸からの発現を評価してもよい。 (もっと読む)
悪性腫瘍の性質の判定方法
【課題】悪性腫瘍の性質を精度良く判定することのできる方法を提供する。
【解決手段】 パラメータを獲得する工程と第一比較工程と第二比較工程と判定工程とを含む悪性腫瘍の性質の判定方法を提供する。パラメータを獲得する工程では、悪性腫瘍の腫瘍細胞に含まれる第一のサイクリン依存性キナーゼ(第一CDK)の活性値及び発現量から得られる第一パラメータと、腫瘍細胞に含まれる第二のサイクリン依存性キナーゼ(第二CDK)の活性値及び発現量から得られる第二パラメータと、第一パラメータと第二パラメータに基づいて得られる第三パラメータと、前記腫瘍細胞のサイクリンの発現量から得られる第四パラメータとが獲得される。第一比較工程では、前記第三パラメータが第一の閾値と比較される。第二比較工程では、前記第四パラメータが、第二の閾値と比較される。判定工程では、第一比較結果及び第二比較結果に基づいて悪性腫瘍の性質が判定される。
(もっと読む)
プロテインキナーゼ活性の解析方法
【課題】基質ペプチドのリン酸化検出で、プロテインキナーゼの動態を網羅的にプロファイリングする方法を提供。
【解決手段】プロテインキナーゼの基質ペプチドが基板の金属薄膜上に固定化されたアレイ上の該ペプチドのリン酸化検出で、ビオチン修飾の例えば式(I)のポリアミン亜鉛錯体を作用させ、その後アビジンを作用させてプロテインキナーゼ活性の解析。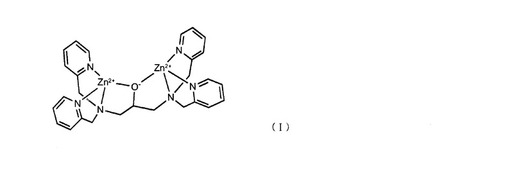 (もっと読む)
(もっと読む)
ホスホエノールピルビン酸:糖ホスホトランスフェラーゼ系タンパク質をコードするコリネバクテリウム−グルタミカム遺伝子
【課題】コリネバクテリウム−グルタミカム由来の新規核酸分子の提供。
【解決手段】コリネバクテリウム−グルタミカム由来の新規PTSタンパク質(ホスホエノールピルビン酸:糖ホスホトランスフェラーゼ)をコードする単離された核酸分子。アンチセンス核酸分子、PTS核酸分子を含む組み換え発現ベクター、および発現ベクターが導入される宿主細胞。また、単離されたPTSタンパク質、突然変異させられたPTSタンパク質、融合タンパク質、抗原性ペプチド、およびC.グルタミカムから得られたPTS遺伝子の遺伝子操作に基づく所望の化合物の製造を改善する方法。
(もっと読む)
リン酸化酵素の新規基質ポリペプチド
【課題】Rho-キナーゼ、タンパク質キナーゼ(PK)C eta、PKC alpha、またはPKC betaにより特異的にリン酸化を受ける基質ポリペプチドを提供する。
【解決手段】Rho-キナーゼ特異的基質として一般式(I)Xaa-Xaa-Xaa-Xaa1-Xaa-Xaa-Ser/Thr-Xaa2-Xaa3-Xaa-Xaa4で表されるポリペプチドが、PKC eta特異的基質として一般式(II)Xaa5-Xaa-Xaa6-Xaa7-Asn-Ser/Thr-Xaa8-Xaa9-Leu-Xaa-Xaaで表されるポリペプチドが、PKC beta特異的基質として一般式(III)Leu-Xaa-Xaa10-Xaa-Xaa11-Ser/Thr-Xaa12-Xaa13-Leu-Xaa-Xaaで表されるポリペプチド。
(もっと読む)
LRRK2が相互作用する分子の同定およびLRRK2の精製のための方法
本発明は第一の側面において、LRRK2が相互作用する化合物を同定のための方法であって、LRRK2を含有するタンパク質調製物を提供する、インドールリガンド91−LRRK2複合体の形成を許容する条件下で、タンパク質調製物を、固体支持体上に固定化されたインドールリガンド91と接触させる、インドールリガンド91−LRRK2複合体を、所定の化合物と共にインキュベーションする、そして化合物が、固定化されたインドールリガンド91からLRRK2を分離することができるかどうかを決定する、というステップを包含する前記方法を提供する。さらに本発明は、LRRK2が相互作用する化合物の同定のための方法であって、LRRK2を含有するタンパク質調製物を提供する、インドールリガンド91−LRRK2複合体の形成を許容する条件下で、タンパク質調製物を、固体支持体上に固定化されたインドールリガンド91、および所定の化合物
と接触させる、そしてインドールリガンド91−LRRK2複合体を検出する、というステップを包含する前記方法に関する。加えて本発明は、LRRK2が相互作用する化合物の同定のための方法であって、LRRK2を含有するタンパク質調製物の2つのアリコートを提供する、インドールリガンド91−LRRK2複合体の形成を許容する条件下で、一方のアリコートを、固体支持体上に固定化されたインドールリガンド91と接触させる、インドールリガンド91−LRRK2複合体の形成を許容する条件下で、他方のアリコートを、固体支持体上に固定化されたインドールリガンド91、および所定の化合物と接触させる、そしてインドールリガンド91−LRRK2複合体の量を決定する、というステップを包含する前記方法を提供する。さらに本発明は、LRRK2の精製のための方法であって、LRRK2を含有するタンパク質調製物を提供する、インドールリガンド91−LRRK2複合体の形成を許容する条件下で、タンパク質調製物を、固体支持体上に固体化されたインドールリガンド91と接触させる、そして固定化されたインドールリガンド91からLRRK2を分離する、というステップを包含する前記方法に関する。
 (もっと読む)
(もっと読む)
221 - 240 / 492
[ Back to top ]



