Fターム[4B063QR16]の内容
酵素、微生物を含む測定、試験 (178,766) | 試薬 (61,469) | 試薬としての酵素 (8,175) | 加水分解酵素 (1,656) | 蛋白質,ペプチド分解酵素 (505)
Fターム[4B063QR16]に分類される特許
201 - 220 / 505
トロンビンインヒビター
本発明は、吸血性節足動物の唾液腺に由来するトロンビン・インヒビター、特に、2または3箇所の異なる部位でトロンビンと相互作用することにより作用する二価および三価のトロンビン・インヒビターに関する。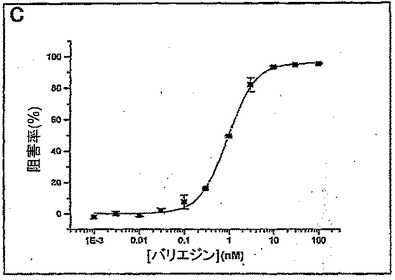
 (もっと読む)
(もっと読む)
脂質を含む組成物を用いたパターニング
チップおよび基材表面を提供する工程、チップ端にパターニング組成物を配置する工程、チップから基材表面にパターニング組成物の少なくともいくらかを堆積させ、基材表面上に配置される堆積物を形成させる工程を含み、パターニング組成物が少なくとも1つの脂質、任意で少なくとも1つの溶媒、ならびに該脂質および任意の溶媒とは異なる少なくとも1つのパターニング種を含む、方法を含む、生体分子アレイを形成するためのより優れた方法を含む、より優れたパターニング法。脂質はDOPC(1,2-ジ-オレオイル-sn-グリセロ-3-ホスホコリン)などのリン脂質でありうる。パターニング種はオリゴヌクレオチドまたはタンパク質でありうる。ナノスケール解像度の堆積物を含むマイクロアレイおよびナノアレイを調製することができる。脂質はパターニングを促進またはパターニング速度を増加させることができる。簡略されたチップ調製が達成できる。ナノスコピック、SPM(原子間力顕微鏡)およびAFM(走査型プローブ顕微鏡)チップを使用することができる。 (もっと読む)
血漿においてタンパク質を検出する方法
本発明は、血漿においてタンパク質を検出する方法を提供し、該方法は、該タンパク質を少なくとも1つの検出可能なフラグメントに消化する能力を有するプロテアーゼに血漿を接触させる工程、ならびに高速液体クロマトグラフィーおよび質量分析を使用して、少なくとも1つの検出可能なフラグメントを検出する工程を含む。 (もっと読む)
新規ペプチダーゼ基質
本発明は、下記の式(I):
[式中、
・XはS;NX1;O;またはNX1-COであり;
・R1は無し、あるいはCl、Br、F、I、OHまたはアルキル、アリールまたはカルボキシル基の置換基の一つであり;
・R2は無し、あるいはCl;O-CH2-O;O-CH3;F、ジエチレンジアミン-CH3、NR3R4、Br、I、OH、アルキル、アリールまたはカルボキシル基、NO2、または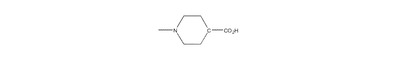
の置換基の一であり;
・X1は、H、C2H4Ph、OH、アルキル基及びアリール基から選択され;
・R3及びR4は、独立にH又は1から4の炭素原子を含むアルキル基であり;
・Pはペプチドである]
の、ペプチダーゼ活性を検出するための酵素基質に関する。 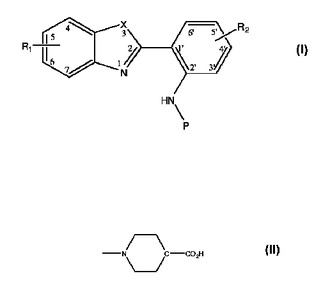 (もっと読む)
(もっと読む)
糖化アルブミン測定試薬
【課題】糖化アルブミンをプロテアーゼで分解し、遊離した糖化アミノ酸に糖化アミノ酸オキシダーゼを作用させ、生成する過酸化水素を測定する糖化アルブミンの測定方法において、プロテアーゼ使用量が少なく、濁りの影響を受けない糖化アルブミン測定方法及び糖化アルブミン測定試薬を提供する。
【解決手段】第4級アンモニウム塩であるトリメチルアンモニウム塩及び/又はジメチルアンモニウム塩を含有させることにより、反応溶液中の濁りの発生を抑制し、プロテアーゼ使用量を低減させることができる。
(もっと読む)
プロテアーゼ耐性ポリペプチドを選択する方法
本発明は、プロテアーゼ、例えばヒトの胃腸管または肺組織に見出されるプロテアーゼによる分解に対して耐性があるペプチドおよびポリペプチドのライブラリーまたはレパートリー(例えば、ディスプレイシステム)からペプチドまたはポリペプチドを選択、単離および/または回収する方法に関する。一般に、本方法はペプチドまたはポリペプチドのライブラリーまたはレパートリーを提供するステップ;プロテアーゼ活性に好適な条件下でそのライブラリーまたはレパートリーをプロテアーゼと組合わせるステップ;およびプロテアーゼによる分解に耐性でありかつ所望の生物学的活性を有するペプチドまたはポリペプチドを選択し、単離しおよび/または回収するステップを含んでなる方法である。選択したペプチドおよびポリペプチドは、例えば、ヒトの胃腸管または肺組織の疾患または症状を治療するための治療薬として有用である。 (もっと読む)
タンパク質の同定方法
【課題】分析対象物と相互作用を有するタンパク質を、効率よく同定する方法を提供すること。
【解決手段】分析対象物と相互作用を有するタンパク質の同定方法であって、(I)分析対象物が共有結合で固定された固相に、タンパク質混合物を接触させる工程、(II)接触により固相上に捕捉されたタンパク質を、固相上でタンパク質分解酵素処理する工程、ついで(III)処理されたタンパク質を質量分析計で測定する工程を含む、同定方法。
(もっと読む)
検体依存性反応における反応ラグ相を決定する方法
【課題】 反応キネティクスの反応ラグ相の特異的な決定をし、これにより反応キネティクスのより正確な評価、そしてさらに検体のより正確な決定を保証する、検体の濃度又は活性の決定方法を得る。
【解決手段】 本発明の方法は、以下の工程
a) 試料を少なくとも1つの試薬と混合し、それによって検体依存性反応を進行中に設定し;
b) 検体依存性反応の結果として時間(t)にわたって変化する信号(x)を測定し、そして信号−時間曲線を保存し;
c) 信号−時間曲線における最大増加を決定し;
d) 信号−時間曲線の反応ラグ相を決定し;
e) 時間に関して反応ラグ相の後にある信号−時間曲線の少なくとも1つのパラメータにより検体の濃度又は活性を決定することからなり、
ここで反応ラグ相の決定は、最初の信号の時間(t0)から時間tlagまでの長さを決定することによって行なわれる。
(もっと読む)
糖化蛋白質測定用組成物
【課題】より正確に糖化蛋白質及び糖化アルブミン割合を測定すること。
【解決手段】本発明は、1)グロブリン成分及びアスコルビン酸の影響回避、2)プロテアーゼ及び少なくとも糖化アミノ酸に作用する酵素の安定化、3)正確にアルブミンを測定、4)糖化ヘモグロビンの影響回避を行うことにより、糖化蛋白質を正確に測定するための組成物、測定方法を提供する。
(もっと読む)
自己免疫性膵炎及び劇症1型糖尿病の検査方法及び検査試薬
【課題】自己免疫性膵炎(AIP)及び劇症1型糖尿病(FT1DM)の検査方法及び検査試薬を提供する。
【解決手段】検体中の、アミラーゼα2−Aと免疫学的に反応する抗体を検出することによりAIPもしくはFT1DMを検査する、または、FT1DMの発症可能性を判定する。この抗体の検出は、例えば、この抗体と免疫学的に反応する抗原を用いる免疫学的方法により行われる。抗原は、好ましくは、ヒトアミラーゼα2−Aのアミノ酸配列のアミノ酸番号299〜512を含む部分断片である。
(もっと読む)
HIV−1のOグループ(またはサブグループ)レトロウイルス性抗原のヌクレオチド配列
【課題】ヌクレオチド配列からの発現、又は化学合成により得られるHIVー1ウイルス粒子から単離することができる配列に相当する抗原、及びその利用に関するペプチドの提供。
【解決手段】上記抗原により誘導されるモノクローナル、ポリクローナル抗体、及びHIV−1のゲノムRNAに相補的なクローン化DNAより生産されるポリペプチド。更にはAIDSの状態にある人のinvitroによる診断方法、及びレトロウイルスに対する免疫原性組成物とワクチン用組成物の産生方法。
(もっと読む)
トロンビンレセプターアンタゴニストによる血小板凝集阻害を測定する方法
トロンビンレセプターアンタゴニストによる血小板凝集阻害を測定する方法が提供される。第一に、トロンビンレセプターアンタゴニストで処置された患者から血液サンプルを採取する。固定化GPIIb/IIIaレセプターリガンドを含む粒子及びトロンビンレセプターアクチベーターを一緒にして前記血液サンプルを混合する。続いて、前記粒子の凝集に適した条件下で前記混合物をインキュベートし、前記混合物で血小板仲介凝集を判定する。凝集がなければ、当該患者は、トロンビンレセプターアンタゴニストによる処置に応答して血小板血栓の形成能力が低下したことを示す。トロンビンレセプターアンタゴニストによる血小板凝集阻害を測定するキットもまた提供される。前記キットは、粒子上に固定されたGPIIb/IIIaレセプターリガンド、トロンビンレセプターアクチベーター、抗凝固剤、及び抗凝固血液を血小板凝集に適した状態で維持するための緩衝物質を含む。 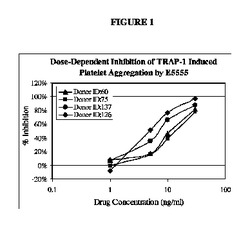 (もっと読む)
(もっと読む)
処理溶液、前処理方法、情報取得方法および検出方法
【課題】大きさが10〜数10μm径の細胞の一つ一つに含まれるタンパク質の種類を高感度で同定する方法を提供すること。また、これを達成するために必要となる検体の処理液を提供すること。
【解決手段】(1)病変組織の切片を、金粒子と消化酵素を含む水溶液で処理し、注目するタンパク質を限定分解分解する工程、(2)TOF−SIMSを用い、断片化したペプチドの二次元分布を測定する工程、(3)プロテオーム解析結果と数値解析的手法を用いることにより、病変組織の切片における注目タンパク質の二次元分布を可視化する工程、の三工程により上記の課題を解決する。
(もっと読む)
細胞表面グリコシル化に関連する方法
本開示は、細胞の細胞表面グリカンを分析することにより、細胞が産生する標的糖タンパク質のグリコシル化を評価するための方法を提供するものである。したがって、本開示は、細胞表面タンパク質のグリコシル化が他のタンパク質のグリコシル化の代用となり得ることを教示するものである。本開示は、ひとつには、細胞によって産生されるタンパク質のグリコシル化に反映される形で、細胞の状態に関する情報を細胞表面グリカンによって得られるという認識に基づくものである。特に、細胞から産生される(かつ任意に分泌される)糖タンパク質のグリコシル化状態に関する情報を細胞表面グリカンによって得られることができることが見いだされている。よって、標的タンパク質のグリコシル化状態に関する情報を得るために、これを細胞から単離する必要がない。 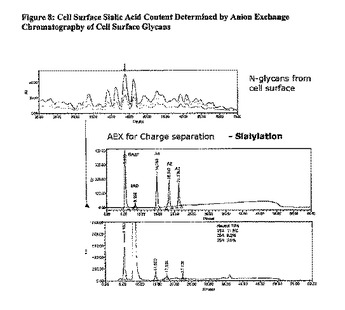 (もっと読む)
(もっと読む)
組織標本からの細胞の調製方法
【課題】組織標本からの細胞の分離調製方法の提供。
【解決手段】下記工程1)〜3)を含むことを特徴とする、組織標本からの細胞の調製方法:
1) 組織標本を、クエン酸溶液中で60〜80℃にて加熱処理する工程、
2) 加熱処理した前記標本を、タンパク質分解酵素で処理する工程、及び
3) 酵素処理した前記標本中の細胞を界面活性剤溶液中に分散させる工程。
(もっと読む)
糖化ヘモグロビンの選択的測定方法
【課題】試料中のヘモグロビンの糖化率を、高精度かつ容易に測定できる方法の提供。
【解決手段】全血試料中の糖化ヘモグロビンを選択的にプロテアーゼで分解し、この糖化ヘモグロビン分解物の糖化部分と糖化アミノ酸酸化還元酵素とを反応させ、この酸化還元反応を測定することによりヘモグロビンの糖化率を決定できる。また、図1に示すように、全血試料において、この方法による糖化ヘモグロビンの測定値とHbA1c濃度とは相関関係にあることから、HbA1cの特徴的構造であるα−アミノ基の糖化部分を測定することなく、糖化ヘモグロビンの測定値から高精度かつ簡便にHbA1c量を求めることができる。
(もっと読む)
プリオンアッセイ
本発明は、試料中のタンパク質を実質的に完全に消化するための少なくとも1種の配列特異的プロテアーゼを用いて、PrPScの存在を検出するアッセイ法であって、PrPSc、PrPC双方におけるオクタリピート領域を無傷で残し、PrPScのプロテアーゼ耐性コアを無傷で、オクタリピート領域に結合したままに残す一方、PrPSc中のプロテアーゼ耐性コアに対応するPrPC中のアミノ酸配列の少なくとも一部を消化・除去するアッセイ法に関する。  (もっと読む)
(もっと読む)
モザイクセリンプロテアーゼ、MSPとその用途
【課題】高病原性トリ(鳥)インフルエンザ、HPAIに対し特異的に有効なワクチンも薬剤も未だ実用化されず、現行の薬剤は重大な副作用を生じるため、更に安全かつ有効な抗ウイルス剤、及びHPAIの基礎と応用研究の進展が待望されている。併せて、MSPが関与するペプチドホルモン産生異常の診断方法の確立も重要課題である。
【解決手段】モザイクセリンプロテアーゼ、MSPに属するMSPL、MSPS及びTMPRSS13阻害剤;これ等の酵素による基質の分解度又は開裂度を指標に用いる上記阻害剤のスクリーニング方法;該阻害剤を有効成分とする抗ウイルス剤及びペプチドホルモン疾患の治療薬;HPAIウイルスの感染と増殖を高め量産を可能にする活性化剤;前記酵素を有効成分とするペプチドホルモン疾患の治療薬;前記酵素の遺伝子発現量を指標として用いるホルモン疾患の診断剤等。
(もっと読む)
プリオンELISA
試料中のPrPScを検出するためのアッセイが記載される。詳細には、病原性プリオンELISAが記載される。このアッセイは、PrPScを捕捉するための病原性プリオン特異的試薬、および試料中に存在することがある非病原性プリオンタンパク質による干渉量を減少させるための、部位特異的プロテアーゼ、例えばトリプシンまたはSV−8プロテアーゼによる消化を利用する。本発明の別の態様では本明細書に記載の検出方法のいずれかによって、対象由来の生体試料中の病原性プリオンの存在を検出することにより、前記対象のプリオン関連疾患を診断する方法を提供する。  (もっと読む)
(もっと読む)
核酸を内部移行している細胞の選択方法
生体への毒性および非特異的作用を低減して細胞に薬剤を送達できる化合物の同定および選択が必要である。加えて、所定の組織、細胞または細胞群に薬剤を迅速に内部移行可能な化合物を選択する方法が必要である。本発明は、核酸標的指向化、ならびにRNA含有分子の選択および送達のための方法、組成物およびキットに関する。本発明は、1つまたは複数の細胞をランダムRNA含有ライブラリーと接触させ、接触した細胞を変性剤または1つもしくは複数のヌクレアーゼによる消化で処理し、細胞からヌクレアーゼまたは変性剤に耐性の1つまたは複数の内部移行した核酸を抽出するための組成物および方法を含む。 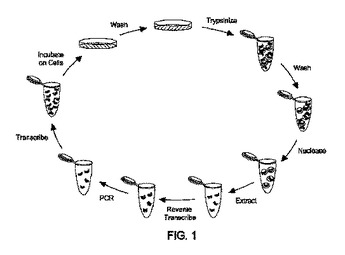 (もっと読む)
(もっと読む)
201 - 220 / 505
[ Back to top ]