Fターム[4B064CA21]の内容
微生物による化合物の製造 (77,679) | 生物材料(微生物、酵素等) (21,110) | 酵素、酵素前駆体 (2,518)
Fターム[4B064CA21]の下位に属するFターム
化学的に変性されたもの (33)
Fターム[4B064CA21]に分類される特許
2,281 - 2,300 / 2,485
オリーブポリフェノール濃縮物
オリーブオイル抽出物の副産物からオリーブポリフェノール濃縮物が得られるプロセスであって、(a)副産物を極性溶媒と混合して副産物/溶媒混合物を得て、(b)該混合物からポリフェノールを抽出してオリーブポリフェノール溶液と抽出固体とを得て、(c)膜分離法技術により該溶液を濃縮してオリーブポリフェノール濃縮物を収量するステップを含んでなり、存在するポリフェノールの濃縮物が少なくとも10wt%であり、さらに脱脂ステップが行われる。 (もっと読む)
(メタ)アクリル酸エステルの酵素的製造
異なるヒドロキシ基を有するポリアルコールの部分エステル化された(メタ)アクリル酸エステルの製造方法、それらの製造方法及びそれらの使用。 (もっと読む)
ランチビオティックの精製法
開示するのは、ランチビオティックを含有する粗または部分精製した溶液からランチビオティックを精製する方法である。好適な態様ではランチビオティックはナイシンであるが、ランチビオティックの共通する構造的特徴が、ランチビオティック種の他の員について開示された精製法の効力を必然的に定める。この方法にはランチビオティックおよびタンパク質分解酵素を含有する溶液を含んでなるインキュベーション混合物を形成し、そして混合物を選択的なタンパク質分解活性について至適化された条件下でインキュベーションする工程を含む。 (もっと読む)
粘膜送達のための方法および製品
本発明は、多糖類製剤の非侵襲性送達に関連した方法および製品を特徴とする。 (もっと読む)
セスキテルペン合成及び使用方法
本発明は、セスキテルペン合成酵素及びその製造方法及びその使用に関する。一実施態様では、本発明は、少なくとも1種のセスキテルペン合成酵素をコードする前記のヌクレオチド配列を有する核酸を提供する。更なる実施態様では、また本発明はセスキテルペン合成酵素及びこれらの酵素の製造方法及び使用方法を提供する。例えば本発明のセスキテルペン合成酵素を用いて、ファルネシルピロリン酸を種々に酸素化された及び脂肪族のセスキテルペン、例えばバレンセン、ビシクロゲルマクレン、クベボール及びδ−カジネンに変換することができる。 (もっと読む)
変異型キシリトールデヒドロゲナーゼ酵素、これを産生する微生物、該酵素または微生物を用いたキシリトールをキシルロースに変換する方法
【課題】 野生型キシリトールデヒドロゲナーゼ(XDH)の補酵素要求性をニコチンアミドアデニンジヌクレオチドリン酸(NADP)型に改良するとともに耐熱性を向上させ、キシリトールからキシルロースへの変換効率を高めた変異型XDHを提供すること。
【解決手段】 野生型XDHの補酵素要求性をNADP要求性に変えるために、そのアミノ酸配列の207番目のアスパラギン酸をアラニンに、208番目のイソロイシンをアルギニンに、209番目のフェニルアラニンをスレオニンもしくはチロシンに、211番目のアスパラギンをアルギニンに置換し、耐熱性を向上させるために、96番目のセリンをシステインに、99番目のセリンをシステインに、102番目のチロシンをシステインに置換して、構造安定化亜鉛結合部位を導入する。
(もっと読む)
カロチノイドの生物変換方法
この発明は、チトクロムP450モノオキシゲナーゼ活性を有する酵素、特に好熱性細菌、特にThermus属エス・ピーのモノオキシゲナーゼ、を用いたカロチノイドの生物変換方法に関する。  (もっと読む)
(もっと読む)
光学活性3−アリール−3−ヒドロキシプロピオン酸及び光学活性3−アリール−3−ヒドロキシプロピオン酸アルキルエステルの製造方法
【課題】 3−アリール−3−ヒドロキシプロピオン酸アルキルエステル(ラセミ体混合物)から、光学活性3−アリール−3−ヒドロキシプロピオン酸及び光学活性3−アリール−3−ヒドロキシプロピオン酸アルキルエステルの製造方法を提供する。
【解決手段】 加水分解酵素の存在下、3−アリール−3−ヒドロキシプロピオン酸アルキルエステル(ラセミ体混合物)の片方のエナンチオマーのみを選択的に加水分解反応させて、光学活性(S又はR)−3−アリール−3−ヒドロキシプロピオン酸を生成させるとともに、未反応の光学活性(R又はS)−3−アリール−3−ヒドロキシプロピオン酸アルキルエステル(逆の立体絶対配置を有する。)を得ることからなる。
(もっと読む)
前生物学的調製物
本発明は、アラビノキシランを含む栄養的添加剤に関する。これは、ヒトの腸内微生物叢の調節を手助けする。さらに、添加剤を含むいくつかの食品および飲料、さらには、上記添加剤を調製するための方法が提供される。 (もっと読む)
治療用縮合二環式アミノ酸の製造における中間体
本発明は、治療用縮合二環式アミノ酸の製造における中間体である、式(I)の化合物(式中、Rは、Hまたは適当なカルボン酸保護基を表す)を提供する。
【化1】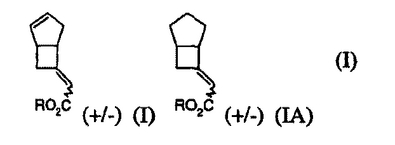
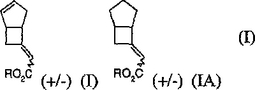 (もっと読む)
(もっと読む)
脂溶性化合物の水分散性製品形態の製造用変性ルピンタンパク質
この発明は、0.1〜20質量%の乾燥質量含有率を有する天然由来のルピンタンパク質を含む水溶液又は水懸濁液のpHを3〜9に調整する工程と、前記ルピンタンパク質の乾燥質量に対して、0.01〜10質量%のプロテアーゼを添加する工程と、前記タンパク質溶液又は懸濁液を、5〜70℃の温度で、加水分解率が1〜30%になるまで、加熱する工程と、前記プロテアーゼを不活性化する工程とを含む変性ルピンタンパク質の製造方法、この製造方法によって得られる変性ルピンタンパク質、脂溶性活性成分又は着色剤と共に前記ルピンタンパク質を含む組成物、並びに、食品、飲料類、動物用食品類、化粧品類又は医薬品類用の、富化剤、補強剤、及び/又は、着色剤としての前記組成物の使用に関する。さらに、この発明は、前記組成物を含む、食品、飲料類、動物用食品類、化粧品類又は医薬品類に関する。 (もっと読む)
光学活性なN−置換ピロリジン−3−カルボン酸の製造方法
【課題】 光学活性なN−置換ピロリジン−3−カルボン酸を製造する際に、反応工程数が少なく工業的にも有利な製造法を提供する。
【解決手段】 N−置換ピロリジン−3−カルボン酸エステル(1)を不斉加水分解する能力を有する酵素の存在下に加水分解することを特徴とする光学活性なN−置換ピロリジン−3−カルボン酸(2)の製造法。
(1)
(2)
[式中、Pはイミノ基の保護基を表す。Rは炭素数1〜8の直鎖状アルキル基又は炭素数1〜8の分岐状アルキル基を表す。*印は不斉炭素原子であることを示す。]
(もっと読む)
光学活性−エリスロ−3−シクロヘキシルセリンの製造方法
本発明は下記一般式(1)で示されるDL−エリスロ−3−置換セリンのN−アシル体を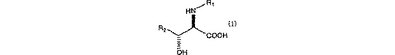
(式中、R1は、炭素数1ないし10のアルカノイル基、ベンゾイル基、ハロゲン原子により置換された炭素数1ないし5のアルカノイル基又はハロゲン原子により置換されたベンゾイル基を表し、R2はフェニル基もしくはシクロヘキシル基を意味する。)L−アミノアシラーゼまたはD−アミノアシラーゼにより不斉加水分解し、L−アミノアシラーゼの場合には未反応のN−アシル−D−エリスロ−3−置換セリンを得、D−アミノアシラーゼの場合には加水分解されたD−エリスロ−3−置換セリン得る方法に関するもので、該D−エリスロ体は医薬品、例えば抗HIV薬として有用なことが知られている薬剤(WO01/40227)等の中間体として有用である。 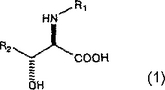 (もっと読む)
(もっと読む)
エノンレダクターゼ遺伝子およびレボディオンの微生物産生
エノンレダクターゼ活性を有する酵素をコードするヌクレオチド配列を含む単離されたDNAが開示され、ここで、この酵素は以下の物理化学的特性によって特徴付けられる:(a)分子量:61,300±5,000Da(ゲル濾過を用いて推定;1つのサブユニットからなる);(b)補因子:NADPHおよびNADH;(c)基質特異性:α,β-不飽和ケトンに対して活性;(d)最適温度:pH 7.4で55℃〜60℃;および(e)最適pH:pH 4.5〜pH 8.5。 (もっと読む)
プレガバリン及び関連化合物の製造
【課題】商業的に実行可能なプレガバリンの製造方法の提供。
【解決手段】酵素的速度論的分割を経た(2)−(+)−3−アミノメチル−5−メチル−ヘキサン酸及び構造的に関連した化合物の製造法。
(もっと読む)
高められた粘度を有する含水媒体、該媒体の製造法及び使用
本発明は、変性がa)ポリフェノールオキシダーゼ活性を有するタンパク質、及び/又はb)ヒドロラーゼ、オキシドレダクターゼ及びペルオキシダーゼを含有する酵素混合物により行われていることを特徴とする、オキシダーゼを用いて変性された、フェノール性置換基を有するゲル化可能なポリマー成分を含有する、高められた粘度を有する含水媒体に関する。相応する変性された媒体は、有利に(部分)乾燥された及び/又は(部分)再水和された状態のゲルであり、その粘度もしくはゲル強度を意図的に調節することができ、乾燥工程及び再水和の後であっても、もとの粘度もしくはゲル強度を再度安定に達成することができる。更に、含水媒体は、感覚的な特性に影響を与えるゲルの品質に不利な影響を与える副生成物を有しない。含水媒体の他に、高められた粘度を有する相応する含水媒体を製造し、オキシドレダクターゼ、ペルオキシダーゼ、ヒドロラーゼ及び/又はカタラーゼを使用する方法も開示される。適用分野として、開示された含水媒体のために、食品分野、化粧品分野及び製薬学的目的が予定される。 (もっと読む)
魚鱗からのコラーゲンペプチドの製造方法
【課題】製造工程を短縮し製造コストを下げるとともに高濃度でコラーゲンペプチドを抽出することができる、酵素分解による魚鱗からのコラーゲンペプチドの製造方法を提供する。
【解決手段】魚鱗を蛋白質分解酵素と魚鱗の構造を破壊する酵素とにより酵素分解し、コラーゲンペプチドを得る。このとき、魚鱗から多段階の酵素分解によりコラーゲンペプチドを抽出し、最終段階の酵素分解で魚鱗の構造を破壊する酵素を使用する。これにより、コラーゲンペプチドを高収率で得ることができる。魚鱗を酵素分解する途中で原料となる魚鱗を追加することが好ましい。魚鱗の構造を破壊する酵素にはケラチナーゼまたはキチナーゼを用いることが好ましい。魚鱗は酸性領域で脱灰した魚鱗から成り、蛋白質分解酵素は至適pHが酸性側にあることが好ましい。
(もっと読む)
ケトイソフォロンからアクチノールを産生するプロセス
組換え型微生物が、例えば、レボジオンレダクターゼ遺伝子、例えばC. アクアチクム(C. aquaticum)AKU611(FREM BP-6448)またはその変異体のようなコリネバクテリウム(Corynebacterium)属に属する微生物に由来するレボジオンレダクターゼ遺伝子によって、ケトイソフォロンをレボジオンに還元することができる、市販のパン酵母、出芽酵母菌(Saccharomyces cerevisie)ATCC7754、サッカロミセス・ロウキシイ(Zygosaccharomyces rouxii)HUT7191(IFO 0494)、サッカロミセス・デルブルエキイ(Saccharomyces unisporus、IFO 0298)、サッカロミセス・デルブルエキイ(Torulaspora delbrueckeii)HUT7102、サッカロミセス・ウィリアヌス(Saccharomyces willianus)HUT7106、チゴサッカロミセス・バイリイ(Zygosaccharomyces bailii)ATCC11486、カンジダ・トロピカリス(Candida tropicalis)IFO 1403、およびその変異体のような、サッカロミセス(Saccharomyces)属、チゴサッカロミセス(Zygosaccharomyces)属、およびカンジダ(Candida)属の微生物からなる群より選択される、宿主微生物を形質転換することによって得ることができる、反応混合物において組換え型微生物またはその無細胞抽出物にケトイソフォロンを接触させる段階、ならびに反応混合物から産生されたアクチノールを単離する段階を含む、ケトイソフォロンからアクチノールを産生するプロセスを開示する。 (もっと読む)
SQS遺伝子
本発明は、微生物によるカロテノイドの産生を増加させる方法において有用な遺伝子に関する。カロテノイド、アスタキサンチンは、動物、藻類、及び微生物のような多様な生物に分布している。それは、活性酸素種に対する強力な抗酸化特性を有する。アスタキサンチンは、動物に独特の橙〜赤色の着色を賦与し、市場における消費者へのアピールに貢献するため、特に、サケのような養殖魚の産業において、着色試薬として使用されている。 (もっと読む)
3−シアノグルタル酸モノエステル類及びその製造方法
【課題】 光学活性な又はラセミ体の3−シアノグルタル酸モノエステル類の提供。
【解決手段】 下式(1)で示される光学活性な又はラセミ体の3−シアノグルタル酸モノエステル類。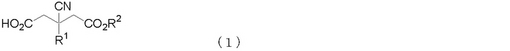
[式中、R1は水素原子、アルキル基、アルケニル基、フェニル基、ナフチル基、ピリジル基、チオフェン−2−イル基又はチオフェン−3−イル基を表す。該フェニル基及びナフチル基の水素原子は、それぞれ、アルキル基、トリアルキルシリルオキシ基、水酸基、アルコキシ基、ハロゲン原子及びトリフルオロメチル基からなる群より選ばれる置換基で置換されていてもよい。また、該ピリジル基の水素原子はアルキル基、アルコキシ基及びハロゲン原子からなる群より選ばれる置換基で置換されていてもよい。R2は炭素数1〜4のアルキル基を表す。]
(もっと読む)
2,281 - 2,300 / 2,485
[ Back to top ]