Fターム[4C065EE04]の内容
その他のN系縮合複素環 (61,549) | 縮合環系中の複素環の数 (4,661) | 4 (51)
Fターム[4C065EE04]に分類される特許
21 - 40 / 51
架橋複素環化合物およびその使用
本開示は、個体においてヒスタミン受容体を調節するために使用することができる新たな化合物に関する。新たな架橋複素環[4,3−b]インドール化合物を包含する新規な化合物が記載されている。医薬組成物も提供されている。前記化合物を含む医薬組成物、同様に、認識障害、精神障害、神経伝達物質媒介障害および/または神経障害の治療を包含する様々な治療用途における前記化合物の使用方法もまた提供されている。本発明の化合物は、新規なヒスタミン受容体調節剤として記載され、また、神経変性疾患を治療する際に使用することもできる。 (もっと読む)
有機トランジスタ
【課題】高い移動度、大きな電流オン/オフ比を有した有機トランジスタを提供する。
【解決手段】一般式(1)で表される化合物を少なくとも1種含有の有機半導体層。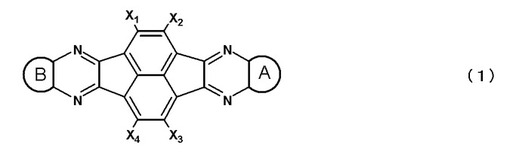
(式中、X1〜X4はそれぞれ独立に、水素原子、ハロゲン原子、直鎖、分岐または環状のアルキル基、直鎖、分岐または環状のアルコキシ基、あるいは置換または未置換のアリール基を表し、さらに、X1とX2、あるいはX3とX4は互いに結合して置換または未置換のベンゼン環を形成していてもよく、環Aおよび環Bはそれぞれ独立に、置換または未置換のベンゼン環、置換または未置換のナフタレン環、置換または未置換のフェナントレン環、置換または未置換のピリジン環、置換または未置換のキノリン環、置換または未置換のピラジン環、あるいは置換または未置換のキノキサリン環を表す)
(もっと読む)
環状化合物、その金属錯体及び変性金属錯体
【課題】耐酸性や耐熱性が優れる金属錯体及び燃料電池用電極触媒の提供。
【解決手段】下記一般式(1)で表される化合物。
(式中、Y1〜Y4は、それぞれ独立に、−N=等を表す。P1〜P6は、対応するY1〜Y4あるいはZ1〜Z2が結合した炭素原子と、隣接位の2つの炭素原子と一体となって複素環を形成する。Q1及びQ2はそれぞれ独立に、連結基または直接結合を表す。Z1及びZ2は、それぞれ独立に、−NR2等を表す。)
(もっと読む)
禁煙を促進するための化合物及び方法
【課題】禁煙及びその他の疾患を治療するための化合物及び方法を提供する。
【解決手段】式(I)〜(III)で表される化合物及び医薬として許容可能なその塩を活性化合物として用いる。
(もっと読む)
HIVインテグラーゼ阻害活性を有する多環性カルバモイルピリドン誘導体
【課題】抗ウイルス作用、特にHIVインテグラーゼ阻害活性を有する抗HIV薬の提供。
【解決手段】下記式の化合物(I)、及びそれを含有する抗HIV薬。
(式中、Z1は、NR4;R1は、水素または低級アルキル;Xは、単結合、O、S、SO、SO2およびNHから選択されるヘテロ原子基、または該ヘテロ原子基が介在していてもよい低級アルキレンもしくは低級アルケニレン;R2は、置換されていてもよいアリール;R3は水素、ハロゲン、ヒドロキシ、置換されていてもよい低級アルキル等;R4およびZ2は一緒になって環を形成し、多環性化合物(例えば、3環性または4環性化合物を含む)を形成する。)
(もっと読む)
ハロゲン含有のペリレンテトラカルボン酸誘導体及びそれらの使用
本発明は、式(I)で示され、その式中、Y1及びY2がO又はNRaもしくはNRbを表し、その際、Ra及びRbがHもしくはオルガニルを表し;Z1〜Z4がOもしくはSを表し;R11〜R14、R21〜R24がCl、Fを表し;その際また基R11〜R14、R21〜R24の1もしくは2つがCNを表してよく、かつ/又は基R11〜R14、R21〜R24の1つがHを表してよく;かつその際Y1がNRaを表し、Z1もしくはZ2がNRcを表してもよく、その際、Ra及びRcは一緒になって架橋基Xであって2〜5個の原子を有する基を表し;かつその際Y2がNRbを表す場合に、Z3もしくはZ4がNRdを表してもよく、その際、Rb及びRdは一緒になって架橋基Xであって2〜5個の原子を有する基を表す化合物、その製造方法と、前記化合物を、発光体材料、電荷輸送材料もしくは励起子輸送材料として用いる使用に関する。 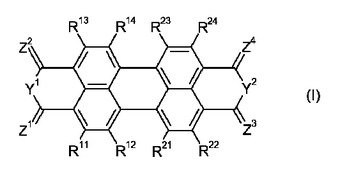 (もっと読む)
(もっと読む)
抗菌剤として使用のスピロ縮合バルビツール酸誘導体
1つの側面において、本発明は、式(I)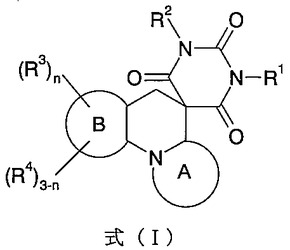
の化合物、その医薬的に許容される塩、それらを使用して細菌感染症を治療する方法、そしてそれらの製造の方法に関する。 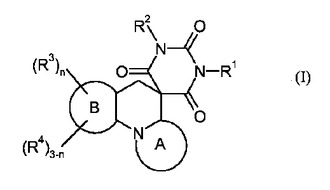 (もっと読む)
(もっと読む)
新規トリアザベンゾ[a]ナフト[2,1,8−cde]アズレン誘導体、その製造法、及びそれを含有する医薬組成物
本発明は、式(I)で示される化合物、その鏡像異性体、ジアステレオ異性体及びN−オキシド、ならびに薬学的に許容され得る酸又は塩基とのその付加塩に関するものである。本発明の化合物は、強力なチロシンヒドロキシラーゼ誘導物質である。 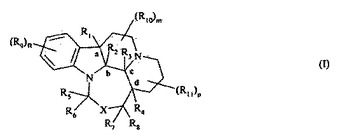 (もっと読む)
(もっと読む)
新規有害生物防除剤
【課題】有害生物防除剤として有用な新規化合物を提供する。
【解決手段】前記化合物は、式(1):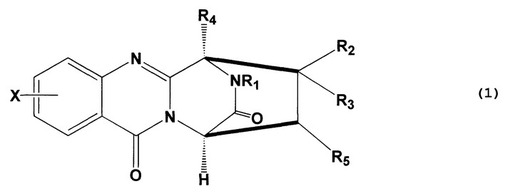
で表されるPF1198A誘導体(具体的には、例えば、9-クロロ-アラントリピノン)である。
(もっと読む)
多環式化合物の精製方法、多環式化合物の製造方法、及び多環式化合物の用途
【課題】 本発明は、硫酸などの不純物を実質的に含まない多環式化合物の製造方法を提供する。
【解決手段】 スルホン化処理をし、−SO3M基を有する多環式化合物(ただし、Mは対イオンを表す)を合成する工程、前記合成物を、SO42−又はSO3−が溶解し且つ前記多環式化合物が難溶な有機溶媒に混合して分散液を得る工程、前記分散液をろ過して多環式化合物を分離する工程、を有することを特徴とする多環式化合物の製造方法。
多環式化合物としては、下記式(I)のキノキサリン誘導体が挙げられる。
【化1】 (もっと読む)
(もっと読む)
有機トランジスタ
【課題】無機半導体デバイスに比べて簡便なプロセスで素子を作製することが可能であり、かつ長時間安定したトランジスタ特性を示す有機トランジスタを提供する。
【解決手段】有機半導体層が、下式で表される化合物を含有する有機トランジスタ。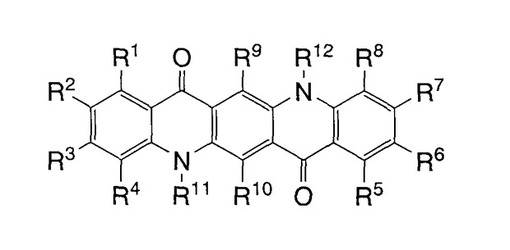
(R1〜R12は、水素原子又は有機残基。R1〜R8の隣り合う同士は環を形成しても可)
(もっと読む)
有機電界効果トランジスタの製造方法
以下の工程:a)基板上に配置されたゲート構造と、ソース電極と、ドレイン電極とを有する基板を提供する工程と、b)前記基板のゲート構造と、ソース電極と、ドレイン電極とが配置された領域に、n型の有機半導体化合物を適用する工程とを含む有機電界効果トランジスタの製造方法において、前記のn型の有機半導体化合物が、式Iで示され、R1、R2、R3及びR4が、無関係に、水素、塩素もしくは臭素であるが、但し、これらの基の少なくとも1つは、水素ではなく、Y1が、OもしくはNRaであり、その際、Raが、水素もしくはオルガニル基であり、Y2が、OもしくはNRbであり、その際、Rbが、水素もしくはオルガニル基であり、Z1、Z2、Z3及びZ4が、Oであり、Y1がNRaの場合に、基Z1及びZ2の一方は、NRc基であってよく、その際、RaとRcは、一緒になって、末端の結合の間に2〜5個の原子を有する橋かけ基であり、Y2がNRbの場合に、基Z3及びZ4の一方は、NRd基であってよく、その際、RbとRdは、一緒になって、末端の結合の間に2〜5個の原子を有する橋かけ基である化合物から選択されることを特徴とする方法。 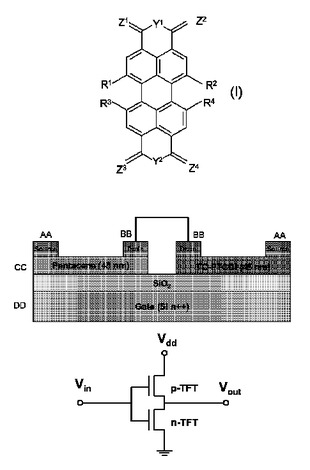 (もっと読む)
(もっと読む)
複素環型ペリレン誘導体及び有機エレクトロルミネッセンス素子
【課題】色純度がよく実用的な発光効率と寿命を有する有機EL素子を提供する。
【解決手段】下記式(1)又は式(2)で表されるペリレン誘導体。及び、陰極と陽極と、これらの間に発光層を含む一層又は複数層からなる有機薄膜層とを有し、有機薄膜層の少なくとも一層が、上記のペリレン誘導体、及び核炭素数10〜50の縮合芳香族環を有する化合物を含有する有機エレクトロルミネッセンス素子。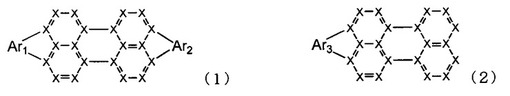
(式中、Ar1,Ar2,Ar3は、それぞれ独立に芳香環又は芳香複素環であり、Xは炭素原子又はヘテロ原子である。)
(もっと読む)
ナフタレンテトラカルボン酸誘導体及び半導体としてのその使用
本発明は、一般式(I)で示され、その式中、R1、R2、R3及びR4は、Br、F及びCNから選択される置換基を表し、かつその他の基は、水素を表し、Y1は、OもしくはNRaを表し、その際、Raは、水素もしくはオルガニル基を表し、Y2は、OもしくはNRbを表し、その際、Rbは、水素もしくはオルガニル基を表し、Z1及びZ2は、互いに無関係に、OもしくはNRcを表し、その際、Rcは、オルガニル基を表し、Z3及びZ4は、互いに無関係に、OもしくはNRdを表し、その際、Rdは、オルガニル基を表す、ナフタレンテトラカルボン酸誘導体、その製造方法並びに前記誘導体を、特にn型の半導体として用いる使用に関する。 (もっと読む)
光導電性部材
【課題】例えば、青色光照射に対して優れた感光性を有する光伝導性部材用の材料を提供する。
【解決手段】次の構造式を持つ化合物であって、式中、R1、R2、R3、およびR4のそれぞれは同じまたは異なるものであって、水素、アルキル、アリール、および炭化水素から成る群より独立して選ばれる。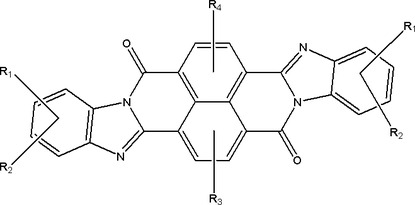
(1)
(もっと読む)
スピロラクタム二環式CGRP受容体アンタゴニスト
CGRP受容体のアンタゴニストであり、及び偏頭痛などのCGRPが関与する疾病の治療又は予防において有用である式(I)の化合物: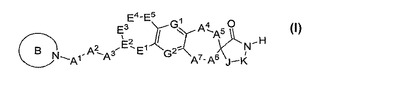
(変数A1、A2、A3、A4、A5、A6、A7、B、E1、E2、E3、E4、E5、G1、G2、J及びKは、本明細書に記載されているとおりである。)。本発明は、これらの化合物を含む医薬組成物並びにCGRPが関与するこのような疾病の治療又は予防におけるこれらの化合物及び組成物の使用にも関する。  (もっと読む)
(もっと読む)
JANUSキナーゼの四環系阻害剤
本発明は、Janusキナーゼの活性を調節し、Janusキナーゼの活性に関連する疾患、例えば、免疫関連疾患、皮膚障害、骨髄増殖性障害、癌、およびその他の疾患の治療に有用な化合物を提供する。 (もっと読む)
ガンマセクレターゼの架橋N−環状スルホンアミド阻害剤
本発明は,式I:
【化116】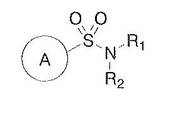
[式中,Aは明細書において説明されるとおりであり,R1およびR2は,一緒になって,[3.3.1]または[3.2.1]環系を形成し,ここで,窒素は2つの橋頭炭素に結合しており,および[3.3.1]または[3.2.1]環系は,任意に,ヘテロアリールまたはヘテロシクロアルキル環と縮合していてもよい]
のN−環状スルホンア認識傷害,例えばアルツハイマー病の治療または予防に有用である。本発明はまた,式Iの化合物を含む医薬組成物,アルツハイマー病等の認識傷害を治療する方法,および式Iの化合物を製造するのに有用な中間体を包含する。 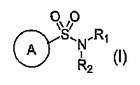 (もっと読む)
(もっと読む)
ナフタレンアミジンイミド
【課題】ナフタレンアミジンイミドの提供。
【解決手段】 式
【化1】
(式中、
R1、R2、R3、R4、R5及びR6は、互いに独立して、水素原子;又は炭素原子数1ないし37のアルキル基を表わすが;
ここで、
−炭素原子数1ないし37のアルキル基のCH2単位の1ないし10個は、互いに独立して、カルボニル基;酸素原子;硫黄原子;セレニウム原子;テルリウム原子;シス−又はトランス−CH=CH−基;アセチレン性のC≡C−基;1,2−、1,3−又は1,4−置換フェニル基;2,3−、2,4−、2,5−、2,6−、3,4−又は3,5−二置換ピリジン基;2,3−、2,4−、2,5−又は3,4−二置換チオフェン基;1,2−、1,3−、1,4−、1,5−、1,6−、1,7−、1,8−、2,3−、2,6−又は2,7−二置換1,2−、1,3−、1,4−、1,5−、1,6−、1,7−、1,8−、1,9−、1,10−、2,3−、2,6−、2,7−、2,9−、2,10−又は9,10−二置換アントラセン基によって置換され得−;ここで、CH=CH−基の1個又は2個のCH−基、ナフタレン基及びアントラセン基は、窒素原子で置換され得;
−CH2−基の単独の水素原子の12個までは、互いに独立して、フッ素原子;塩素原子;臭素原子;又はヨウ素原子;シアノ基;18個までの炭素原子を有する直鎖のアルキル基;シス−又はトランス−CH=CH−基;アセチレン性のC≡C−基;1,2−、1,3−又は1,4−置換フェニル基;2,3−、2,4−、2,5−、2,6−、3,4−又は3,5−二置換ピリジン基;2,3−、2,4−、2,5−又は3,4−二置換チオフェン基;1,2−、1,3−、1,4−、1,5−、1,6−、1,7−、1,8−、2,3−、2,6−又は2,7−二置換ナフタレン基;1,2−、1,3−、1,4−、1,5−、1,6−、1,7−、1,8−、1,9−、1,10−、2,3−、2,6−、2,7−、2,9−、2,10−又は9,10−二置換アントラセン基によって、同一の炭素原子において置換され得−;ここで、アルキル鎖の6個までのCH2−単位は、互いに独立して、カルボニル基;酸素原子;硫黄原子;セレニウム原子;テルリウム原子によって置換され得、かつアルキル基の−CH2−基の単独の水素原子の12個までの各々はまた、互いに独立して、フッ素原子、塩素原子、臭素原子又はヨウ素原子又はシアノ基又は18個までの炭素原子を有する直鎖のアルキル基によって同一のC−原子において置換され得、ここで、1ないし6個のCH2−単位は、互いに独立して、カルボニル基、酸素原子、硫黄原子、セレニウム原子、テルリウム原子、シス−又はトランス−CH=CH−基によって置換され得、ここで、1個のCH−単位はまた、窒素原子によって、アセチレン性のC≡C−基、1,2−、1,3−又は1,4−置換フェニル基、2,3−、2,4−、2,5−、2,6−、3,4−又は3,5−二置換ピリジン基、2,3−、2,4−、2,5−又は3,4−二置換チオフェン基;1,2−、1,3−、1,4−、1,
5−、1,6−、1,7−、1,8−、2,3−、2,6−又は2,7−二置換ナフタレン基によって置換され得、ここで、1又は2個の炭素原子は、窒素原子によって、1,2−、1,3−、1,4−、1,5−、1,6−、1,7−、1,8−、1,9−、1,10−、2,3−、2,6−、2,7−、2,9−、2,10−又は9,10−二置換アントラセン基によって置換され得、ここで、1又は2個の炭素原子は、窒素原子によって置換され得るか;又は、
置換基の代わりに、メチン−又は四級炭素原子の遊離原子価は、対になって結合してシクロヘキサン環等の環を形成し得るか;又は、
R1及びR2が炭素原子C1及びC2と一緒になって又はR3及びR4が炭素原子C3及びC4と一緒になって6−員基を形成する場合、アミノ基を表わし;
=NH−が窒素原子N1(R6における)と一緒になって又は窒素原子N2(R7における)と一緒になって5−員基を形成する場合、R7及びR8は、互いに独立して、=O;又は=NH−を表わす。)で表わされるナフタレンアミジンを開示する。
該化合物は、様々な目的のために、好ましくは化粧品用途のUV吸収剤として有用である。
(もっと読む)
環式アニリノ−ピリジノトリアジン
本発明は式(I)
【化1】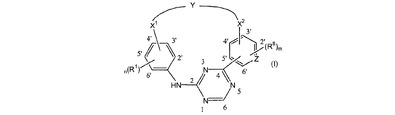
[式中、mは1を表し、nは1を表し、ZはNもしくはC、特にNを表し;−X1−はC1〜4アルキル、特にメチルを表し;−X2−は−C1〜4アルキル−もしくは−C1〜4アルキル−NR7−、特にプロピル、−エチル−NR7−もしくは−プロピル−NR7−を表し;−Y−は−NR2−C1〜6アルキル−CO−NR4−、−Het1−C1〜6アルキル−CO−NR5−もしくは−Het2−CO−NR6−を表し、そしてこここで、−NR2−C1〜6アルキル−CO−NR4−もしくは−Het1−C1〜6アルキル−CO−NR5−の−C1〜6アルキル−リンカーは場合によりヒドロキシ、ハロおよびフェニルから選択される1個または可能な場合には2個もしくはそれ以上の置換基で置換されていてもよく;R1は水素、クロロ、フルオロもしくはブロモを表し;R2は−C1〜4アルキル−、特にエチルもしくはメチルを表し;R7は水素を表し;R8は水素を表し;R4、R5およびR6は水素を表し;Het1はピペラジニルもしくはピペリジニル、特にピペラジニルから選択され;Het2はピロリジニルもしくはピペリジニル、特にピロリジニルから選択され、ここで、該ピロリジニルは場合によりヒドロキシで置換されていてもよい]
の化合物、そのN−オキシド形態、製薬学的に許容しうる付加塩および立体化学的異性体に関する。 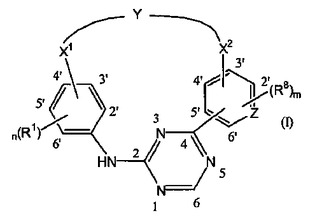 (もっと読む)
(もっと読む)
21 - 40 / 51
[ Back to top ]