Fターム[4C076EE50]の内容
Fターム[4C076EE50]に分類される特許
21 - 40 / 82
ナノバブルの形成方法
【課題】超音波造影剤を用いるナノバブルの形成方法の提供。
【解決手段】本発明はナノバブルの形成方法を開示するものであり、前記形成方法は公知技術に使用する油水乳化反応とは異なる特徴を持つ。本発明のナノバブルの形成方法は、無機粒子を中心核として、前記中心核の表面に最低一つの第一高分子をコーティングして有機/無機複合粒子を形成する。次に、第一溶剤によって前記有機/無機複合粒子の中心核を溶解して除去し溶剤型ナノ粒子を形成する。続いて冷凍乾燥プロセスにおいて前記第一溶剤を除去し前記溶剤型ナノ粒子に中空ナノ粒子を形成させる。最後に前記中空ナノ粒子を第二溶剤に溶かして前記ナノバブルを形成する。
(もっと読む)
重合体−白金化合物
【課題】インビボで抗腫瘍活性を有する新規な重合体−白金化合物を提供すること。
【解決手段】腫瘍の処置で使用する重合体−白金化合物が記述されている。この化合物は、重合体骨格に沿って間隔を置いて配置された白金含有側鎖を有する重合体骨格から構成されている。これらの側鎖は、一端でこの骨格に結合され、そして他端でこの白金化合物に結合されたオリゴペプチドから構成されている。1局面では、本発明は、腫瘍処置で使用するための組成物を包含し、この組成物は、腫瘍部位で蓄積するように設計された重合体−白金錯体化合物を含有する。
(もっと読む)
膨潤性および生分解性を有するポリマーマトリクス並びにその製造方法
本発明は、優れた耐久性および膨潤性を有する生分解性ポリマーヒドロゲルマトリクスを提供する。前記マトリクスは、ポリ−α(1→4)グルコピラノースマクロマー、並びに、生体適合性、生体安定性および親水性を有するマクロマーの組み合わせから形成される。前記マトリクスは、医療デバイスと組み合わせて、または単独で使用しうる。いくつかの方法で、前記ポリマーマトリクスは、標的部位に配置され、または標的部位で形成される。前記マトリクスは、膨潤して標的領域を閉塞し、その後、標的部位で分解されうる。 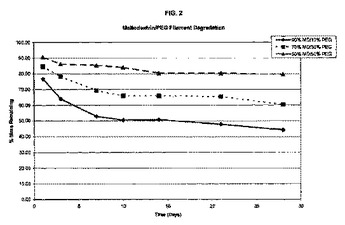 (もっと読む)
(もっと読む)
制御放出系の調製方法
本発明は、制御放出系の調製方法に関し、特に、薬物などの活性成分、好ましくは生物活性成分の制御放出のためにポリマー担体中に化合物を封入するための方法に関する。この方法により、活性成分の制御放出、特に制御された薬物送達のための系がもたらされる。本発明によると、用語「制御放出」は、徐放出、持続放出および遅延放出を含むあらゆる種類の制御放出を包含する。特に、本発明は、制御放出のための、ミセル、ナノ粒子、ミクロスフェアなどのポリマー担体または高分子デバイスおよび他の種類のポリマーデバイスに封入された、または他の方法で組み入れられた、またはそれらに結合した活性成分をもたらす。活性成分は、ポリマー担体または高分子デバイスに共有結合している。 (もっと読む)
特定の分離層を含むオメプラゾールの経口医薬製剤
本発明は、活性成分としてオメプラゾール、オメプラゾールのアルカリ塩、オメプラゾールのエナンチオマー、もしくはオメプラゾールのエナンチオマーのアルカリ塩、並びにポリビニルアルコール/ポリエチレングリコールのグラフト共重合体及び/又は場合により加工されたエンドウ豆デンプンを含む、活性成分と腸溶コーティングとの間の特定の分離層を含む、腸溶コーティング経口医薬製剤に関する。 (もっと読む)
組成物
蜂蜜および超吸収性材料を含んでなる組成物。病巣を治療する方法であって、蜂蜜および超吸収性材料を含んでなる組成物を病巣に適用する工程を含んでなる方法。本発明の組成物を製造する方法であって:(a)少なくとも1つのタイプの蜂蜜を提供する工程;(b)少なくとも1つの超吸収性材料を提供する工程;ならびに(c)蜂蜜と超吸収性材料とを組み合わせる工程を含んでなる、方法。 (もっと読む)
水性液剤
【課題】菌の繁殖が抑制され、コーティング液の調製が簡便であり、さらに添加剤の分散安定性にも優れた水性液剤の提供。
【解決手段】ポリビニルアルコール及びその誘導体から選択される少なくとも1種と重合性ビニルモノマーとを重合して得られるポリビニルアルコール系共重合体を含む水性液剤。好ましくは、上記重合性ビニルモノマーがアクリル酸及びメタクリル酸からなる群から選ばれる少なくとも1種とメタクリル酸メチルを含むものである水性液剤。
(もっと読む)
生体関連物質の非特異吸着防止剤
【課題】蛋白質などの非特異吸着性が少ない生分解性のコーム型ポリマーを提供する。
【解決手段】生体関連物質の非特異吸着防止剤は、生分解性部位を有する主鎖と、低非特異吸着性部位を有する側鎖とを有するコーム型ポリマーを含有する。
(もっと読む)
安定化効果を有する薬物送達システム
薬物送達システムはまた、水溶性の薄いフィルム・マトリックスを含んでなる単位剤形であって、ここで、当該フィルム・マトリックスが、以下の:a)水溶性マトリックスポリマーとしてのポリビニルアルコール‐ポリエチレングリコール・グラフトコポリマー(PVA‐PEGグラフトコポリマー);b)ステロイド骨格の6及び7位が共に‐CH2‐残基であるところのステロイドである有効成分、を含んでなり;且つ、当該フィルム・マトリックスが300μm未満の厚みを持つ単位剤形、としても意図される。 (もっと読む)
グラフト共重合体およびブロック共重合体の多機能混合ミセルならびにその製造方法
【課題】グラフト共重合体およびブロック共重合体に基づく混合ミセルを提供する。
【解決手段】機能性の内部コアならびにグラフト高分子および1以上のブロック共重合体、好ましくはグラフト共重合体および2以上のジブロック共重合体から自己組織化される、親水性の外部シェルを有する、新規の混合ミセルを開示する。グラフト高分子は、骨格構造および前記骨格構造に結合する疎水性側鎖を有し、前記ブロック共重合体は、疎水性重合体セグメントおよび親水性重合体セグメントを有し、この際、前記ブロック共重合体は、親水性重合体セグメントの末端に結合した末端官能基をさらに有する。前記末端官能基は、腫瘍細胞の表面の受容体に結合しうる配位子、蛍光性基または色素である。本発明によって合成されたミセルは、癌の診断薬および癌のドラッグデリバリーの担体として用いられうる、約50〜200nmのサイズを有する。
(もっと読む)
治療薬送達のための可溶性疎水性コア担体組成物、およびその製造・使用方法
本発明は、(i)直鎖高分子主鎖、(ii)直鎖高分子主鎖に共役的に結合し吊り下がった複数の親水性高分子保護鎖、および(iii)直鎖高分子主鎖に共役結合し吊り下がった少なくとも1つの疎水性部分を有する、可溶性の疎水性コア担体組成物に関連する。特定の実施例では、担体中の疎水性部分に対する親水性保護鎖の重量比は少なくとも15:1である。他の実施例では、高分子主鎖残基の少なくとも90%が親水性高分子保護鎖または疎水性部分に結合している。他の実施例では、組成物はさらに(iv)担体の疎水性部分に解離結合した疎水性負荷分子を有する。 (もっと読む)
成形された高分子材料の製造方法
本開示は成形された高分子材料を製造するための方法を記載する。極性溶媒と、極性溶媒に混和性である重合可能な物質とを含有している前駆体組成物から成形された高分子材料を製造するための方法が提供される。前駆体組成物は成形型中で少なくとも部分的に重合させられる。  (もっと読む)
(もっと読む)
膣内薬剤放出システム
本発明は、ドロスピレノンおよびエストロゲンを長時間に亘って制御放出するための膣内薬剤放出システムであって、所望により、細菌および真菌の感染に対する防御性を与える及び/又は高める能力、および、性行為感染症に対する防御性を高める能力からなる群より選ばれる少なくとも1つの能力を有する1種または2種以上の治療的に活性なまたは健康を増進する物質を含有するシステムに関する。該薬剤放出システムは、1つまたは2つ以上のコンパートメント(2、4、5)からなり、各コンパートメントは、芯(7)と該芯を包む膜(3)とを含み、該芯と該膜とは互いに同一または異なる重合体組成物から実質的になる。少なくとも1つのコンパートメントはドロスピレノンを含み、少なくとも1つのコンパートメントはエストロゲンまたはドロスピレノンとエストロゲンとの混合物を含み、エストロゲンまたはドロスピレノンとエストロゲンとの混合物を含む該少なくとも1つのコンパートメントは、ドロスピレノンを含む該少なくとも1つのコンパートメントと同一であっても異なっていてもよい。膜もしくは膜の表面または少なくとも1つの芯は、該治療的に活性なまたは健康を増進する物質を含有する。 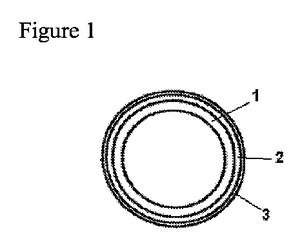 (もっと読む)
(もっと読む)
ラモトリジンの改良製剤
環境のpHと関係なくGI管全体で著しく類似した放出速度を示す、ラモトリジン(lamothgine)の1日1回投与の持続放出製剤を提供する。本製剤は、ラモトリジン、有機酸、放出促進ポリマー及び放出制御ポリマーを含む。神経学的障害を治療する製剤の使用も開示する。 (もっと読む)
不溶性薬剤の制御放出のための、シクロデキストリンおよびポリ(アミドアミン)に基づく超分岐ポリマー
ビスアクリルアミドへのα−、β−またはγ−シクロデキストリンおよびアミンのマイケル型重付加により得ることができる超分岐水溶性ポリマー。 (もっと読む)
微粒子および製造方法
【課題】生理活性物質、薬剤、造影剤、遺伝子等を効率よく封入しうる親水性部分を内部に有し、生体内での安定性向上や体内動態を改善しうる微粒子および製造方法を提供する。
【解決手段】本発明は、両親媒性ポリマーからなる微粒子であって、両親媒性ポリマーの親水性セグメントで形成される内核に親水性ポリマーと親水性ポリマーの架橋成分を含む微粒子である。
(もっと読む)
遺伝子導入剤及びその製造方法
【課題】遺伝子導入効率がさらに向上した遺伝子導入剤及びその製造方法を提供する。
【解決手段】芳香族環を核とし、それから放射状に伸延したカチオン性の複数の分岐鎖を有するスター形分岐型重合体同士が架橋した架橋体よりなる遺伝子導入剤。この遺伝子導入剤は、N,N−ジアルキル−ジチオカルバミルメチル分子団を同一分子内に3個以上有する化合物をイニファターとし、これにビニル系モノマーを光照射リビング重合させたスター形分岐型重合体を架橋処理したものである。固体状態の該分岐型重合体を液状エーテルに浸漬させた状態で光照射することにより、分岐型重合体同士を架橋させる遺伝子導入剤の製造方法。
(もっと読む)
遺伝子導入材
【課題】生体内の特定部位に埋入された後、ベクターが当該部位に留まる遺伝子導入材を提供することを目的とする。
【解決手段】分岐鎖を有するカチオン性ポリマーよりなるベクターと核酸との複合体が、連通性のある多孔質三次元網状構造の合成樹脂よりなる多孔体に保持されてなる遺伝子導入材。分岐鎖を有するカチオン性ポリマーよりなるベクターは、好ましくはベンゼン環に対し3,4又は6分岐鎖が結合したものである。このベクターが核酸と複合体とされ、ソフトセグメント化ポリウレタン製の細棒体に含浸されて遺伝子導入材とされる。核酸はHGF肝細胞増殖因子などである。
(もっと読む)
スフェンタニルおよびナロキソンを含む経口腔投与製剤
本発明は、医薬担体とスフェンタニルとを含む経口腔投与製剤を被験者に投与することと、in vitroドナー媒体試験を用いて決定される、経口腔投与製剤の投与後の投薬期間の間の平均pHを、約3.5〜約5.5の範囲内に保持することと、を含む方法に関する。関連する投与製剤をも開示する。そのほかに開示されるのは、経口腔投与製剤および関連する方法である。ただし、経口腔投与製剤は、(1)約5〜約1000マイクログラムのスフェンタニルと、(2)約50マイクログラム〜約100ミリグラムのナロキソンと、(3)in vitroドナー媒体試験を用いて決定される、経口腔投与製剤の投与後の投薬期間の間の平均pHを、約3.5〜約5.5の範囲内にするのに十分な量の酸性化用材料と、を含みうる。この場合、投薬期間は、経口腔投与製剤の投与後約1分以降に始まり、かつ経口腔投与製剤の投与後約120分以内に終わる。 (もっと読む)
制御された薬物送達のためのテザー基を有するポリマー−薬物コンジュゲート
本発明は、治療薬に共有結合で連結されたポリマー部分を含む新規組成物に関し、この場合、該治療薬は、ポリマー部分にテザーによって連結されている。様々なテザー基および標的化リガンドからポリマーを選択することにより、治療剤の制御送達のための方法を提供する。本発明は、本明細書に記載される治療組成物で被験体を治療する方法にも関する。テザーは、自己環化性部分、例えば、−S−CH2−CH2−CO−、−NR−CH2−CH2−NR−CO−および−S−CH2−CH2−NR−CO−を含む。本発明は、シクロデキストリン系ポリマーを含む薬物コンジュゲートにも関する。  (もっと読む)
(もっと読む)
21 - 40 / 82
[ Back to top ]