Fターム[4C085HH03]の内容
抗原、抗体含有医薬:生体内診断剤 (92,173) | 診断用途 (3,297) | 造影剤 (2,448) | 放射線 (1,001)
Fターム[4C085HH03]に分類される特許
361 - 380 / 1,001
炭酸脱水酵素IXの阻害剤
CA−IXの過剰な発現によって特徴付けられる疾患の診断的画像化及び治療処置に有用である新規な放射性医薬品は、CA−IXの活性な触媒部位に結合し得るスルホンアミド部分、並びに、放射性イメージング及び/又は放射性治療に適した放射性核種を含む錯体を含んで構成される。  (もっと読む)
(もっと読む)
エフリンA型受容体10タンパク質
本発明は、膀胱癌、乳癌、結腸直腸癌、頭頸部癌、腎癌、肺癌若しくは膵癌の治療、スクリーニング、診断及び予後のための、膀胱癌、乳癌、結腸直腸癌、頭頸部癌、腎癌、肺癌若しくは膵癌治療の効果をモニタリングするための、並びに薬剤開発のための、エフリンA型受容体10タンパク質に基づく、方法並びに組成物を提供する。 (もっと読む)
造影剤としてのN−アルコキシアミド抱合体
本開示は、化合物、診断薬、および関連する方法に向けられている。一部の例では、患者を治療する方法が提供される。より具体的には、本開示は、エラスチンに富む組織を検出し、および/または造影し、および/またはモニターするための化合物、診断薬、およびキットを提供する。さらに、本開示は、総血管壁面積、細胞内腔(internal lumen)サイズ、および動脈外周の長さの変化によって示される冠動脈プラーク、頸動脈プラーク、腸骨/大腿動脈プラーク、大動脈プラーク、腎動脈プラーク、いずれかの動脈血管のプラーク、動脈瘤、血管炎、動脈壁の他の疾患、および/または靱帯、子宮、肺もしくは皮膚の損傷もしくは構造変化の存在を検出し、および/または造影し、および/またはモニターする方法を提供する。  (もっと読む)
(もっと読む)
マークされたプリン誘導体の製造方法、該プリン誘導体、およびその使用
【課題】本発明は、2−ニトロプリン誘導体のフッ素化工程を含む、放射性同位体18Fでマークされた2−フルオロプリンの製造方法に関する。本発明は、本発明またはそのさまなざまな使用による方法により得られる、放射性同位体18Fでマークされた2−フルオロプリン誘導体を含む。
【解決手段】本発明の18F放射性同位体でマークされた2−フルオロプリン誘導体の製造方法は、任意に保護された2−ニトロプリン誘導体を、[18F]でマークされたフッ化物イオン源と反応させることを含むフッ素化工程と、任意に続く、脱保護工程とを含む。
(もっと読む)
アミロイドーシスの処置および予防
ネオエピトープ、たとえばAAのC末端領域からのAA断片と、凝集アミロイドタンパク質のネオエピトープに特異的な抗体、たとえばAA原線維のC末端領域に特異的な抗体とを含むペプチドを投与することによって、AAアミロイドーシスおよびALアミロイドーシスを含む、アミロイドーシスの予防または処置を実施するのに有用な方法。患者のアミロイド沈着の形成の抑制および/または排除の増加による、アミロイド疾患の予防の実施またはアミロイド疾患の処置のための抗体。 (もっと読む)
ウイルスに用いる癌の処置および検出方法
【課題】化学療法および放射線照射における最近の進歩に関わらず、癌が死因の上位に
位置する現在において、哺乳動物の癌を処置する方法において、医薬的に許容される担体
中でニューキャッスル病ウイルスの有効量を哺乳動物に投与することからなる方法を提供
すること。
【解決手段】哺乳動物の癌を処置する方法において、医薬的に許容される担体中でニュ
ーキャッスル病ウイルスの有効量を哺乳動物に投与することからなる方法および哺乳類動
物の癌を処置する方法において、ニューキャッスル病ウイルスを他の薬剤と併用し、その
両者をその併用が癌に対して有効である十分な量で哺乳類動物に投与することからなる方
法。
(もっと読む)
腫瘍画像化化合物
【課題】脳および身体の腫瘍の検出および評価に使用する新規のアミノ酸化合物を提供する。
【解決手段】アミノ酸化合物は、インビボで投与される場合、標的部位に、高い特異性を有し、好ましいアミノ酸化合物としては、例えば2-アミノ−3−フルオロ−2−メチルプロパン誘導体で、該誘導体のFが18Fである化合物が挙げられる。さらに、四員環炭素鎖、五員環炭素鎖または六員環炭素鎖のいずれかに結合したα−アミノ酸部分からなる薬学的組成物であり、標識されたアミノ酸化合物は、陽電子放射断層撮影法および単一光子放射型コンピュータ断層撮影法による被験体の腫瘍の検出および/またはモニタリングにおける画像化薬剤として有用である。
(もっと読む)
フィブリンのD二量体断片に特異的なDD−3B6/22から誘導されるヒト化抗体
【課題】
血塊に特異的な抗体であって、ヒトや非ネズミ動物において免疫原性を示さない抗体を提供すること。
【解決手段】
架橋結合したフィブリンを認識するがフィブリノゲンを認識しない、ヒトD二量体上のエピトープに特異的な抗体であって、(i)該抗体の可変(v)領域の一以上のアミノ酸残基をMHCクラスII分子と結合する該v領域のぺプチド断片を消失若しくは減少させるように変異させた脱免疫化抗体、(ii)該ヒト化抗体のv領域の相補性決定領域(CDR)の少なくとも一つがD二量体特異的なモノクローナル抗体に由来し且つ該ヒト化抗体分子の残りの免疫グロブリン由来部分がヒト免疫グロブリンに由来するものであり、そして該ヒト化抗体が可溶性D二量体を用いて選択されるものであるヒト化抗体、及び(iii)架橋結合したフィブリンを認識するがフィブリノゲンを認識しない、(i)又は(ii)の抗体の断片、から選択される抗体を提供する。
(もっと読む)
ベンゾチアゾールおよびベンゾオキサゾール誘導体ならびに使用方法
式(I)の化合物は、ヒスタミン−3受容体リガンドによって予防または緩和される状態または障害の治療に有用である。また、式(I)の化合物の医薬組成物、かかる化合物および組成物の使用方法、ならびに化合物の調製方法が開示される。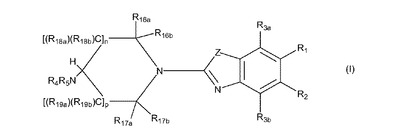
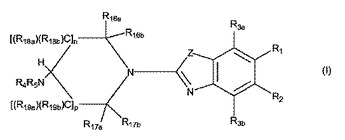 (もっと読む)
(もっと読む)
生体分子の選択的放射性標識
本発明によれば、生体分子上にフッ素原子を導入するための方法であって、(i)チオール反応性末端及びアジド/アルキン反応性末端を含むリンカーを用意する段階、(ii)リンカーのチオール反応性末端を、1以上のチオール基又はその反応性誘導体を含む生体分子と反応させる段階、並びに(iii)次いでリンカーのアジド/アルキン反応性末端をフッ素置換アジド又はアルキン基とそれぞれ反応させる段階を含んでなる方法が提供される。また、二官能性リンカー及びバイオコンジュゲートの組成物及び合成方法並びにフッ素標識生体分子を含む放射性診断剤も提供する。 (もっと読む)
HER2に対する親和性を有する新規なポリペプチド
位置2におけるX1がM、I又はLであり、位置39におけるX2がS又はC(配列番号1)であるアミノ酸配列EX1RNAYWEIA LLPNLTNQQK RAFIRKLYDD PSQSSELLX2E AKKLNDSQを含むHER2結合ポリペプチドが開示されている。更に、キレート環境を含むそのようなペプチドが開示されている。また、キレート環境を含むペプチド及び放射性核種によって形成される、放射性標識されたポリペプチドが開示されている。更に、そのような放射性標識されたポリペプチドの投与と、それに続く医療用画像機器を使った身体の画像の取得を含む、HER2の過剰発現によって特徴付けられるがんを有するか、疑われる哺乳類対象の身体の、インビボ画像化の方法、そしてまたそのような癌の治療方法が開示されている。更に、HER2の過剰発現によって特徴付けられるがんの診断と治療における、そのような放射性標識されたポリペプチドの使用。また、ポリペプチドをコード化する核酸、核酸を含む発現ベクター及び発現ベクターを含む宿主細胞が開示されている。 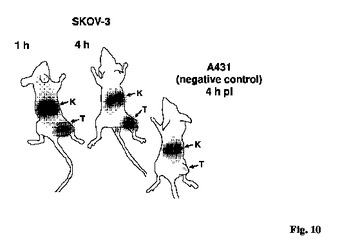 (もっと読む)
(もっと読む)
トランスロケータータンパク質リガンド
本発明は、被験体においてトランスロケータータンパク質(18kDa)(TSPO)発現を画像化する化合物および方法に関する。本発明はまた、被験体における神経変性障害、炎症または不安神経症の治療のための化合物および方法に関する。 (もっと読む)
表面修飾した固体無機/有機ハイブリッド
本発明は、表面修飾した固体有機金属ハイブリッドに関する。該固体は、例えば、活性医薬剤、化粧品における対象化合物およびマーカー、例えば造影剤等の対象分子の封入および方向付けに使用され得る。該固体は、薬剤における充填容量および生体適合性の観点から良好な結果を示す。 (もっと読む)
タンパク質、ペプチド、および他の分子のF−18標識のための改良された方法および組成物
本出願は、例えば、PET画像化技術で有用なF−18標識分子の組成物および合成方法および使用を開示する。特定の実施形態において、標識分子はペプチドまたはタンパク質であってもよいが、アプタマー、オリゴヌクレオチド、および核酸を含むが、これらに限定されない、他の種類の分子を、このような画像化研究のために標識し、利用してもよい。好ましい実施形態において、金属錯体を形成し、このF−18−金属錯体をDOTA、NOTA、DTPA、TETA、またはNETAなどのキレート部分に結合させることによって、F−18標識をターゲッティング分子にコンジュゲートしてもよい。他の実施形態において、金属をまずキレート基にコンジュゲートし、次にF−18を金属にコンジュゲートしてもよい。他の好ましい実施形態において、F−18標識部分は、F−18を疾患、医学的状態、または病原体と関連する細胞または組織に発現した抗原にターゲッティングするために、二重特異性抗体または多重特異性抗体と組み合わせて使用し得るターゲッティング可能なコンジュゲートを含んでもよい。例示的な結果により、F−18標識されたターゲッティング可能なコンジュゲートペプチドが、ヒト血清中、37℃で数時間(PET画像化解析の実施に十分な時間)、安定であることが示されている。 (もっと読む)
核医学診断用医薬
【課題】PBR(末梢性ベンゾジアゼピン受容体)に対して適度な親和性と高い選択性を有する核医学診断用医薬の提供。
【解決手段】下記式(1)で表される放射性ハロゲン標識N−ベンジル−N−(2−(8−オキソ−2−アリール−9H−プリン−9−イル)アセトアミド誘導体。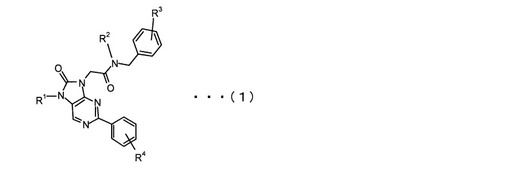
(式(1)中、R1、R2、R3、R4のうちの少なくとも1つは、121I、123I、124I、125I、131I、76mBr、77Br、82Br、34mCl及び18Fから選ばれる放射性ハロゲン原子である。)
(もっと読む)
線維症の非侵襲性の特異的イメージングのための、ポリペプチド、環状ポリペプチドおよびそれを含む医薬
本発明は、画像診断法、特に、線維症の画像診断法に関する。さらに詳しくは、本発明は、線維症の非侵襲性可視化に適した、ポリペプチド、環状ポリペプチドおよび医薬組成物を提供する。本発明のポリペプチドは、X1−X2−M−H−G−L−X7−L−X9−X10−D−E[式中、アミノ酸X1は、R、FまたPであり;アミノ酸X2は、FまたはVであり;アミノ酸X7は、Q、HまたはLであり;アミノ酸X9は、WまたはGであり;アミノ酸X10は、AまたはDである]からなるアミノ酸配列を含み得る。 (もっと読む)
肝臓繊維化レベルの識別方法及びその糖質医学イメージ分子造影剤
【課題】肝臓繊維化レベルを臨床的に精確に識別する方法を提供する。
【解決手段】肝臓標的糖質医学イメージ分子造影法において、
(a)ガラクトースペプチドを含む医学イメージ造影剤を静脈注射し、
(b)特定時間内に医学イメージ器具で単位肝臓体積が発生する医学イメージ信号を測定する。ここで、前記医学イメージ造影剤がTc-99m-SOCTA-galactopeptideまたはTc-99m-DTPA-galactopeptideであり、単光子放射コンピュータ断層測定機器で単位肝臓体積が放出するγ放射量を測定する。または、前記医学イメージ造影剤が磁性造影剤であり、核磁気共鳴機器で単位肝臓体積が発生する電磁信号を測定する。
(もっと読む)
高密度リポタンパク質様ペプチド−リン脂質足場(「HPPS」)ナノ粒子
本発明は、非天然存在高密度リポタンパク質様ペプチド−リン脂質足場(「HPPS」)ナノ粒子を提供する。より詳細には、本発明は:(a)少なくとも1つのリン脂質;(b)少なくとも1つの不飽和脂質、好ましくは不飽和ステロールエステル、さらに好ましくは不飽和コレステロールエステル、さらに好ましくはオレイン酸コレステリル;および(c)少なくとも1つの両親媒性αらせんを形成可能なアミノ酸配列を含む、少なくとも1つのペプチドを含み;構成要素a)、b)およびc)が会合して、ペプチド−リン脂質ナノ足場を形成する、非天然存在ペプチド−脂質ナノ足場を提供する。本発明の態様において、細胞表面受容体リガンドはHPPS内に取り込まれる。1つの態様において、細胞表面受容体リガンドは、HPPSナノ粒子のペプチド足場に共有結合する。他の態様において、細胞表面受容体リガンドは脂質アンカーにカップリングし、そしてHPPSナノ粒子のリン脂質単層内への脂質アンカーの取り込みによってHPPSナノ粒子表面上にディスプレイされる。本発明はまた、HPPSナノ粒子を含む薬学的配合物およびHPPSナノ粒子を作製する方法も提供する。 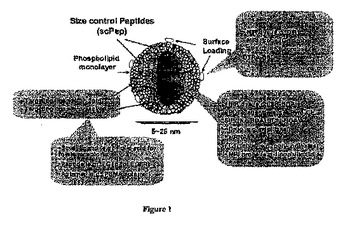 (もっと読む)
(もっと読む)
放射性標識薬剤
【課題】標的に効率的に集積し、かつ、生体内での高い安定性を有する放射性標識薬剤、および該放射性標識薬剤を使用する診断および治療の提供。
【解決手段】標的分子と結合する化合物と結合させた配位子であって金属(例えばテクネチウムやレニウム)と多配位の錯体を形成する配位子と該金属の放射性核種とから形成される錯体を含み、標的部位への集積性が増加した放射性標識薬剤;診断用または治療用の該放射性標識薬剤;前記放射性標識薬剤の調製用配位子;前記配位子を含む薬剤と金属放射性核種を含む薬剤とを、別々の包装単位として含んでなるキット;および、前記放射性標識薬剤を使用することを特徴とする、放射性標識薬剤の標的部位への集積を増加させる方法。
(もっと読む)
新規イメージング法
本発明は、被検体において線維形成の識別を容易にするのに有用な方法に関する。本発明の方法は、肝臓の線維形成を診断するための方法の一部として応用する場合に特に有用である。本発明は、被検体において線維形成を識別するための方法に使用するための化合物も用意する。本発明の別の態様は、被検体において線維形成を識別するための方法に使用するための医薬品の調製に使用するための化合物である。 (もっと読む)
361 - 380 / 1,001
[ Back to top ]



