Fターム[4H006BV62]の内容
有機低分子化合物及びその製造 (186,529) | カルボン酸アミド (2,553) | Cy−CON< (219) | Cy−CON−CR (89)
Fターム[4H006BV62]に分類される特許
61 - 80 / 89
スフィンゴシンキナーゼ阻害剤
本発明は、式(I)の置換アダマンタン化合物、その医薬組成物、それらの製造方法ならびにスフィンゴシンキナーゼの阻害方法および過剰増殖性疾患、炎症性疾患または血管新生性疾患の治療方法または予防方法に関する。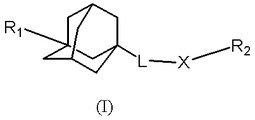
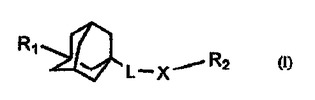 (もっと読む)
(もっと読む)
新規ジベンゾ[B,F]オキセピン−10−カルボキサミドおよびその薬学的使用
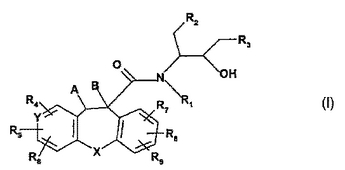
本発明は、式I
【化1】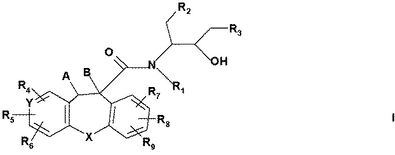
[式中、
Xは、O、NH、N(C1−4)アルキル、COまたはCHOHであり、
Yは、CHまたはNであり、
AおよびBはそれぞれ水素であるか、または一体となって、それらが結合している炭素原子間のもう1つの結合を形成しており、
R1は、水素または(C1−4)アルキルであり、
R2は、所望により置換されていてよい(C1−8)アルキル、(C3−7)シクロアルキル、(C3−7)シクロアルキル(C1−4)アルキル、アリールまたはヘテロアリールであり、
R3は、CH(Re)CONRaRbまたは(CH2)nNRcRdであり、
nは、0、1または2であり、
Ra、Rb、RcおよびRdは、独立して、水素であるかまたは所望により置換されていてよい(C1−8)アルキル、(C3−7)シクロアルキル、(C3−7)シクロアルキル(C1−4)アルキル、(C7−9)ビシクロアルキル、1−アザ−(C7−9)ビシクロアルキル、アリール、アリール(C1−4)アルキル、ヘテロアリール、ヘテロアリール(C1−4)アルキルもしくはヘテロシクリルであるか、または
Ra、Rb、RcおよびRdは、それらが結合している窒素と一体となって、所望により置換されていてよいピロリジニル基、ピペリジノ基、モルホリノ基またはピペラジニル基を形成しており、
Reは、(C1−8)アルキル、(C1−4)アルコキシ(C1−4)アルキル、(C3−7)シクロアルキルまたは(C3−7)シクロアルキル(C1−4)アルキルであり、および
R4、R5、R6、R7、R8およびR9は、独立して、水素、(C1−4)アルキル、(C1−4)アルコキシ、(C1−4)アルキル−SO2、シアノ、ニトロまたはハロゲンである]
で示される化合物;式Iのかかる化合物の製造方法、とりわけベータ−アミロイド生成および/または凝集に関係する神経障害および血管障害の処置における、医薬としてのそれらの使用、および式Iのかかる化合物を含む医薬組成物および組合せに関する。
 (もっと読む)
(もっと読む)
VR1受容体アンタゴニストとしての置換アリールオキソエチルシクロプロパンカルボキサミド化合物
本発明は、式(I)の化合物を提供する。これらの化合物は、哺乳動物において、疼痛など、VR1受容体の過剰活性化に起因する疾患状態の治療に有用である。本発明はまた、上記化合物を含む医薬組成物を提供する。
【化1】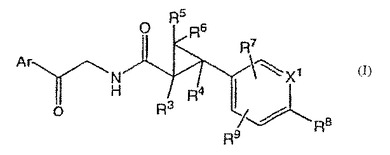
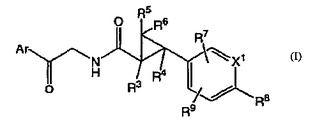 (もっと読む)
(もっと読む)
清涼化合物
身体の皮膚または粘膜へ清涼感を与える方法であって、式I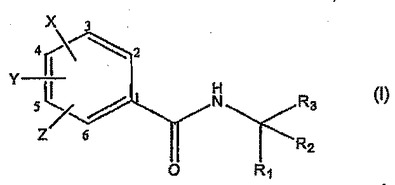
式中、Xは、Hまたは(CH2)n−Rであり、nは、0または1であり、YおよびZは、独立して、H、OH、フェニル、C1〜C4の直鎖もしくは分枝鎖アルキル、またはC1〜C4の直鎖もしくは分枝鎖アルコキシであり、またはXおよびYは、−O−CH2−O−、−N=CH−O−および−N=CH−S−からなる群より選択される2価の基を共に形成し、これらは結合する炭素原子と共に5員環を形成し;および、Rは、非結合電子を有する基であり、R1は、HまたはC1〜C5の分枝鎖アルキルであり、R2およびR3は、C1〜C4の分枝鎖アルキルであり、またはR2およびR3は、R1、R2およびR3が合わせて少なくとも6個の炭素原子を含む条件で、最大10個の炭素原子を有する単環式、二環式または三環式の基を共に形成する、で表される化合物の適用による、前記方法。本化合物は、例えば、歯磨き剤、食料品、菓子類、飲料、化粧品および医薬製剤等の製品中に取り入れてもよい。 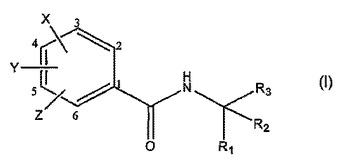 (もっと読む)
(もっと読む)
ヒドロキシビフェニルカルボン酸およびそれらの誘導体、それらの製造方法、ならびにそれらの使用
本発明は、置換されたヒドロキシビフェニル類、それらの誘導体および生理学的に許容できる塩に関する。本発明は、式(I)
【化1】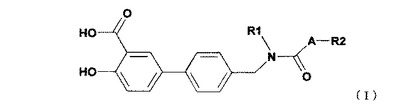
(式中、置換基R1、R2およびAは定義された通り)で示される化合物、それらの生理学的に許容できる塩に関する。本発明の化合物は、例えば血糖降下剤として、さらに、糖尿病の予防および治療に使用するための薬物として適切である。 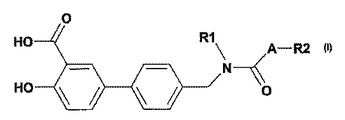 (もっと読む)
(もっと読む)
新規なアダマンタン反応物の製造方法
【課題】フルオロアダマンタン構造を有する新規なアダマンタン反応物の製造方法を提供する。
【解決手段】アダマンタンの水素原子の2〜4個が反応性基(Y)を含有する基に置換され残余の水素原子の1個以上がフッ素原子に置換されたアダマンタン化合物と、Yと反応しうる基(Z)を2個以上有する多官能化合物とを反応させるアダマンタン反応物の製造方法。たとえば、下記化合物(a−1F)と式ClCO−Ph2−COClで表される化合物(ただし、Ph2は1,3−フェニレン基を示す。)を重縮合反応させることにより、ペルフルオロアダマンタン構造と1,4−ジフェニレン基とが、エステル結合で連なった単位を有するポリエステルが提供される。
【化1】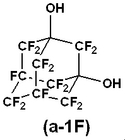 (もっと読む)
(もっと読む)
ケモカイン受容体活性のテトラヒドロピラニルシクロペンチルベンジルアミド調節剤
本発明は、ケモカイン受容体活性の調節剤として有用な式(I)の化合物に関するものである(式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R27、R28、R29、R30、R31、X、m、nおよび点線は本明細書で定義されている)。詳細にはそれら化合物は、ケモカイン受容体CCR−2の調節剤として有用である。
【化507】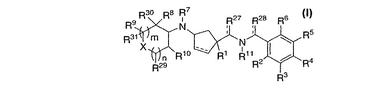
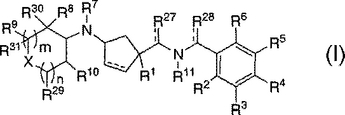 (もっと読む)
(もっと読む)
スピロシクロプロピルアミド及び酸並びに治療へのそれらの適用
本発明は、てんかん、双極性障害、精神疾患、偏頭痛、疼痛、又は運動疾患を治療し、神経を保護するための式(I)の化合物の使用に関する。
【化37】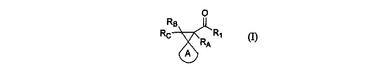
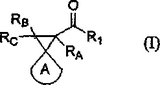 (もっと読む)
(もっと読む)
ジアミノアルカンアスパラギン酸プロテアーゼ阻害剤
現在、式Iのジアミノアルカンが発見され、これらは、経口的に活性であり、それらの活性を阻害するアスパラギン酸プロテアーゼに結合する。それらは、高いレベルのアスパラギン酸プロテアーゼ活性に関連した疾患の治療または改善において、有用である。本発明はまた、それを必要とする被験体におけるアスパラギン酸プロテアーゼ活性関連疾患を改善または治療する際における式Iの化合物を使用する方法に関し、該方法は、該被験体に、式Iの化合物の有効量を投与する工程を包含する。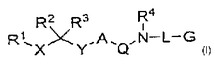
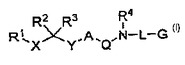 (もっと読む)
(もっと読む)
エンドペプチダーゼ阻害剤としてのシクロペンチル置換グルタルアミド化合物
本発明は、心臓血管障害を処置するためのNEP阻害剤に関する。好適なNEP阻害剤は、式(I)
【化1】
(式中、R1は、C1−C6アルキル、C1−C6アルコキシC1−C3アルキルまたはC1−C6アルコキシC1−C6アルコキシC1−C3アルキルであり;R2は、水素またはC1−C6アルキルであり;Lは、−CH2−X−CH2−および−CH2−CH2−X−より選択される三5原子結合であり、当該結合の右側はR3に結合しており、そしてXは、酸素、硫黄またはメチレンであり;R3は、フェニルまたは芳香族ヘテロシクリルであり、そのどちらも、C1−C6アルキル、ハロ、ハロC1−C6アルキル、C1−C6アルコキシ、ハロC1−C6アルコキシ、C1−C6アルキルチオ、ハロC1−C6アルキルチオおよびニトリルより選択される1個またはそれを超える基で独立して置換されていてよく;そしてR4およびR5は、両方とも水素であるか、またはR4およびR5の一方は水素であり、もう一方は、患者の体内において水素で置き換えられる生体不安定性エステル形成性基である)を有する化合物である。  (もっと読む)
(もっと読む)
ナテグリニドの多形性形状
A、C、D、F、G、I、J、K、L、M、N、O、P、Q、T、U、V、Y、α、β、γ、δ、ε、σ、θ及びΩ形とラベルづけされたナテグリニドの結晶性形状、その調製プロセス及びその他のナテグリニド結晶性形状の調製プロセスが提供されている。同様に提供されているのは、その薬学製剤及び投与方法である。 (もっと読む)
風味組成物において味および風味の増強効果を示す飽和および不飽和N−アルカミド
【課題】食品、チューインガム、医薬品、歯磨き粉、アルコール飲料、水様の飲料、スナック、ソース、もしくはスープの風味を増強する、または5つの基本味特性である甘味、酸味、塩味、苦味、及び旨味の1つもしくは複数の知覚を変更する。
【解決手段】
構造式1及び構造式2:
【化1】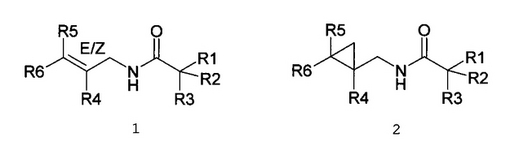
R1;水素又はメチル
R2;水素、C1−C4アルキル、アルケニル、メチレン
R3;水素、C1−C8直鎖又は分岐鎖アルキル、アルケニル、ジエンアルキル、フェニル
R4;水素、メチル、エチル
R5;水素、メチル、エチル
R6;水素、C1−C9直鎖又は分岐鎖アルキル、アルケニル、アルキルジエニル、非環式又は1つだけ環を含む置換基
から成る群より選択される構造式で表されるN置換不飽和アルキルアミド化合物を、
食品、チューインガム、医薬品、歯磨き粉、アルコール飲料、水様の飲料、スナック、ソース、又はスープに添加する。
(もっと読む)
新規な化合物、高分子化合物、レジスト組成物およびレジストパターン形成方法
【課題】 高解像性のレジスト組成物を構成できる高分子化合物、該高分子化合物を製造するのに好適な化合物、該高分子化合物を含有するレジスト組成物、および該レジスト組成物を用いたレジストパターン形成方法を提供する。
【解決手段】 下記一般式(1)で表される化合物[式中、Rは水素原子または低級アルキル基であり;Xは硫黄原子または酸素原子であり;Yは、水素原子の一部がヘテロ原子を含む基で置換されていてもよい炭素数1〜20の鎖状、分岐状または環状のアルキル基、もしくは該アルキル基の炭素原子の一部がヘテロ原子で置換されている基である。]。
【化1】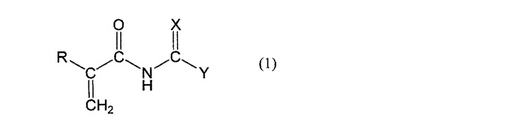 (もっと読む)
(もっと読む)
神経変性疾患の処置のための1−フェニルアルカンカルボン酸の誘導体
本発明は、1−フェニルアルカンカルボン酸の新規な誘導体、それらの製薬学的組成物、それらの製造方法、並びに神経変性疾患、例えばアルツハイマー病の処置および/または予防のためのそれらの使用に関する。 (もっと読む)
(Z)−1−フェニル−1−ジエチルアミノカルボニル−2−ヒドロキシメチルシクロプロパンの製造方法
【課題】 (Z)−1−フェニル−1−ジエチルアミノカルボニル−2−アミノメチルシクロプロパン塩酸塩を製造するための中間体である(Z)−1−フェニル−1−ジエチルアミノカルボニル−2−ヒドロキシメチルシクロプロパンを、簡便な工程で、従来の製造方法よりもより安全かつ安価に、高収率で得ることのできる製造方法を提供すること。
【解決手段】 2−オキソ−1−フェニル−3−オキサビシクロ[3.1.0]ヘキサンとジエチルアミンとを、アルカリ金属アルコキシドの存在下で反応させることを特徴とする、(Z)−1−フェニル−1−ジエチルアミノカルボニル−2−ヒドロキシメチルシクロプロパンの製造方法。
(もっと読む)
p−ヒドロキシ−ミルナシプランの立体異性体およびその使用方法
本発明は、一般的に、パラ−ヒドロキシ−ミルナシプランのエナンチオマーまたはその同種のものに関する。生物学的アッセイによって、ラセミ型パラ−ヒドロキシ−ミルナシプランは、セロトニン摂取およびノルエピネフリン摂取の阻害がほぼ等しい(ノルエピネフリンでは、IC50=28.6nM、セロトニンでは、IC50=21.7nM)ことが明らかになった。興味深いことに、(+)パラ−ヒドロキシ−ミルナシプランは、セロトニン摂取よりもノルエピネフリン摂取をより強く阻害する(ノルエピネフリンでは、IC50=10.3nM、セロトニンでは、IC50=22nM)。対照的に、(−)パラ−ヒドロキシ−ミルナシプランは、ノルエピネフリン摂取よりもセロトニン摂取をより強く阻害する(ノルエピネフリンでは、IC50=88.5nM、セロトニンでは、IC50=40.3nM)。本発明はまた、上記化合物の塩およびプロドラッグ形状にも関連する。いくつかの態様において、本発明の化合物および薬学的に許容される添加剤を組み合わせて、患者に投与するための製剤を調製する。最終的に、本発明は、種々の苦痛、例えば、鬱病、慢性痛、または線維筋痛症を患う哺乳動物を治療するための方法であって、本発明の化合物の治療的有効量を、それを必要とする哺乳動物に投与することを含む方法に関する。 (もっと読む)
抗糖尿病性および抗炎症性を有するコロソリン酸の新規構造類似体
本発明は、式Iの新規コロソリン酸類似体に関する。式中、R1、R2、R3、R4、およびR5は、前記類似体のそれぞれにおいて、以下に示す通りである:1.R1=COCH3、R2=R3=R4=H、R5=COOH、またはR1=R3=R4=H、R2=COCH3、R5=COOH 2.R1=R2=COCH3、R3=R4=H、R5=COOH 3.R1=COC5H4N、R2=R3=R4=H、R5=COOH 4.R1=COCH2NH2・HCl、R2=R3=R4=H、R5=COOH 5.R1=COCH(CH3)NH2・HCl、R2=R3=R4=H、R5=COOH 6.R1=COCH:CHC6H2(OCH3)3、R2=R3=R4=H、R5=COOCH3 7.R1&R2=SO2、R3=R4=H、R5=COOH 8.R1=R2=R3=R4=H、R5=CONH2 9.R1=R2=R3=R4=H、R5=CONHC6H5 10.R1=R2=R3=R4=H、R5=CONHCH2CH2NH2 11.R1=R2=R3=R4=H、R5=CON(CH2CH2)2NH 12.R1=R2=R3=R4=H、R5=CONHCH2CH2OH 13.R1=R2=R3=R4=H、R5=COOCH3 14.R1=R2=COCH3、R3=R4=H、R5=COOCH3 15.R1=R2=H、R3&R4=O、R5=COOCH3 16.R1=R2=COCH3、R3&R4=O、R5=COOCH3 17.R1=R2=H、R3&R4=O、R5=COOH 18.R1=R2=COCH3、R3&R4=O、R5=COOH 19.R1&R2=SO2、R3&R4=O、R5=COOH 20.R1=R2=H、R3&R4=O、R5=CONH2 21.R1=R2=R3=H、R4=OH、R5=CONH2 22.R1=R2=R3=H、R4=OH、R5=COOCH3 23.R1=R2=R3=R4=H、R5=CH2OH 24.R1=R2=R3=R4=H、R5=CHO 25.R1=R2=R3=R4=H、R5=COOCOC6H2(OCH3)3 26.R1=R2=R3=H、R4&R5=OCO。これらの化合物は、優れた血糖降下活性および5−リポキシゲナーゼ抑制活性を示す。これらの化合物はまた腫瘍の成長も抑制する。既知の助剤と表題の化合物とを含む医薬組成物も本発明の範囲内である。
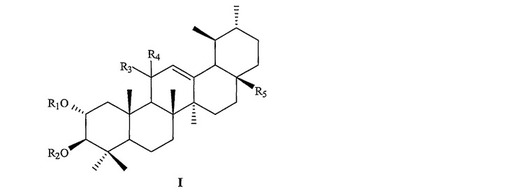 (もっと読む)
(もっと読む)
(Z)−1−フェニル−1−ジエチルアミノカルボニル−2−アミノメチルシクロプロパン塩酸塩の製造方法
【課題】 (Z)−1−フェニル−1−ジエチルアミノカルボニル−2−アミノメチルシクロプロパン塩酸塩を簡便かつ安全に、高品質かつ収率よく製造できる方法を提供すること。
【解決手段】 (Z)−1−フェニル−1−ジエチルアミノカルボニル−2−フタルイミドメチルシクロプロパンを、25重量%以下の濃度のメチルアミン水溶液中で反応させて、(Z)−1−フェニル−1−ジエチルアミノカルボニル−2−アミノメチルシクロプロパンを得る工程を含み、さらに、得られた(Z)−1−フェニル−1−ジエチルアミノカルボニル−2−アミノメチルシクロプロパンを酢酸エチルおよびイソプロピルアルコールの混合溶媒中で塩化水素で処理する工程を含む、(Z)−1−フェニル−1−ジエチルアミノカルボニル−2−アミノメチルシクロプロパン塩酸塩の製造方法。
(もっと読む)
化学化合物および炎症性疾患を処置するためにその化学化合物を含む薬学的組成物
本発明は、式(I)の化合物、あるいはそれらの薬学的に受容可能な塩、溶媒和物または異性体に関し、これらは、MMP、ADAM、TACE、TNF−α、またはそれらの任意の組み合わせにより媒介される疾患または病気の治療に有用であり得る。その多くの実施態様では、本発明は、TACEの阻害剤、TNF−α、MMP、ADAMまたはそれらの任意の組み合わせの産生の阻害剤としての新規種類の化合物、このような化合物を調製する方法、1種またはそれ以上のこのような化合物を含有する医薬組成物、1種またはそれ以上のこのような化合物を含有する医薬処方を調製する方法、およびこのような化合物または医薬組成物を使用してTACE、TNF−α、MMP、ADAMまたはそれらの任意の組み合わせに関連した1種またはそれ以上の疾患を治療、予防、阻止または軽減する方法を提供する。 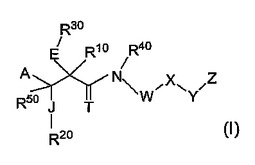 (もっと読む)
(もっと読む)
置換されたシクロヘキシルカルボン酸誘導体
本発明は、置換されたシクロヘキシルカルボン酸誘導体, その製造方法、この化合物を含む医薬及び置換されたシクロヘキシルカルボン酸誘導体を医薬の製造に使用する方法に関する。 (もっと読む)
61 - 80 / 89
[ Back to top ]


