Fターム[4H045EA23]の内容
Fターム[4H045EA23]に分類される特許
21 - 40 / 457
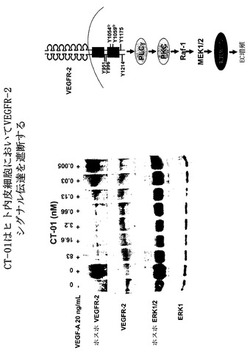
2型血管内皮増殖因子受容体の阻害剤
【課題】新規な血管内皮増殖因子受容体(VEGFR)結合ポリペプチド、および血管内皮増殖因子(VEGF)によって媒介される生物活性を阻害するためのこれらのポリペプチドの使用法、また、単一ドメイン結合ポリペプチドに関する様々な改良を提供する。
【解決手段】VEGFR-2などの標的に結合するポリペプチドであり、標的結合活性は、単一構造ドメイン内に存在する単一ドメインポリペプチド。前記単一ドメインポリペプチドは、免疫グロブリンドメインまたは免疫グロブリン様ドメインである構造単位を含む前記ポリペプチド。
(もっと読む)
小血管の構造および機能を改善するための方法
【課題】小血管の構造及び機能を改善させ、そしてそれにより循環障害に関連する病的状態を緩解する新しい方法の提供。
【解決手段】本発明は最も小型の動脈(即ち小動脈)よりさえも小型の血管が肥厚化し、機能不全となり、そして脳及び腎臓のように多様な組織に対し終末器損傷をもたらすという予測されなかった発見に関する。本発明は小動脈の構造及び機能を改善させ、そして、脳及び腎臓のような終末器の機能を温存するための方法を提供する。この方法は、典型的には、小動脈の構造又は機能を改善させるために十分な用量において本明細書に典型的に記載した活性剤1つ以上をそれを必要とする哺乳動物に投与することを包含する。
(もっと読む)
クリングル配列を有する蛋白質またはペプチドを精製または除去するアフィニティ担体とその精製方法、除去方法。
【課題】プラスミノゲンをはじめとするクリングル配列を有する蛋白質やペプチドを除去または精製するためのアフィニティ担体、及び、そのアフィニティ担体を用いたクリングル配列を有する蛋白質やペプチドの除去方法または精製方法を提供する。
【解決手段】pH9以下で活性化担体とリジンを接触させることによって得たリジンが固定化されたアフィニティ担体は効率良くクリングル配列を有する蛋白質やペプチドを除去・精製可能である。また前記アフィニティ担体を用いたクリングル配列を有するタンパク質またはペプチドの精製方法ならびに除去方法。
(もっと読む)
血管内皮増殖因子の可溶性インヒビターおよびその使用
【課題】可溶性ニューロピリン(sNP)タンパク質、および該タンパク質をコードするcDNAの提供。
【解決手段】VEGF165に特異的に結合し、そしてVEGF165媒介HUVEC増殖を減少させる、単離された可溶性ニューロピリン、NP−1およびNP−2。また、sNPをコードするポリヌクレオチド、および該ヌクレオチドを有する宿主細胞。更に、該sNPを含むVEGF関連疾患用の薬学的組成物。
(もっと読む)
生物活性ナトリウム利尿ペプチドを測定するための、およびその治療可能性を向上させるための方法および組成物
【課題】サンプル中の生物活性ナトリウム利尿ペプチド、またはその断片の存在または量を調べるよう設計された組成物および方法を提供する。
【解決手段】生物活性ナトリウム利尿ペプチドを検出するが、ナトリウム利尿ペプチドの1種以上の生物学的不活性断片からのシグナルは少なくとも5分の1に低下し、好ましくは、これを感知できるほど検出しないアッセイを実施することを含んでなる、サンプル中のナトリウム利尿ペプチドの存在または量を検出する方法、ならびにナトリウム利尿ペプチドの分解のこれまでには未知であった経路を阻害する組成物を提供する。
(もっと読む)
高温安定性酸素担体を含む医薬組成物の製造方法およびその使用
哺乳類における使用に適切な高効率な酸素送達を有し、腎障害および血管収縮の原因とはならない、高温安定性で高精製された架橋化(任意に≧70%β−β架橋化された)された四量体ヘモグロビンが提供される。ヘモグロビンの二量体形態は変性され、精製プロセスが全血からの赤血球において行われる。瞬間細胞溶解装置における制御された低張溶解は白血球の溶解を防止する。白血球からの核酸およびリン脂質不純物は検出されない。スルフヒドリル試薬による反応性スルフヒドリル基の阻害は、酸素化環境において行われる。流液カラムクロマトグラフィは異なる血漿タンパク質不純物を除去する。N−アセチルシステインが架橋四量体ヘモグロビンに対して添加され、低濃度のメトヘモグロビンが維持される。安定化されたヘモグロビンは、アルミニウム上包装を有する注入バッグ中に保存され、酸素の侵入によるメトヘモグロビンの形成を防止する。生成物は組織酸素化および癌治療における使用を提供する。 (もっと読む)
DKK−1に対する抗体
【課題】Dkk−1に選択的に結合する種々の結合剤の提供。
【解決手段】本発明は、Dkk−1ポリペプチド類に特異的に結合する抗体およびその免疫機能性フラグメントを提供する。対象の抗体およびフラグメントは、Dkk−1タンパク質のカルボキシ領域に位置する配座エピトープに高親和性で結合する。このような抗体またはそのフラグメント、ならびに抗体またはそのフラグメントを含有する生理的に受容可能な組成物を調製する方法もまた提供する。骨疾患、炎症性疾患、神経系疾患、眼疾患、腎疾患、肺疾患および皮膚疾患など、種々の疾患を治療するための抗体およびフラグメントの使用法もまた開示する。
(もっと読む)
RFアミド関連ペプチドおよびその方法
非免疫原性ポリマー結合体の調製のための凝集体非含有尿酸オキシダーゼ
【課題】尿酸分解活性を弱めずにウリカーゼ免疫原性を実質的に排除するポリ(アルキレングリコール)−ウリカーゼ結合体を提供する。
【解決手段】八量体より大きい凝集体を実質的に含有しない精製尿酸オキシダーゼ(ウリカーゼ)。ウリカーゼの精製方法であって、八量体より大きいウリカーゼ凝集体を分離する工程と、精製ウリカーゼからこのような凝集体を排除する工程とを包含する。及び前記分離工程が、イオン交換クロマトグラフィー、サイズ排除クロマトグラフィーおよび限外濾過からなる群から選択される。
(もっと読む)
VEGF−CまたはVEGF−D遺伝子またはタンパク質を用いた再狭窄の予防
【課題】血管の狭窄または再狭窄を予防するための被験哺乳類の治療法の提供。
【解決手段】血管内皮増殖因子C(VEGF−C)および/または血管内皮増殖因子D(VEGF−D)遺伝子またはタンパク質を用いた血管の狭窄または再狭窄を予防する材料および方法。
(もっと読む)
CXCR7調節活性を備えたテンプレート固定ペプチド模倣体
一般式(I) 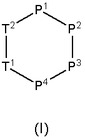
[式中、単一要素TまたはPは、カルボニル(C=O)付着部位から時計回り方向での次の要素の窒素(N)に接続されたα-アミノ酸残基である。]の新規なテンプレート固着β-U字型ペプチド模倣体。ここで、前記要素は、連鎖中のそれらの位置に依存するが、明細書に定義されており、及び、請求項はレセプタCXCR7に作用する特性を有する。従って、これらのβ-U字型のペプチド模倣体は、皮膚科学的病気、代謝病、炎症性疾患、繊維症疾病、感染症、神経学的疾病、心疾患、呼吸器疾患、胃腸管疾患、泌尿器科学的疾病、オフタルミン酸疾病、口腔病学的疾病、血液病および癌の領域の疾病若しくは症状の治療若しくは予防、または幹細胞の動員に役立つことができる。 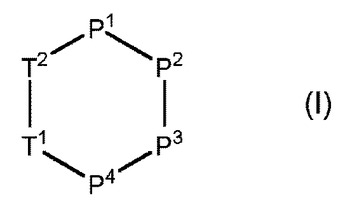 (もっと読む)
(もっと読む)
プロミニン−1の血管新生促進フラグメントおよびその使用
本明細書において記載されるのは、プロミニン−1ペプチドDRVQRQTTTVVA(配列番号1)のペプチドアナログであって、配列番号1のペプチドと比較して、増強された再生および/または血管新生活性を有し、内皮細胞へのVEGFの結合を増大させ、および/または創傷治癒活性を増大させるものである。本明細書において提供されるのは、これらのペプチドアナログを含む融合タンパク質および組成物、ならびにその使用である。  (もっと読む)
(もっと読む)
血管内皮細胞バリアの完全性の保存ための方法及び医薬的組成物
本発明は、血管内皮細胞バリアの完全性の保存及び心筋梗塞を伴うノーリフロー現象における低下における使用のためのANGPTL4ポリペプチドに関する。 (もっと読む)
血漿カリクレイン結合タンパク質
血漿カリクレイン結合タンパク質およびこのタンパク質の使用方法が記載されている。 (もっと読む)
抗Bv8抗体およびその使用
本発明はBv8に対する抗体およびその使用に関する。 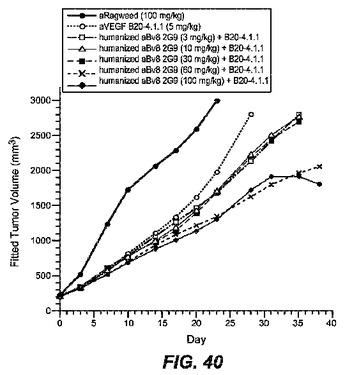 (もっと読む)
(もっと読む)
動脈硬化性関連遺伝子、およびその利用
【課題】動脈硬化性関連遺伝子および該遺伝子の特徴を利用する用途を提供する。
【解決手段】アテローム血栓性脳梗塞をターゲットとした大規模な症例-対照相関研究により、脳梗塞等の動脈硬化性疾患に関連するとして同定された2種の遺伝子上に見出された多型変異を指標とする、動脈硬化性疾患のリスク素因の有無の検査方法。また、該遺伝子の発現もしくは機能を指標とする、動脈硬化性疾患の治療薬のスクリーニング方法。さらに該遺伝子の発現を抑制する、動脈硬化疾患の治療・予防薬。
(もっと読む)
インスリン組成物および組成物の製造方法
【課題】遷延性の作用特性と高い亜鉛含有量を有するアシル化インスリンの製薬学的組成物の提供。
【解決手段】6分子のアシル化インスリン毎に高含有量の亜鉛原子を有するインスリン組成物であり、インスリンはアシル化インスリンである。アシル化インスリンドデカマー複合体もしくはアシル化インスリンドデカマーより高分子量の複合体であってもよい。例えば即効型インスリンAspB28ヒトインスリンのような更なるインスリンアナログと混合されてもよい。
(もっと読む)
GPVIに対する新規アンタゴニスト抗体および該抗体のFabフラグメントならびにこれらの使用
FR2009/113 PCT特許出願 名称 GPVIに対する新規アンタゴニスト抗体および該抗体のFabフラグメントならびにこれらの使用 SANOFI−AVENTIS 要約 本発明は、ヒト血小板膜タンパク質・糖タンパク質VI(GPVI)に特異的に結合する新規抗体および該抗体の一価フラグメントまたは誘導体を開示する。本発明の抗体は、GPVI枯渇表現型を誘導することができる、ハイブリドーマクローン390からの抗体および該抗体のフラグメント抗体である。これらの抗体およびFabフラグメントは、コラーゲン結合を遮断することができ、従って、コラーゲンによる血小板活性化を防止することができる。本発明は、開示する抗体およびFabフラグメントの生産のためのハイブリドーマクローンおよび発現プラスミドにも関する。本発明は、さらに、血栓症および他の血管疾患の治療用の研究、診断および免疫療法薬を製造するための一価抗体フラグメントの使用に関する。本発明は、C末端先端部に分子を有するFabにも関し、およびこのような修飾Fabを使用して抗体によるFabの認識を防止する方法にも関する。本発明は、抗GPVI Fabを使用するときの血小板活性化の防止方法に関する。 (もっと読む)
抗炎症抗体およびその使用
種々の炎症性疾患または障害の治療に用いることのできる補体の活性化を抑制する抗体を提供する。 (もっと読む)
脳梗塞の検査方法
【課題】脳梗塞を簡便で効率よく検査することのできる方法を提供すること。
【解決手段】 被検動物より採取された血液試料中の、α−1アンチトリプシン、α−2マクログロブリン、アポリポプロテイン−A1、アポリポプロテイン−CIII、アポリポプロテイン−H、β−2ミクログロブリン、脳由来神経栄養因子、カルシトニン、癌抗原CA-125、CD40、CD40リガンド、Complement3、クレアチンキナーゼMB、上皮成長因子、ENA-78、エンドセリン−1、EN-RAGE、エオタキシン、エリスロポエチン、FactorVII、脂肪酸結合タンパク質、フェリチン、塩基性線維芽細胞増殖因子、フィブリノゲン、G-CSF、グルタチオン-Sトランスフェラーゼ、成長ホルモン、ハプトグロブリン、IgA、IGF-1、IgM、IL-10、IL-13、L-15、IL-16、IL-1ra、IL-3、IL-4、IL-6、IL-7、IL-8、インスリン、レプチン、MCP-1、MDC、MIP-1α、MIP-1β、MMP-2、MMP-3、ミエロペルオキシダーゼ、PAI-1、PAPP-A、前立腺酸性フォスファターゼ、RANTES、血清アミロイドP、SGOT、SHBG、幹細胞因子、トロンボポエチン、甲状腺刺激ホルモン、TIMP-1、組織因子、TNFレセプターII、TNF-α、VCAM-1、VEGFからなる群から選択される1つ以上の蛋白質量を測定する工程を含む、該動物における脳梗塞の検査方法。
(もっと読む)
21 - 40 / 457
[ Back to top ]