Fターム[4B063QQ21]の内容
酵素、微生物を含む測定、試験 (178,766) | 検体,検出物 (39,509) | 酵素 (3,244)
Fターム[4B063QQ21]の下位に属するFターム
酸化還元酵素(←ペルオキシダーゼ) (623)
転移酵素 (880)
加水分解酵素 (1,188)
リアーゼ(脱離酵素) (67)
イソメラーゼ(異性化酵素) (28)
リガーゼ(合成酵素) (72)
Fターム[4B063QQ21]に分類される特許
321 - 340 / 386
蛍光共鳴エネルギー移動酵素基質
式(I)の化合物が開示されている。
【化1】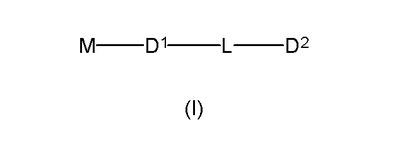
式中、D1は第1の色素部分であり、その蛍光特性は、エネルギー移動構成におけるドナー又はアクセプターとして適するよう調節することができ、D2は、前記第1の色素とのエネルギー移動構成においてアクセプター又はドナーとして適切な第2の色素部分であり、Lは、2〜200個の連結原子を含んでなり、また酵素切断部位を適宜含む連結基であり、Mは、D1の蛍光特性を調節するように選択される酵素切断可能基である。式(I)の化合物は、蛍光共鳴エネルギー移動を利用するアッセイにおいて生化学的切断現象を検出するためのレポーター分子として使用することができる。
(もっと読む)
癌マーカーとしてのSENP1
本発明は、試料中のSENP1および/またはテロメラーゼの量を検出することによる癌細胞の検出方法を提供する。 (もっと読む)
細胞単離方法
本発明は、一般に実質的に均質な未分化細胞集団を生成するための方法に関する。より詳細には、本発明は、実質的に均質な幹細胞、特に哺乳動物幹細胞(MaSC)の集団を単離するための方法に関する。本発明のMaSCは、それらの細胞表面上に存在するタンパク質の示差的レベルに基づいて単離される。本発明のMaSCは、正常および腫瘍組織などであるがそれに限定されない罹患組織の両方におけるMaSC生存率、自己再生、増殖および/または分化を調節する物質を同定するための標的として、さらに疾患もしくは傷害後に損傷を受けたおよび/または消失した組織を再生、置換および/または増強するための組織の起源として特に有用である。 (もっと読む)
マイクロアレイ用の機能性多孔質支持体
本発明は、少なくとも1つの多孔質表面(3,4)を有する少なくとも1つの材料(2)を有しており、前記材料表面の細孔(5)内に分子特異的認識部位を有するナノ粒子(6)が含有される、機能性多孔質支持体(1)に関する。本発明は更に、機能性多孔質支持体の製造方法、この機能性支持体を使用して製造される、マイクロタイタープレート、マイクロアレイ、及び循環装置等の機能エレメント、並びに、機能性支持体及び機能エレメントの使用にも関する。 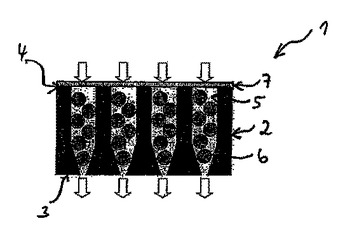 (もっと読む)
(もっと読む)
イヌ寒冷およびメントール感受性受容体1
本発明は、本明細書でイヌCMR1(cCMR1)と命名された新規イヌ寒冷およびメントール感受性受容体を記述する核酸およびポリペプチド配列を提供する。本発明の単離された核酸若しくはポリペプチド分子は、検出アッセイおよびスクリーニングアッセイで使用し得る。 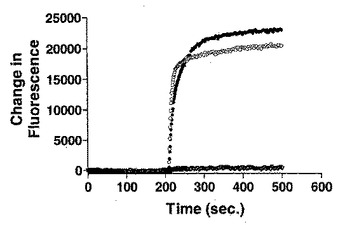 (もっと読む)
(もっと読む)
粒子の誘導アッセンブリーをベースとするバイオセンサー
エフェクター又は補助因子を検出するセンサーシステムは、(a)核酸酵素;(b)第一のポリヌクレオチドを含む、前記核酸酵素の基質;(c)前記基質と少なくとも部分的に相補的である第二のポリヌクレオチドを含む第一の粒子セット(前記ポリヌクレオチドはその3'末端で前記粒子に付着している);及び(d)前記基質と少なくとも部分的に相補的である第三のポリヌクレオチドを含む第二の粒子セット(前記ポリヌクレオチドはその5'末端で前記粒子に付着している)を含む。 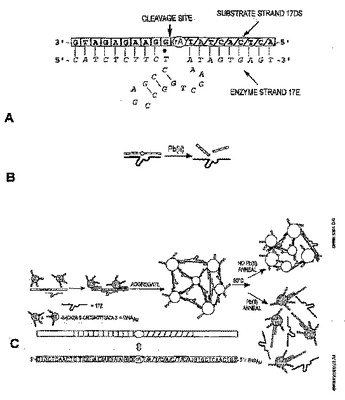 (もっと読む)
(もっと読む)
HAUSP−Mdm2相互作用及びその使用
本発明は、新形成の診断、新形成治療の有効性の評価、新形成罹患対象者の予後評価のための方法を提供する。本発明はまた、新形成の検出で使用されるキットを提供する。本発明はさらに、細胞内でMdm2を脱ユビキチン化及び/又は安定化させる方法、及び細胞内でp53の脱ユビキチン化及び/又は安定性を調節する方法を提供する。さらにまた、本発明は、Mdm2-HAUSP相互作用の調節因子を同定する方法を提供する。さらにまた本方法で同定された調節因子、前記調節因子を含む医薬組成物、および新形成を治療する方法での前記調節因子の使用が提供される。本発明はさらに、Mdm2と反応する作用因子及びHAUSPと反応する作用因子を同定する方法を提供する。さらにまた、これらの方法によって同定された作用因子が提供される。最後に、本発明はMdm2及びHAUSPを含む複合体を提供する。 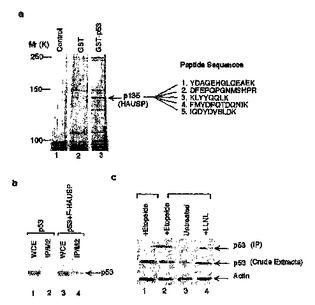 (もっと読む)
(もっと読む)
試料中のPUFA−PKSを同定するためのスクリーニング方法
本発明は、微生物中のPUFA PKSを迅速かつ簡潔に同定するための方法に関する。前記方法は、PUFA(ポリ不飽和脂肪酸)を特異的に生じるPKSを表すDNA部分がin vitroで複製されるという事実を特徴とする。PUFA PKSの特異的アミノ酸配列LGIDSIKRVEILにより、PUFA PKS遺伝子またはPUFA生成微生物の効率的なPCRスクリーニングのために使用されるオリゴヌクレオチドを得ることが可能になる。本発明の方法は、PUFA PKS遺伝子についての微生物のハイスループットなスクリーニングに特に適している。  (もっと読む)
(もっと読む)
非侵襲性生体外機能組織検定システム
基板に一体化された多機能微小電極アレイに基づき、幹細胞技術を実施する機能細胞および組織の検定システム。このシステムにより、通常および病原性特性が網羅される。 (もっと読む)
混合系統キナーゼの阻害およびそのための用途
例えば癌のような新生物形成細胞での細胞増殖を阻害するためのMLKタンパク質若しくはポリペプチドの阻害剤の使用方法が本明細書に提供される。こうした方法は癌を処置するのに使用することができ、かつ、さらに、処置を受領する個体に対する毒性の付随する低減を伴い、癌を処置するための低下された投薬量での抗癌剤の投与と共に使用しうる。MLKタンパク質若しくはポリペプチドの活性を阻害しかつMLK活性を有する新生物形成細胞の細胞増殖を阻害するための阻害剤のスクリーニング方法もまた提供される。 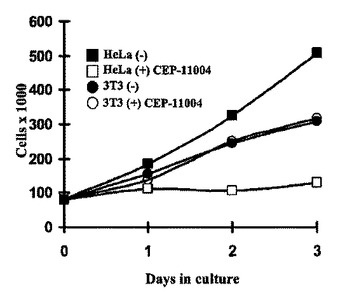 (もっと読む)
(もっと読む)
ヒトBPLPタンパク質由来のペプチド、該ペプチドをコードするポリヌクレオチド及び該ペプチドに対する抗体
本発明は、塩基性のプロリンに富んだ涙液タンパク質(BPLP)の成熟生成物であるペプチド、又は該成熟生成物のペプチド誘導体若しくは模倣体に関し、前記ペプチド又はペプチド誘導若しくは模倣体は、金属−エクトペプチダーゼ、特にNEP及び/又はAPNに対する阻害特性を提示する。本発明はまた、前記ペプチドをコードするポリヌクレオチド、及び前記ペプチドに対する抗体に関する。さらに、本発明は、ヒトBPLPタンパク質及びそれから誘導された阻害性ペプチド、ヒトBPLPタンパク質又はそれから誘導されたペプチドをコードするポリペプチド、並びにBPLPタンパク質又はそれから誘導されたペプチドに対する抗体の診断的及び治療的使用に関する。 (もっと読む)
神経障害性疼痛の代用マーカー
本開示は、神経障害性疼痛ならびに薬物もしくは薬物候補の神経栄養活性あるいは他の活性を評価するための、方法および組成物を提供する。この開示される方法において、皮膚生検試料由来の組織抽出物中のある遺伝子の発現が、関係する最終結果の代理として役立つ。本発明は、皮膚生検試料を非組織学的に、神経障害性疼痛の状態を反映する遺伝子(類)(「神経障害性疼痛代用マーカー」。「損傷・疾患マーカー」とも呼ばれる)の発現に関して評価することができる。 (もっと読む)
フィトクロムと相互結合作用する新規蛋白質及びこれの用途(NOVELPHYTOCHROME−INTERACTINGPROTEINANDAUSETHEREOF)
本発明はフィトクロムと相互結合する新規蛋白質及びこれの用途に関し、より詳しくは配列番号4で表示されるアミノ酸配列又は前記アミノ酸配列と少なくとも70%以上の相同性を有するアミノ酸配列を有するポリペプチド及びこれの用途に関するものである。本発明で提供するポリペプチドはフィトクロムA及びBと交叉相互結合し、前記相互結合にはそのN−末端に存在するTPRドメインが関与する。さらに、前記ポリペプチドのC−末端には、脱リン酸化酵素活性を担当するPP2A触媒ドメイン(PP2Ac)が存在する。本発明に伴うポリペプチドは脱リン酸化酵素として利用することができ、光信号伝達に敏感な植物体の製造に有用に利用できる。さらに、本発明のポリペプチド内に存在するTPRドメインは矮性植物体の製造に利用できる。 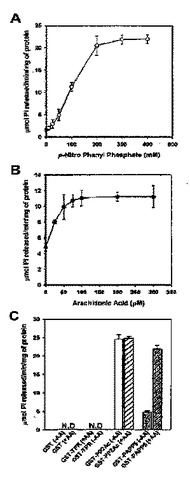 (もっと読む)
(もっと読む)
体細胞核初期化物質のスクリーニング方法
(a) ECAT遺伝子の発現調節領域により発現調節を受ける位置にマーカー遺伝子を存在させた遺伝子を含有する体細胞と被験物質とを接触させる工程、および(b) 前記(a)の工程の後、マーカー遺伝子発現細胞の出現の有無を調べ、該細胞を出現させた被験物質を体細胞の核初期化候補物質として選択する工程、を含む、体細胞の核初期化物質のスクリーニング方法等を提供する。 (もっと読む)
クローン原性内皮前駆細胞の単離、増殖および使用
内皮性コロニー形成細胞(EPC)の階層は、哺乳動物の臍帯血、臍静脈、および大動脈から同定された。高増殖能内皮性コロニー形成細胞(HPP−ECFC)と名付けられた新規に単離された細胞が、単離され、そして特徴付けられた。臍帯血に由来する内皮細胞か、またはHUVECおよびHAECに由来する内皮細胞の増殖能およびクローン原性能を試験する単一細胞アッセイが開発された。EPCは、脈管壁中に常在することが判明している。ヒト臍帯血に由来する高増殖能内皮性コロニー形成細胞(HPP−ECPCS)に由来する細胞の支持細胞層の使用は、再増殖性の造血幹細胞および造血前駆細胞の成長および生存を刺激する。成長および生存の刺激は、インビトロ培養における前駆細胞の数の増加、およびNOD/SCID免疫不全マウス移植系におけるヒト細胞移植のレベルの増加によって決定される。 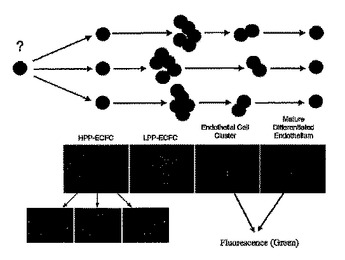 (もっと読む)
(もっと読む)
GPR49の使用による、神経変性疾患の治療
本発明は、神経生成(neurogenerative)疾患治療用の薬剤組成物を調製するためのGPR49相互作用分子の使用に関する。これによって、GPR49相互作用分子は、好ましくはGPR49の阻害剤であり、そして特に、該分子は、ガンマ−セクレターゼおよび/またはベータ−セクレターゼの活性を調節する能力を有する。さらに、本発明は、ガンマ−セクレターゼおよび/またはベータ−セクレターゼの調節剤を同定する方法であって:a.既定の試験化合物がGPR49相互作用分子であるかどうか決定することによって、GPR49相互作用分子を同定し、b.工程a)のGPR49相互作用分子がガンマ−セクレターゼおよび/またはベータ−セクレターゼの活性を調節可能であるかどうか決定する工程を含む、前記方法に関する。 (もっと読む)
免疫応答を誘導または調節する方法
適切には脊椎動物、例えば哺乳動物における、外来または自己いずれであってもよい抗原に対する免疫応答を誘導するかまたは制御するための、MARCH VIIとしても知られる、アキソトロフィンの使用を開示する。単離されたアキソトロフィン、並びにアキソトロフィンにコードされるかまたは由来するヌクレオチドおよびポリペプチド、その1以上を含有する組成物、並びにアッセイ法を、本発明のさらなる側面として提供する。 (もっと読む)
受容体ポリペプチドを有する植物細胞
異種(例えばヒト)受容体ポリペプチドまたはその断片を含む新規なトランスジェニック植物細胞を開示する。これらの植物細胞を使用して、受容体ポリペプチドまたはその断片と相互作用することのできる分子(すなわちリガンド)を同定することが可能である。これらの植物細胞を使用して、トランスジェニック植物細胞に内因性のリガンド、または植物細胞に添加される外因性リガンドを同定することができる。このような受容体ポリペプチドリガンドは新規医薬の同定に使用される。 (もっと読む)
ルミネセンス発生及びルミネセンス非発生多重アッセイ
ルミネセンス発生/ルミネセンス非発生多重アッセイにおける酵素媒介反応に関する少なくとも1種の分子の存在又は量を検出する方法を提供する。 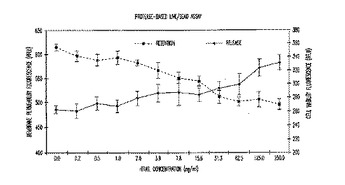 (もっと読む)
(もっと読む)
バイオチップ及びそれを用いた試料溶液の機能性検査方法
血液などの酵素活性や免疫学的特性を網羅的に測定して病理学的診断を行う際のデータの取り扱い性や信頼性に優れ、化学処理が容易でしかも検出部の集積度を高められ微量の検体溶液でも酵素活性及びその傾向を取得できるバイオチップを提供する。
チップ基板11に導入される試料溶液中の酵素を検出するバイオチップであって、全体が渦巻き状やツリー状、放射状などの流路パターンで前記チップ基板上に形成された試料溶液流路12と、試料溶液流路12に所定順で複数配置され所定の酵素に対してそれぞれ異なる活性を有する酵素活性検知部13と、を備える。
(もっと読む)
321 - 340 / 386
[ Back to top ]



