Fターム[4H006AC81]の内容
有機低分子化合物及びその製造 (186,529) | 反応 (20,822) | 不斉合成;不斉保持合成 (948)
Fターム[4H006AC81]に分類される特許
141 - 160 / 948
プロスタグランジン誘導体の製造方法
本発明は、プロスタグランジン誘導体の製造方法及びそのための中間体に関する。本発明によれば、高純度のプロスタグランジンF(PGF)誘導体を、共役付加反応を通じて得られたプロスタグランジンE(PGE)誘導体の保護基をまず除去してから、シクロペンタノン環に存在するケトン基を立体選択的に還元させることにより、効率的かつ経済的に製造することができる。 (もっと読む)
シクロペンタジオン誘導化除草剤
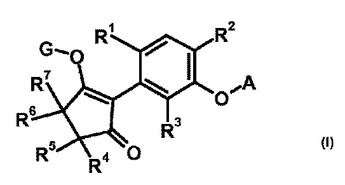
式(I)(式中、置換基は請求項1に規定されるとおりである)の化合物は除草剤としての使用に適切である。
 (もっと読む)
(もっと読む)
ワインラクトンの製造方法
【課題】
取り扱いに厳重な注意を有する危険な試薬、環境に負荷をかける重金属試薬、極度な低温条件などを必要としない簡便な方法で、工業的に、天然型ワインラクトンを豊富に含むワインラクトンを高純度かつ高収率で得る方法を提供すること。
【解決手段】
3−メチルブタ−1,3−ジエン−1−イル 2−メチル−3−ブテノエートを分子内ディールス・アルダー反応を行うことを特徴とする、ワインラクトンの製造方法。
(もっと読む)
光学活性含フッ素アルキニル化生成物の製造方法
【課題】重要な医農薬中間体に成り得る光学活性含フッ素アルキニル化生成物の実用的な製造方法を提供する。
【解決手段】含フッ素α−ケトエステルとシリルアセチレンを「光学活性な配位子を有する遷移金属錯体」の存在下に反応させ、引き続いて加水分解することにより光学活性含フッ素アルキニル化生成物を製造することができる。
本発明の製造方法は触媒的な不斉合成法であり、さらに、目的とする光学活性含フッ素アルキニル化生成物が収率良く極めて高い光学純度で得られる。また、プロパルギル位に水素原子を有するシリルアセチレンを用いても、所望のアルキニル化生成物のみが選択的に得られる。よって、化学純度の高い生成物を得ることができる。
この様に、本発明は、重要な医農薬中間体に成り得る光学活性含フッ素アルキニル化生成物の実用的な製造方法を提供するものである。
(もっと読む)
光学活性コンボルタミジン誘導体の製造方法
【課題】種々の生理活性を有することが期待される光学活性コンボルタミジン誘導体の実用的な製造方法を提供する。
【解決手段】イサチン類とケテンシリルアセタールを「光学活性な配位子を有する遷移金属錯体」の存在下に反応させ、引き続いて加水分解することにより光学活性コンボルタミジン誘導体を製造する。
本発明において、イサチン類とケテンシリルアセタールの不斉触媒による炭素−炭素形成反応が良好に進行することを見出した。さらに、目的とする光学活性コンボルタミジン誘導体が収率良く高い光学純度で得られる、好適な不斉触媒および反応条件を明らかにした。本発明によれば、分離の難しい不純物が含まれず、化学純度の高い生成物を得ることができる。本発明で得られる光学活性コンボルタミジン誘導体は、導入された炭素求核部位の多様な官能基変換反応が可能であり、構造活性相関に必要な多種の誘導化に好適に利用できる。
(もっと読む)
ケトンの立体選択的水素化
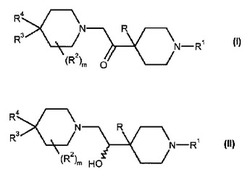
本発明の方法は、化学式Iのケトンを還元するステップを含む方法であって:
化学式IIの実質的にエナンチオピュアなアルコールを形成するため、エナンチオ選択性の水素化剤によってなされ: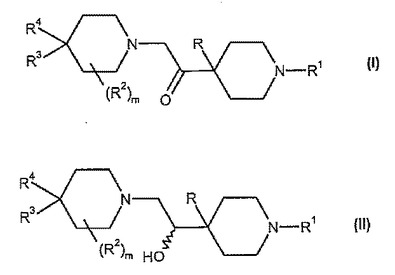
式中のR−R4およびmは、本明細書中で定義されるとおりである、方法に関する。本発明の方法は、CCR2モジュレータおよびCCR2モジュレータの前躯体の製造に有用である。
(もっと読む)
アミノオキシ化合物の製造方法
【課題】環境負荷が少なく且つ工業的に有利な方法で、アミノオキシ化合物を高収率で製造でき、光学純度が高い光学活性なアミノオキシ化合物も製造できる方法の提供。
【解決手段】下記一般式(1)で表されるニトロソ化合物と、下記一般式(2)で表されるスズエノラート化合物とを、下記一般式(3)で表されるピラジン誘導体と銀化合物との錯体の存在下で反応させることを特徴とする下記一般式(4)で表されるアミノオキシ化合物の製造方法。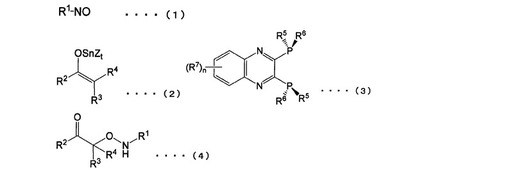 (もっと読む)
(もっと読む)
シナカルセト塩酸塩の製造方法
式(I)で表されるN−[(11R)−1−(1−ナフチル)エチル]−3−[3−(トリフルオロメチル)−フェニル]プロパン−1−アミン塩酸塩(すなわち、シナカルセト塩酸塩)及び式(VII)及び(VIII)(式中、Zは塩化物イオン又は他の薬学的に許容され得るアニオン性対イオンである)で表されるその中間体の製造方法。
【化1】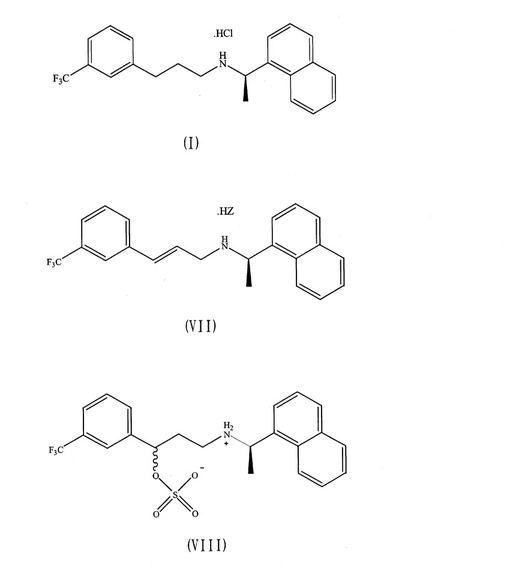 (もっと読む)
(もっと読む)
3,3−ジフェニルプロピルアミン類の新規誘導体の安定な塩
【課題】 塩の形態での3,3−ジフェニルプロピルアミン誘導体の高純度で、結晶性の安定な化合物、その製造方法、ならびに高純度で安定な中間体生成物を提供する。
【解決手段】 3,3−ジフェニルプロピルアミン類のフェノールモノエステル類を提供する。好適な化合物は、R−(+)−2−(3−ジイソプロピルアミノ−1−フェニルプロピル)−4−ヒドロキシメチルフェニルイソブチレートエステルのフマル酸水素塩および塩酸塩水和物である。結晶性中間体生成物のうち好適なものは、R−(−)−3−(3−ジイソプロピルアミノフェニルプロピル)−4−ヒドロキシ安息香酸メチルエステルである。
(もっと読む)
S1P受容体アゴニストおよびアンタゴニストを調製するための方法
本明細書において開示されているのは、S1P受容体ファミリーの1つまたは複数の各受容体のアゴニストまたはアンタゴニストである化合物を製造する方法である。 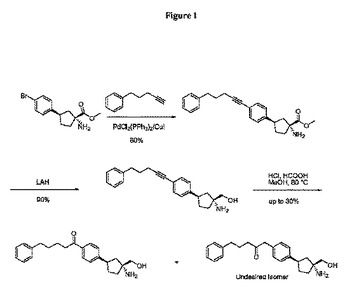 (もっと読む)
(もっと読む)
エナミノカルボニル化合物およびその使用
本発明は、式(I)のエナミノカルボニル化合物(式中、XはOまたはCH2を表し、YがNを表し、R1およびR2がそれぞれ水素であるか、あるいはYがCHを表し、R1またはR2のいずれかがC1〜4アルキルを表し、残りのR1またはR2が水素を表すかのいずれかであり、YがCHを表し且つR1またはR2がC1〜4アルキルである場合には、R鏡像体またはS鏡像体のいずれかに富むRおよびS鏡像体混合物、R鏡像体、ならびにS鏡像体からなる群から選択される)に関する。本発明は、式(I)の化合物(式中、XがOまたはCH2を表し、YがCHを表し、R1またはR2のいずれかが水素およびC1〜4アルキルからなる群から選択され、残りのR1またはR2が水素を表す)の、製品および/または経口投与用製剤の味を修正するための使用にも関する。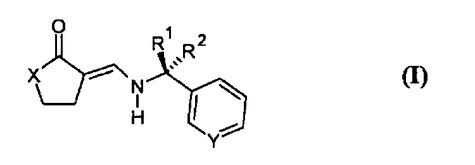
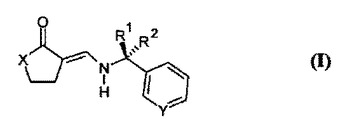 (もっと読む)
(もっと読む)
(1S,2R)−ミルナシプランの合成方法
本発明は、(1S,2R)−ミルナシプランの薬学上許容される酸付加塩の合成方法であって、下記の一連の工程:(a)フェニルアセトニトリルと(R)−エピクロルヒドリンを、アルカリ金属を含有する塩基の存在下で反応後、塩基性処理を行い、次いで酸性処理を行い、ラクトンを得る工程、(b)該ラクトンを、ルイス酸−アミン複合体の存在下でMNEt2(ここで、Mはアルカリ金属を表す)またはNHEt2と反応させてアミド−アルコールを得る工程、(c)該アミド−アルコールを塩化チオニルと反応させて塩素化アミドを得る工程、(d)該塩素化アミドをフタルイミド塩と反応させてフタルイミド誘導体を得る工程、(e)該フタルイミド誘導体のフタルイミド基を加水分解して(1S,2R)−ミルナシプランを得る工程、および(f)(1S,2R)−ミルナシプランを好適な溶媒系で、薬学上許容される酸の存在下で塩化する工程を含んでなる方法に関する。 (もっと読む)
配位子
配位子として働き、金属錯体を形成することのできる、かご型ホスフィン生成物を提供する。この金属錯体は触媒として使用することができる。かご型ホスフィンは、式(I)の化合物又はその塩である:
【化1】
(式中、R1基及びR8基は各々独立して、(a)無置換;(b)オキシド置換基 =O;(c)スルフィド置換基 =S;(d)セレニド置換基 =Se;(e)C1〜C8アルキル置換基;(f)C6〜C8アリール置換基、若しくは5員環〜8員環のヘテロアリール置換基;又は(g)ルイス酸置換基を表し、R2基、R3基、R4基、R5基、R6基及びR7基は各々独立して、(1)無置換;(2)水素置換基;(3)C1〜C8アルキル置換基;(4)C1〜C8アルコキシ置換基;又は(5)C1〜C8アシル置換基を表し、かつXは、(i)C1〜C12アルキレン連結基;(ii)エーテル連結基;(iii)C2〜C6アルケニレン連結基;(iv)エステル連結基;(v)(ヘテロ)アリーレンリンカー;(vi)アミンリンカー;又は(vii)チオエーテルリンカーから選択される連結基を表す)。  (もっと読む)
(もっと読む)
トランス体構造を有する環状脂肪族ジアミンの製造方法
【課題】ポリウレタン樹脂やポリアミド樹脂のモノマー原料および医農薬原料の中間体として有用な、トランス体構造を有する環状脂肪族ジアミンの製造方法を提供する。
【解決手段】トランス体構造及びシス体構造からなるジハロゲン化物をアンモニアでアミノ化する下記一般式(2)で表されるトランス体構造を有する環状脂肪族ジアミンの製造方法であって、アミノ化時にシス体構造を有するジハロゲン化物1モルに対して塩基性化合物を1.0〜10.0モル使用する。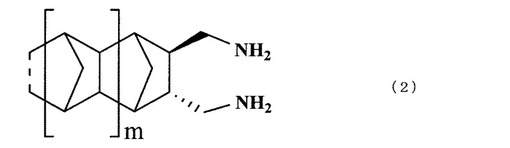
(式中、点線は単結合又は二重結合を表し、mは0又は1を表す。)
(もっと読む)
JAK阻害剤および関連中間化合物の製造方法
本発明は、式IIIのキラル置換ピラゾリルピロロ[2,3−di]ピリミジンおよび関連合成中間化合物の製造方法に関する。キラル置換ピラゾリルピロロ[2,3−d]ピリミジンは、炎症性疾患、骨髄増殖性障害および他の疾患の治療のためのヤヌスキナーゼファミリーのタンパク質チロシンキナーゼ(JAK)の阻害剤として有用である。  (もっと読む)
(もっと読む)
不斉水素化によるキラルなベータアミノ酸誘導体の製造方法
【課題】キラルなフェロセニルジホスフィン配位子と錯形成した遷移金属前駆体の存在下、プロキラルなベータアミノアクリル酸誘導体のエナンチオ選択的水素化により得た生物活性分子の不斉合成に有用なエナンチオマー富化ベータアミノ酸誘導体の提供。
【解決手段】下記式で表される(2R)−4−オキソ−4−[3−(トリフルオロメチル)−5,6−ジヒドロ[1,2,4]トリアゾロ[4,3−a]ピラジン−7(8H)−イル]−1−(2,4,5−トリフルオロフェニル)ブタン−2−アミン。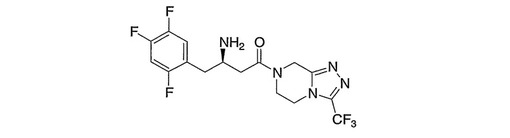 (もっと読む)
(もっと読む)
光学活性なジアミン誘導体およびその製造方法
【課題】国際公開第01/74774号パンフレットに開示されているプロセス問題点を解決し、化合物(VI−I)の工業的製造方法を提供する。
【解決手段】
式(VI−I)
(式中、R1は炭素数2〜7のアルコキシカルボニル基を示し、R3はジメチルカルバモイル基を示す。)
で表される化合物のマレイン酸塩、フマル酸塩、シュウ酸塩又はトシル酸塩。
(もっと読む)
水素移動反応を使用する光学活性化合物の調製の方法
光学活性化合物の調製のための接触法、および所望の製剤原料へのそれらのその後の変換。特に、この方法は、不斉接触還元および水素移動反応を使用する(S)−3−(1−ジメチルアミノ−エチル)−フェノールの調製に関するものであり、それによってリバスチグミンおよびリバスチグミン酒石酸水素塩などの製剤原料を形成する改良された経路を提供する。 (もっと読む)
キラルな配位子
光学的に純粋又は光学的に非常に富化された、式(1)[ここで、R0は、C1−C12−アルキル(非置換であるか、又は1〜2個のC1−C4−アルコキシで置換されている);シクロペンチル又はシクロヘキシル(非置換であるか、又は1〜3個のC1−C4−アルキルもしくはC1−C4−アルコキシで置換されている);あるいはベンジル、フェニル又はナフチル(非置換であるか、又は1〜3個のC1−C4−アルキル、C1−C4−アルコキシ、C1−C4−フルオロアルキルもしくはC1−C4−フルオロアルコキシ、F又はClで置換されている)であるか、あるいは、R0は、−CR5R6OH又は−CR5R6OSi(C1−C8−アルキル)3(ここで、R5及びR6は、H、非置換C1−C12アルキル、置換C1−C12アルキル、非置換C4−C8シクロアルキル、置換C4−C8シクロアルキル、非置換アリール、置換アリールからなる群より独立して選択されるか、又はR5及びR6は、非置換5〜6員脂肪族炭素環又は置換5〜6員脂肪族炭素環を形成することができる)であり、各々R1及びR’1は、独立して、水素であるか、又はR0の意味を有し、R1、R’1及びR0は、同じであるか異なっていることができ、R2及びR3は、独立して、C−結合炭化水素基又はヘテロ炭化水素基であり、そして各々両方のR4は、C1−C6−アルキル、シクロペンチル、シクロヘキシル、フェニル、メチルフェニル、メチルベンジル又はベンジルであるか、あるいは両方のR4は一緒になって脂肪族C4−C6炭素環を形成する]のキラルな化合物。これらの配位子の金属錯体は、不斉付加反応、特に水素化のための、均一系触媒である。 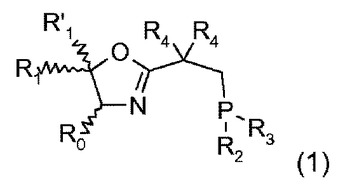 (もっと読む)
(もっと読む)
HCVのマクロ環状プロテアーゼ阻害剤を製造するための方法および中間体
【化1】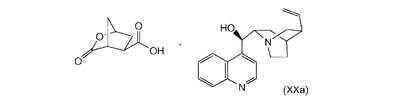
本発明は、マクロ環状HCV阻害剤を製造するための中間体の製造において有用なシンコニジン塩、ならびにこの塩を必要とする方法に関する。 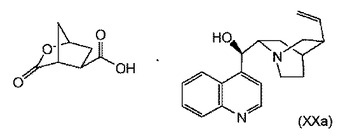 (もっと読む)
(もっと読む)
141 - 160 / 948
[ Back to top ]