Fターム[4H045BA01]の内容
Fターム[4H045BA01]に分類される特許
61 - 80 / 119
アルファ−シヌクレイン凝集の阻害
本発明はペプチジル化合物を用いたα−シヌクレイン凝集の阻害に関し、そのペプチジル化合物α−シヌクレイン配列のレトロエンチオマー、特に1から60の残基又は61から96の残基の間の領域内の配列のレトロエンチオマーである。本発明のペプチジル化合物を、必要に応じてドパミン作動性標的化部分(moiety)、及び/又は、血液脳関門輸送部分と連結してもよく、パーキンソン病などのα−シヌクレイノパチーの治療において有用でありうる。 (もっと読む)
改良型抗菌ペプチド
本発明は、網の末端又はカルボキシ末端に結合された約2〜約36のアミノ酸残基又はそのアナログを有するアミノ酸残基の第一セット、及び3〜8の疎水性アミノ酸残基又はそのアナログを含む大にセットを含む抗菌ペプチドに関し、ここで当該ペプチドは、抗菌活性を有する。 (もっと読む)
ペプチドを含むインテグリン結合モチーフと骨疾患の治療法
【課題】骨格系疾患の治療に有用なペプチドおよびその製剤を提供する。
【解決手段】10〜50 アミノ酸を含むペプチド配列を開示する。この配列は、RGD配列などのインテグリン結合モチーフ、グリコサミノグリカン結合モチーフ、およびカルシウム結合モチーフの少なくとも一つを含み、基質細胞外リン糖タンパク質のRGD配列に隣接する残りのアミノ酸を含むことを特徴とする。これらの配列は、注射用に製剤化することができるほか、練り歯磨きもしくは口内洗浄剤、または歯肉パッチ中に分散させることが可能であり、これを投与することで骨/歯の成長を促したり、および/または体内から尿中へのリン酸塩の過剰な喪失を抑えたりすることができる。
(もっと読む)
昆虫抗微生物タンパク質改変ペプチド、およびその利用
【課題】本発明は、D型アミノ酸からなる昆虫抗微生物タンパク質改変ペプチドを提供することを課題とする。また、該ペプチドを対象に投与する工程を含む、細菌感染症または癌疾患を予防または治療する方法の提供を課題とする。さらに、該ペプチドを有効成分とする、細菌感染症または癌疾患を予防または治療する薬剤の提供についても課題とする。
【解決手段】本発明者らは、上記の課題を解決するために、L型およびD型改変ペプチドの静脈内投与が、MRSA感染症制御に及ぼす効果、TNF-α抑制効果、エンドトキシンショック防御効果、トリパノソーマ原虫のin vitro増殖に対する効果、および癌細胞増殖に対する効果について検討を行った。その結果、D型アミノ酸からなる昆虫抗微生物タンパク質改変ペプチドが様々な細菌感染症または癌疾患に対して効果を示すことを見出した。
(もっと読む)
生理的機能の測定方法
【課題】体細胞の生理的機能の測定方法を提供する。
【解決手段】一群の体細胞の生理的機能を測定する方法は、測定可能な電磁線を発光し得る検出可能作用物質を選択する工程を含む。作用物質は、一群の身体細胞に接触する体液中に導入される。発光を測定し、発光の測定値を基礎にして生理的機能を確定する。
(もっと読む)
ペプチド誘導体
【課題】優れた鎮痛作用を有し、その作用の持続性に優れた新規なオピオイド様ペプチド誘導体を提供する。
【解決手段】下記式(1)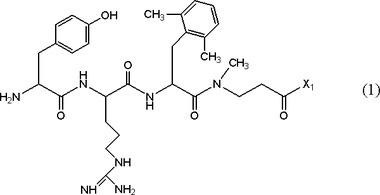
で表されるペプチド誘導体またはその薬学的に許容される塩。(式中、アルギニン残基はD体であり、チロシン残基および2’,6’−ジメチルフェニルアラニン残基はL体であり、X1は水酸基またはアミノ基を表す)
(もっと読む)
腫瘍成長の阻害
本発明は、癌の治療およびワクチン接種の方法だけでなく、腫瘍の成長または成立(establishment)に対する適応免疫を対象に誘導する医薬の製造における、溶解性化合物、特に、溶解性ペプチドの使用を提供する。  (もっと読む)
(もっと読む)
金属イオン結合能およびナノチューブ形成能を有する環状ペプチドと、それを用いたペプチドで構成されるナノチューブ、並びにそれらの製造方法。
【課題】規則的な微細構造で中空構造を有するナノメートルスケールのナノチューブを形成する新規環状ペプチドの配列、当該配列を成す物質のナノチューブ形成条件を提供する。
【解決手段】環状ペプチドの環内部に金属イオンを配位させるため、3残基連続して同じ光学異性体が並んだ領域を2つ連続せずに配置し、それ以外のアミノ酸はL−体とD−体が交互に配された配列を持たせることにより、3残基の真ん中のアミノ酸は環内部を向き、その位置に金属イオンと配位結合するHis、Aspなどのアミノ酸を設定するように設計する。環状ペプチドは特定条件下で自己組織化的に会合し、金属イオンを環内部に配位させながらナノチューブを形成するため、ナノチューブ内に一次元的に金属イオンを配列化させることができることで、機能的なナノ素材、ナノ材料へ応用が可能である。
(もっと読む)
IgGのFcRNへの結合をブロックするペプチド
本発明は、ヒトFcRnに結合してFcRnへのIgGのFc部分の結合を阻害し、それにより、血清IgGレベルを調整するペプチドに関する。開示の組成物および方法を、例えば、自己免疫疾患および炎症性障害の治療で使用することができる。本発明はまた、本発明のペプチドの使用方法および作製方法に関する。本発明は、FcRnに特異的に結合してFcRnへのIgG Fcの結合を阻害し、それにより、リソソームによる分解からIgGを防御する役割でFcRnが機能するのを妨害することによってIgGが再利用されるのを防止するペプチドを提供する。例示的実施形態では、ペプチドは、FcRnに結合してFcのIgG1、IgG2、IgG3、またはIgG4サブクラスのFcRnへの結合を阻害する。  (もっと読む)
(もっと読む)
テンプレート固定ペプチド擬似体
一般式(I)[式中、Zは12個のα−アミノ酸残基のテンプレート固定鎖であり、これらのアミノ酸残基は、鎖中の残基の位置(N末端アミノ酸から開始して数えた位置)に応じて、Gly、もしくはProであるか、または特定のタイプの残基であり、上の式中の残りの記号と同様に、本明細書および特許請求の範囲に定義されている]で表わされるテンプレート固定β−ヘアピンペプチド擬似体およびその塩は、シュードモナス・アエルギノーザ[Pseudomonas aeruginosa](緑膿菌)のような微生物の増殖を選択的に阻害する、またはそれを殺す特質を有する。これらは、食品、化粧品、医薬品、および他の栄養素含有材料用の殺菌薬として、または感染を治療または予防するための医薬として用いることができる。こうしたβ−ヘアピンペプチド擬似体は、混合型固相・液相合成法に基づいた方法により製造することができる。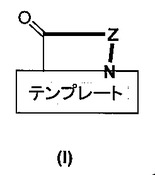 (もっと読む)
(もっと読む)
非天然アミノ酸およびポリペプチドを含んでいる組成物、それらに関する方法、ならびに、それらの使用
本明細書には、非天然アミノ酸を少なくとも1つ含んでいる非天然アミノ酸ポリペプチド、および当該非天然アミノ酸ポリペプチドを作製する方法が記載されている。非天然アミノ酸は、それ自体またはポリペプチドの一部であるとき、機能性基として可能な多様なものを含むことができるが、通常は少なくとも1つのヘテロ環基、アルドールに基づく基、ジカルボニル基、および/またはジアミン基を有することができる。また、本明細書には、さらに翻訳後修飾された非天然アミノ酸ポリペプチド、上記修飾をするための方法、ならびに上記ポリペプチドを精製する方法も開示されている。通常、修飾型非天然アミノ酸ポリペプチドは、少なくとも1つのヘテロ環基、アルドールに基づく基、ジカルボニル基、および/またはジアミン基を含んでいる。さらに、上記非天然アミノ酸ポリペプチドおよび修飾型非天然ポリペプチドを使用する方法(治療的使用、診断的使用、および他の生物工学的使用など)が開示されている。 (もっと読む)
ヒスチジン含有ジアステレオマーペプチド及びその使用
少なくとも13アミノ酸残基を有し、ヒスチジン及び1つ又は複数の疎水性アミノ酸残基を含み、C末端でエステル化若しくはアミド化及び/又はN末端でアシル化されていてもよく、正味の正電荷が+1を超えるジアステレオマーペプチド及びその環状誘導体を提供する。上記ペプチドは、非天然アミノ酸を含めた他のアミノ酸残基を含有していてもよい。上記ペプチドは癌の治療に特に有用である。 (もっと読む)
神経変性疾患の治療
配列D-Arg-L-Glu-L-Argまたは配列L-Arg-D-Glu-L-Argを有するペプチド、及びそれらの誘導体を開示する。そのようなペプチドは、神経変性疾患の治療において、並びに向知性薬として有用である。好ましいペプチドは、保護基を含む。 (もっと読む)
ペプチダーゼに対する耐性が向上しているGLP−1(グルカゴン様ペプチド−1)融合ペプチド
本発明は、GLP−1活性を有しており、インビボにおける安定性が向上している(特にジペプチジルペプチダーゼIVに対して耐性がある)融合ペプチドを提供する。前記融合ペプチドは、構成要素(I)として、N末端にGLP−1(7−35、7−36または7−37)の配列、および構成要素(II)として、C末端に少なくとも9アミノ酸のペプチド配列、またはその機能的な断片、変異体もしくは誘導体を含んでいる。構成要素(II)は、完全または部分的なIP2(介在性ペプチド2)であることが好ましい。好ましい実施の形態は、GLP−1(7−35、36または37)/IP2/GLP−1(7−35、36または37)またはGLP−2の配列を含んでいる。融合ペプチドは、組み換え細胞において、または合成的に生産されていてもよいし、様々な病気または疾患(例えば、1型糖尿病または2型糖尿病、アポトーシスが関連する病気、または、神経変性疾患など)を治療するための薬物を調製するために使用していてもよい。 (もっと読む)
タンパク様薬剤およびその使用
本発明は、システイン含有スカフォールドおよび/またはタンパク、および、そのようなシステイン含有産物を担持するか、および/または発現する発現ベクター、宿主細胞、および提示システムを提供する。本発明はさらに、そのような産物のライブラリーの設計法、そのようなライブラリーをスクリーニングして、標的分子に対し結合特異性を示す実体を生成する方法を提供する。さらに、本発明によって、本発明のシステイン含有産物を含む製薬組成物が提供される。 (もっと読む)
CD36の発現を減少させる方法
本発明は、細胞でCD36の発現を減少させる方法を提供する。前記方法は、以下を有する芳香族性陽イオンペプチドの有効量と細胞を接触させることを含む:少なくとも1つの正味の陽電荷;最小限4つのアミノ酸;最大限約20のアミノ酸;正味の陽電荷の最小数(pm)とアミノ酸残基総数(r)との間で、3pmがr+1以下の最大の数であるという関係;及び芳香族基の最小数(a)と正味の陽電荷の総数(pt)との間で、2aはpt+1以下の最大数であるが、ただしaが1のときはptもまた1でありえる関係。 (もっと読む)
予め標的化されたポジトロン放出断層撮影画像化のためのF−18ペプチド
F−18で放射能標識されたペプチドが、ヒドロキシルアミン基、チオセミカルバジド基、ヒドラジン基、または遊離アミン基を含むペプチドと4−[18F]フルオロベンズアルデヒドとを反応させることによって調製される。F−18放射能標識ペプチドの特定の非限定的な例が、本明細書に記載されている。標識ペプチドは、例えば臨床ポジトロン放出断層撮影法において有用である。  (もっと読む)
(もっと読む)
膀胱機能不全治療のためのキニンアンタゴニスト
本発明は、膀胱機能不全の治療及び/又は予防のための薬剤の製造のためのキニン受容体アンタゴニストの使用に関するもので、キニン受容体はB1及びB2受容体を含む群から選択される。 (もっと読む)
モチリン様ペプチドを含む、安定した薬学的組成物。
緩衝液で処理された溶液中に合成モチリン様ペプチドを含む、安定した薬学的組成物が開示される。この組成物は、長期の保管の間および蒸気滅菌後に、安定なままであり、そして実質的にその初期の効力を保持する、ペプチドを提供する。具体的には、本発明は、16個以下のアミノ酸および構造を有する、約0.5μg/ml〜100mg/mlの合成モチリン様ペプチドを含む、薬学的組成物に関する。上記組成物は、pH3〜9の間および重量オスモル濃度約10〜500mOsm/kgを有する水性組成物として提供され得る。 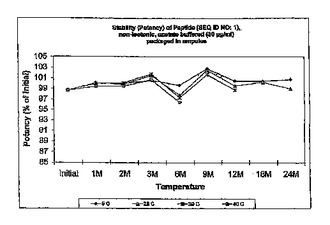 (もっと読む)
(もっと読む)
ウロテンシン−IIアゴニスト及びアンタゴニスト
【課題】ウロテンシンーII(U−II)のアンタゴニスト及びアゴニスト活性を有する新規なクラスの環状ポリペプチドの提供。
【解決手段】ウロテンシンーIIのポリペプチドのC末端保存領域におけるアミノ酸配列を基本に各種ポリペプチドの合成およびその生理活性を解析し、有効と判定される環状ポリペプチドを選択する。更に、ウロテンシン−IIの過剰または過小発現に特徴付けられる生理学的または心理学的状態を治療する為の方法をも特徴とする。
(もっと読む)
61 - 80 / 119
[ Back to top ]