Fターム[4H050BB11]の内容
第5−8族元素を含む化合物及びその製造 (19,778) | 反応媒体、分離・精製・回収用溶媒 (1,406) | 有機溶媒 (1,059) | 炭化水素 (203)
Fターム[4H050BB11]に分類される特許
121 - 140 / 203
製薬学的使用のためのマラチオンの調製方法
本発明は、毒性不純物の含量の低下した高純度のマラチオンを調製する方法を提供する。更に、本発明の方法により調製されたマラチオンは貯蔵安定性である。マラチオン中の毒性不純物、例えば、イソマラチオン、O,O,S-トリメチルホスホロジチオエート(MeOOSPS)、O,O,S-トリメチルホスホロチオエート(MeOOSPO)、O,S,S-トリメチルホスホロジチオエート(MeOSSPO)、マラオクソン、イソマラチオン、ジエチルフマレート、メチルマラチオン、ジメチルマラチオン、O,O-メチル,エチル-S-(1,2-ジカルボエトキシ)エチル-ホスホロジチオエートの量は、薬品の目的に使用されうるいずれかのその他の市販のマラチオン製剤より低い。 (もっと読む)
無水環状ホスホン酸の製造法
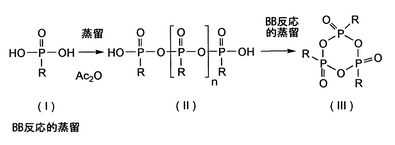
式(III)の無水環状ホスホン酸を、a)式(I)のホスホン酸誘導体を無水酢酸と30〜150℃で、酢酸と無水酢酸の混合物を蒸留により除去しながら反応させ、b)次いで、工程a)で得られた式(II)のオリゴマー状無水ホスホン酸を反応的蒸留にかけ、対応する式(III)の環状三量体状無水ホスホン酸に転化することにより、製造する方法を開示する。ここで、nは0〜300の数であり、Rは、アリル、アリール、または開鎖、環状、または分岐したC1〜C8アルキル基、アリールオキシ、アリルオキシ、または開鎖、環状、または分岐したC1〜C8アルキル基を含んでなるアルコキシである。好ましくは、工程b)で形成された環状三量体状無水ホスホン酸を、環状三量体状無水ホスホン酸に対して不活性な挙動を示す有機溶剤に直ちに溶解させる。 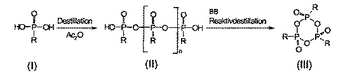 (もっと読む)
(もっと読む)
多孔性金属錯体の製造方法、多孔性金属錯体、吸着材、分離材、ガス吸着材及び水素吸着材
【課題】反応時間の短縮及び収率の増加が可能な多孔性金属錯体の製造方法を提供する。
【解決手段】中心金属とカルボキシレート基を有する有機配位子とを備える金属錯体の三次元的多孔性骨格構造からなる多孔性金属錯体の製造方法であって、有機配位子の塩をモノカルボン酸金属塩として調製し、中心金属の塩を第2の金属塩として調製し、モノカルボン酸金属塩及び第2の金属塩を反応させることを含む。
(もっと読む)
ヒドロキシ基を含有するホスホニトリル酸エステルの製造方法
【課題】1分子中にヒドロキシフェノキシ基及び/またはヒドロキシアルコキシ基を少なくとも1つ以上含有する環状及び/または鎖状ホスホニトリル酸エステルの製造方法の提供。
【解決手段】1価フェノール類及び/または1価アルコールをホスホニトリルジクロライド1分子中に含有されるクロロ基のモル数よりも当量未満となるように、ホスホニトリルジクロライドと反応(第1段目反応)させ、次いでアルカリ金属無機塩に対して過剰量の2価フェノール類及び/または2価アルコールを作用させることにより調製したモノアルカリ金属塩と該第1段目反応生成物とを反応(第2段目反応)させる。
(もっと読む)
不斉合成における使用のためのキラル配位子
本発明はビアリールビスホスフィン及びその中間生成物に関する。更に、本発明の範囲は、該ビスアリールホスフィンから製造できる触媒並びに不斉合成におけるその使用を包含する。 (もっと読む)
新規ホスフィン酸含有甲状腺ホルモン様剤
本発明は、ホスホン酸含有T3様剤およびそのモノエステル、その立体異性体、医薬的に許容される塩、共結晶、およびプロドラッグ、ならびにそのプロドラッグの医薬的に許容される塩および共結晶、それらの製造、そしてまた代謝性疾患、例えば肥満、NASH、高コレステロール血症および高脂質血症、ならびに関連する状態、例えばアテローム性動脈硬化、冠動脈心疾患、耐糖能異常、代謝症候群Xおよび糖尿病を予防および/または処置するためのそれらの使用に関する。 (もっと読む)
有機金属ベンゼンホスホナートカップリング剤
本発明は、有機合成のクロスカップリングに有用で、Rがホウ素、亜鉛、スズ、及びケイ素残基から選択される、一般式(I)有機金属ベンゼンホスホナートの化学属に関する。  (もっと読む)
(もっと読む)
ハロゲン化メタロセン化合物の製造方法
ジアルキル誘導体と、式R3xTLw(式中、Lは塩素、ヨウ素または臭素であり;R3は水素または炭化水素基であり;Tは元素の周期率表の2−14族の金属であり;x≧1であるため、x+wは金属Tの酸化状態に等しい)のハロゲン化剤と反応させる工程からなるハロゲン化メタロセン化合物の製造方法。 (もっと読む)
奇数の炭素原子を持つオレフィンを製造するための触媒前駆体、その調製方法、並びにそのようなオレフィンの製造方法
本発明は、XおよびYがハロゲンであり、nが2または3である化学式(I)を持つ奇数の炭素原子を持つオレフィンを製造するための触媒前駆体、並びにその調製方法およびエチレンのオリゴマー化方法に関する。 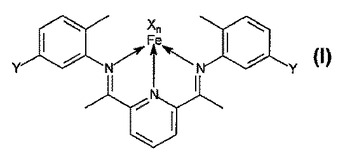 (もっと読む)
(もっと読む)
ジチオカルバメートの光分解によるアルコキシアミンの製造方法
【課題】【解決手段】ニトロオキシドとジチオカルバメートとから光分解反応によってアルコキシアミンを製造する新規な方法。本発明方法金属を含む廃液を生じず、アルコキシアミンの公知の合成方法より低温度でバッチまたは連続モードで実行できる。 (もっと読む)
ホスフェート誘導体
本発明に従って、以下のステップ(d)フェノール性ヒドロキシ化合物をアルキルα:ωジアルデヒド又は糖様ポリヒドロキシジアルデヒドと反応して、ヘミアセタールを形成し;(e)ステップ(a)からの生成物の末端アルデヒド基を水酸基と反応し;そしてステップ(b)から形成された水酸基をリン酸化して、フェノール性ヒドロキシ化合物のホスフェート誘導体を生成するステップの反応生成物を含むフェノール性ヒドロキシ化合物のホスフェート誘導体が提供される。 (もっと読む)
アミン置換ジフェニルホスフィン
本発明は、少なくとも1個のアミン置換基をホスフィン基に対してパラ位に有する、式(Ia)、(Ib)の1,1’−ジフェニル−2,2’−ジホスフィンに関する。これらの新規な化合物は、プロキラル有機化合物の不斉付加反応の触媒である金属錯体の配位子であり、そしてこの触媒特性は、アミノ基の置換を介して基質特異的なやり方で調整することができる。 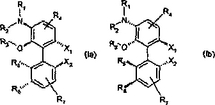 (もっと読む)
(もっと読む)
光学異性体の光学分割方法、及び光学分割装置
【課題】 分割効率及び回収率に優れ、汎用性が高く、さらに工業的スケールに好適に応用可能な光学異性体混合物の光学分割方法、及び光学分割装置を提供する。
【解決手段】 光学分割を行う対象である光学異性体混合物を含む試料含有溶媒相を、前記光学異性体混合物に含まれる一の光学異性体に対して他の光学異性体よりも強く相互作用可能な不斉源を含み、かつ前記試料含有溶媒相に対し不溶乃至難溶な不斉源含有溶媒相の中を移動させることを特徴とする光学異性体の光学分割方法である。該光学異性体の光学分割方法に用いられる光学分割装置である。
(もっと読む)
不斉合成用触媒およびそれに用いる配位子、並びにこれらを用いた不斉合成反応による光学活性化合物の製造方法
【課題】広範な光学活性アリール化合物の合成に利用できる汎用性と、工業的に有利な穏和な条件で短時間、高収率で合成できる反応性、選択性とを併せ持った製造法の提供。
【解決手段】下記一般式(1a)または(1b)で表される化合物。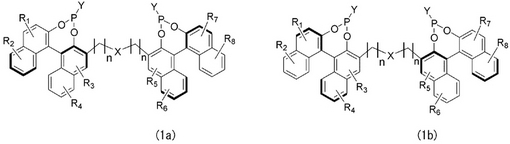
中心金属がロジウムであり、一般式(1a)または(1b)で表される化合物を配位子として含む錯体。
(もっと読む)
リン置換ポルフィリン化合物の製造方法
【課題】 各種のリン官能基をポルフィリン環に自在に導入することを可能にする、リン置換ポルフィリン化合物の新規な製造方法を提供すること。
【解決手段】 ハロゲン置換ポルフィリン化合物と第二ホスフィンを、遷移金属を触媒としてカップリング反応させることで、ホスフィン置換ポルフィリン化合物を製造する。ホスフィン置換ポルフィリン化合物は、例えば、酸化反応に付することでホスフィンオキシド置換ポルフィリン化合物に変換することができる。また、ハロゲン置換ポルフィリン化合物と亜リン酸エステルを、遷移金属を触媒としてカップリング反応させることで、ホスホン酸エステル置換ポルフィリン化合物を製造する。ホスホン酸エステル置換ポルフィリン化合物は、例えば、脱エステル化反応に付することでホスホン酸置換ポルフィリン化合物に変換することができる。
(もっと読む)
カルジオリピン組成物、その製造方法及び使用
本発明は、異なる鎖長を有し、及びまた不飽和の有無の両方の場合の異なる脂肪酸及び/又はアルキル鎖を有するカルジオリピンの新規合成経路を提供する。カルジオリピン変異体を含むカルジオリピンの新規形態を製造するために、反応スキームが使用できる。本方法によって製造されるカルジオリピンは、疎水性又は親水性薬剤などの活性剤をまた含むことができるリポソームや他の脂質製剤に便利にも組み込むことができる。このような製剤は、疾患の治療、あるいは診断アッセイ及び/又は分析アッセイで使用できる。リポソームはまた、例えば、リガンドをある細胞型又は特異的組織に向かわせるために、リガンドを含むことができる。
【化1】
 (もっと読む)
(もっと読む)
結晶性カルバペネム中間体
本発明は、式(I)の化合物(式中、TBSは、t−ブチルジメチルシリル基を表し、Phはフェニル基を表す)またはその塩もしくは溶媒和物の結晶に関する。式(I)の化合物は、抗菌剤として有用な2−置換−1βメチルカルバペネム化合物の合成中間体である。本発明の結晶は、取扱い性に優れ、優れた抗菌活性を有するカルバペネム化合物を、より簡便に製造することができ、さらに、その収率および純度を向上させることができる。
【化1】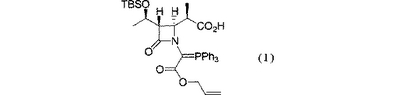
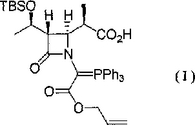 (もっと読む)
(もっと読む)
ポリイソブテンホスホン酸及びその誘導体
本発明は、ポリイソブテンホスホン酸及びその誘導体、その製法並びにその使用に関する。 (もっと読む)
アシルホスファン、並びにこれらの酸化物及び硫化物の製造方法
式I:
R1P(COR2)2
〔式中、
R1は、非置換フェニル、又は1〜5つのハロゲン、C1〜C8−アルキル、C1〜C8−アルキルチオ及び/若しくはC1〜C8−アルコキシにより置換されているフェニルであり;
R2は、C1〜C18−アルキル又はC2〜C18−アルケニル;C1〜C18−アルキル、又はハロゲン、−OR10、−OCO-R10、−OCO−Hal、−COO−R10、−N(R11)−CO−R10、−N(R11)−CO−Hal、−CO−NR11R10、−CH=CH−CO−OR10又は−CH=CH−フェニルにより1回又は1回以上置換されているC2〜C18−アルケニル;−C(C1〜C4−アルキル)=C(C1〜C4−アルキル)−CO−OR10又は−C(C1〜C4−アルキル)=C(C1〜C4−アルキル)−フェニル;C5〜C12−シクロアルキル、C2〜C18−アルケニル、フェニル−C1〜C4−アルキル、フェニル、ナフチル、ビフェニル又は5員若しくは6員の−O−、S−若しくはN含有複素環であり、基フェニル、ナフチル、ビフェニル又は5員若しくは6員の−O−、S−若しくはN含有複素環は、非置換であるか、又は1〜5つのハロゲン、C1〜C8−アルキル、C1〜C8−アルコキシ及び/若しくはC1〜C8−アルキルチオで置換されており;
R10は、水素、C1〜C18アルキル、1個又は数個の非連続−O−原子で中断されているC2〜C18アルキル、C5〜C12−シクロアルキル、フェニル−C1〜C4−アルキル、C2〜C18−アルケニルであり、フェニル、ナフチル又はビフェニルは、非置換であるか又は1〜5つのC1〜C8−アルキル、C1〜C8−アルコキシ、C1〜C8−アルキルチオ及び/若しくはハロゲンで置換されており;
R11は、水素、C1〜C18アルキル、1個又は数個の非連続O原子で中断されているC2〜C18アルキル、C5〜C12−シクロアルキル、C2〜C18−アルケニル、フェニル−C1〜C4−アルキル、フェニル、ナフチル、ピリジルであり、基フェニル、ナフチル又はピリジルは、非置換であるか又は1〜5つのC1〜C8−アルキル、C1〜C8−アルコキシ、C1〜C8−アルキルチオ及び/若しくはハロゲンで置換されている〕
で示されるビス−アシルホスファンの製造方法であって、
a)式II:
R1P(Cl)2
で示されるジクロロフェニルホスファンを、20〜200℃の範囲の温度及び大気圧から20barの水素圧下で、水素化触媒、第三級脂肪族アミン又は芳香族アミンの存在下、及び水素化条件下で非反応性である非プロトン性溶媒の存在下で、水素を用いて選択的還元して、環状フェニルホスファン(R1P)n(n=4〜6)を得る工程;或いは
b)R1P(Cl)2を、80〜200℃の範囲の温度及び20bar〜250barの水素圧下で、水素化触媒、第三級脂肪族アミン又は芳香族アミンの存在下、及び水素化条件下で非反応性である非プロトン性溶媒の存在下で、水素を用いて選択的還元して、R1PH2を得る工程;
c)続いて、適切な塩基の存在下で式IIIの酸ハロゲン化物:
R2COHal
(ここでR2は上記で定義されたとおりである)と反応させる工程
を含む方法。
(もっと読む)
シクロペンタジエニル−フルオレニル配位子をベースにした第III族の架橋メタロセン
本発明は式(Flu−R”−Cp)M(η3−C3R’5)(エーテル)n(I)を有するメタロセン触媒成分に関する。但し上式中Cpは置換基をもったまたはもたないシクロペンタジエニル、Fluは置換基をもったまたはもたないフルオレニル、R”は成分に立体的な剛性を与えるためのCpとFluとの間の構造的な架橋、Mは周期律表の第III族の金属であり、各R’は同一または相異なり水素、または炭素数1〜20のヒドロカルビルであり、nは0、1または2である。さらに該触媒成分の製造法、並びに極性または非極性の単量体の制御された重合に対する該触媒成分の使用が開示されている。 (もっと読む)
121 - 140 / 203
[ Back to top ]

