Fターム[4B065AB01]の内容
微生物、その培養処理 (127,014) | 遺伝子工学技術により創製された微生物 (11,728) | 外来遺伝子が導入されたもの (10,397)
Fターム[4B065AB01]に分類される特許
2,061 - 2,080 / 10,397
mRNAの阻害/不安定領域の除去方法
【課題】 mRNAのコード領域内の阻害/不安定配列の効果を減少させる方法の提供。
【解決手段】 mRNAをコードする遺伝子を提供し、mRNAのコード領域内の阻害/不安定配列(群)の位置決定を行い、多重点突然変異を作成することにより遺伝子内の阻害/不安定配列へ突然変異を導入する。この方法により、該mRNAをコードする遺伝子を改変して、遺伝子のコード能を変更しないようにクラスターヌクレオチド置換を施すことで、これらの阻害/不安定配列群を取り除く。
(もっと読む)
CHO/CERT細胞系
本発明は、細胞培養技術の分野に関する。本発明は、CERT S132A発現カセットを含むベクターコンストラクトを含む産生宿主細胞系を記載する。それらの細胞系は、改善された増殖特徴及び高いCERT S132A発現レベルを有する。本発明は、特に、DSMZにナンバーDSM ACC2989(CHO/CERT 2.20)及びDSM ACC2990(CHO/CERT 2.41)の下で寄託されている2つの細胞系に関する。本発明は、さらに、そのような好ましい産生宿主細胞を生成する方法ならびにDSMZにナンバーDSM ACC2989(CHO/CERT 2.20)及びDSM ACC2990(CHO/CERT 2.41)の下で寄託されている2つの細胞系を使用してタンパク質を産生する方法に関する。  (もっと読む)
(もっと読む)
イソプロパノール、n−ブタノール、及びイソブタノールの産生のための微生物
イソプロパノール経路を有する非天然微生物には、イソプロパノール経路酵素をコードする少なくとも1つの外来性核酸を含む。該経路には、4-ヒドロキシブチリル-CoAデヒドラターゼ、クロトナーゼ、3-ヒドロキシブチリル-CoA脱水素酵素、アセトアセチル-CoAシンテターゼ、アセチル-CoA:アセトアセタート-CoAトランスフェラーゼ、アセトアセチル-CoAヒドロラーゼ、アセトアセタートデカルボキシラーゼ、及びアセトン還元酵素から選択される1つの酵素を含む。W-ブタノール経路を有する非天然微生物には、w-ブタノール経路酵素をコードする少なくとも1つの外来性核酸を含む。他の非天然微生物は、w-ブタノール経路又はイソブタノール経路を有する。該生物を培養して、イソプロパノール、w-ブタノール、又はイソブタノールを産生する。 (もっと読む)
Apo−2リガンド
【課題】Fas/Apo-1、TNF-R1、又はTNF-R2レセプター等によって感知できるほどに阻害されない新規なサイトカインを提供する。
【解決手段】哺乳動物癌細胞のアポトーシスを誘発するApo-2リガンドと命名された新規なサイトカイン。Apo-2リガンドは、TNFサイトカインファミリーのメンバーに属すると考えられる。Apo-2リガンドキメラを含有する組成物、Apo-2リガンドをコードする核酸、及びApo-2リガンドに対する抗体、さらに、アポトーシスを誘発し癌などの病理学的状態を治療するためのApo-2リガンドの使用方法。
(もっと読む)
多重遺伝子ベクターによってコードされる組換えウイルス様粒子
本発明は、産生のための組換えDNA技術および細胞培養技術に基づいて、ワクチン、診断ツールおよびR&Dツールとして使用するための新たなウイルス様粒子を記載する。本発明の組換えウイルス様粒子は、(a)同じウイルスの異なるウイルス株および/または(b)同じウイルスの異なる血清型および/または(c)異なる宿主に特異的な異なるウイルス株のいずれかから選択される、いくつかの、特に2個以上の異なるエピトープを取り込んだポリペプチド鎖によって会合されている。その後、これらのエピトープは粒子表面上にディスプレイされる。 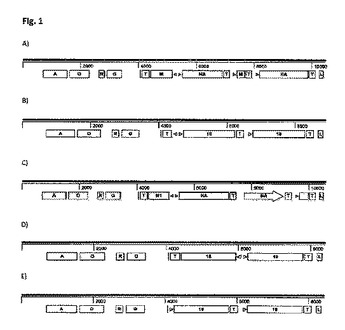 (もっと読む)
(もっと読む)
コウジ酸の産生に必須の遺伝子を利用してコウジ酸の産生量を向上する方法
【課題】微生物のコウジ酸の産生に必須である遺伝子を利用して、コウジ酸の産生能が向上された微生物およびその製造方法の提供する。
【解決手段】微生物における特定の塩基配列からなる群から選択される1または複数のコウジ酸の産生に必須の遺伝子の発現量および/または当該遺伝子にコードされるタンパク質の活性を正に制御することを含む、コウジ酸の産生能が向上した微生物の製造方法。前記微生物を用いたコウジ酸の製造方法。
(もっと読む)
増大した光出力を有する合成オプロフォルスルシフェラーゼ
改変ルシフェラーゼポリペプチドをコードするポリヌクレオチド。改変ルシフェラーゼポリペプチドは、野生型オプロフォルスルシフェラーゼに対して少なくとも60%のアミノ酸配列同一性を有し、配列番号1の野生型オプロフォルスルシフェラーゼのアミノ酸に対応する位置で少なくとも1つのアミノ酸置換を含む。改変ルシフェラーゼポリペプチドは、野生型オプロフォルスルシフェラーゼに対して、増大した発光、増大したシグナルの安定性及び増大したタンパク質の安定性の少なくとも1つを有する。 (もっと読む)
キメラ因子H結合タンパク質(FHBP)およびその使用方法
N.メニンギティディスの様々なfHbp変種株に対して殺菌性である抗体を誘発することができるキメラfHbp、および使用方法が提供されている。 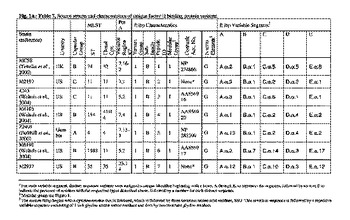 (もっと読む)
(もっと読む)
方法
【課題】高純度アルブミンの精製法であって、アルブミン(好ましくは、形質転換酵母によって発現され分泌されたもの)に一連のクロマトグラフィー段階を施してなる方法を提供する。
【解決手段】カチオン交換クロマトグラフィー、アニオン交換クロマトグラフィー、アフィニティークロマトグラフィーの段階を含む方法。アルブミン溶液中のニッケルの濃度を減少させる方法も、組換えアルブミンコード配列と同様であり、組換えアルブミンコード配列を発現する真菌細胞を培養することを含んでなり、この細胞の組換え発現アルブミンのマンノシル化能力が減少していることを特徴とする方法。
(もっと読む)
HIV治療のための抗CXCR4抗体
本発明は、CXCR4と結合することができるだけでなく、CXCR4ホモ二量体のコンフォメーション変化を誘導することができ、かつ、PBMCにおけるHIV−1一次単離物の複製を阻害することができる新規な単離された抗体、またはその誘導化合物もしくは機能的フラグメントに関する。より詳細には、本発明は、CXCR4タンパク質に特異的な515H7および301aE5モノクローナル抗体、ならびにHIV感染の処置のためのそれらの使用に関する。このような抗体から構成される医薬組成物およびこのような抗体の選択のための方法も包含される。 (もっと読む)
免疫化組成物およびアミロイド前駆体タンパク質のβ−セクレターゼ切断部位に対する免疫応答を誘発するための方法
【課題】アミロイド前駆体タンパク質のβ−セレクターゼ切断部位に対する免疫応答を誘発するための方法を提供する。
【解決手段】多重抗原ペプチドシステム(MAPS)のような抗原生成物またはAβPPのβ−セクレターゼ切断部位にまたがるAβPPエピトープを提示する繊維状バクテリオファージを含む免疫化組成物、およびこの免疫化組成物を使用してAβPPのβ−セクレターゼ切断部位に対する免疫応答を誘発するための方法からなる。また、AβPPのβ−セクレターゼ切断部位に対する抗体、およびアミロイドβの形成を阻害するための方法からなる。
(もっと読む)
α4β7インテグリンと反応するヒト化免疫グロブリン
【課題】炎症性腸疾患に対する改良された治療アプローチを提供すること。
【解決手段】ヒト化免疫グロブリン軽鎖またはその抗原結合断片をコードするヌクレオチド配列を含む単離された核酸であって、該ヒト化免疫グロブリン軽鎖またはその抗原結合断片は、ネズミAct−1モノクローナル抗体の軽鎖の相補性決定領域(CDR1、CDR2およびCDR3)を含み、該相補性決定領域は、以下:
軽鎖: CDR1 配列番号:12のアミノ酸44−59
CDR2 配列番号:12のアミノ酸75−81
CDR3 配列番号:12のアミノ酸114−122
に示されるアミノ酸配列を含み、軽鎖枠組み領域は、GM607’CL抗体の軽鎖(配列番号:8)に由来し、カバット2位のイソロイシンは、バリンに交換されており、その結果、該軽鎖またはその抗原結合断片を含む抗体が、α4β7インテグリンに選択的に結合する、核酸。
(もっと読む)
フルクタン生合成の操作および植物バイオマスの増強
本発明は、植物の光合成細胞におけるフルクタン生合成を操作することができる遺伝的構築物であって、細菌FT酵素をコードする核酸またはその機能的に活性な断片もしくは変異体に作動的に連結したプロモーターまたはその機能的に活性な断片もしくは変異体を含む遺伝的構築物に関する。本発明はまた、植物におけるフルクタン生合成の改変に関し、特に、光合成細胞におけるフルクタン生合成を操作する方法に関する。本発明はまた、植物バイオマスの増加に関し、特に、植物におけるシュートおよび/または根の生長を含むバイオマス収量および/または収量安定性を増強する方法に関する。本発明はまた、生化学的経路の生産性を増強する方法に関する。 (もっと読む)
ブレビバチルス属細菌を用いたプロテインA様蛋白質の生産方法
【課題】本発明は、プロテインA様蛋白質の生産のための効率的で経済的な方法に関する。
【解決手段】プロテインA様蛋白質の遺伝子組換え技術を用いた生産は、大腸菌、枯草菌などの宿主が使用されているが生産性の低さにより高価格の大きな原因となっている。従って大腸菌や枯草菌以外の組換えDNA技術を用いたプロテインA様蛋白質の安価で大量な生産を可能にする技術の早急な確立が強く望まれている。本発明は、プロテインA様蛋白質の大量生産方法であり、組換えブレビバチルス属細菌により該蛋白質を培養液中へ大量に分泌発現させ、培養液中からその蓄積された該プロテインA様蛋白質を分離回収することからなる方法などを提供する。
(もっと読む)
遺伝子ベクター
造血前駆細胞(HSPC)または造血幹細胞(HSC)中ではヌクレオチド配列の発現を防止するか、または低下させるが、分化した細胞中ではそうしない、HSPCまたはHSC中に対応するmiRNAを有するヌクレオチド配列に機能し得る形で連結された少なくとも1個のmiRNA配列標的を含む、遺伝子療法における使用のための遺伝子ベクター。 (もっと読む)
EphA2モノクローナル抗体およびその使用法
【課題】癌を治療するための新しい治療薬、および癌を治療するための新しいより有効な療法の組み合わせを提供する。
【解決手段】EphA2と結合しEphA2に作用し、それによってEphA2リン酸化を増大しEphA2レベルを低下させる、有効量の抗体の投与を含むことからなる。また、EphA2と結合し、癌細胞の軟寒天中でのコロニー形成を阻害し、三次元基底膜または細胞外マトリックス調製物中での管状ネットワーク形成を阻害し、非癌細胞ではなく癌細胞上で露出したEphA2エピトープと優先的に結合し、かつ/またはKoffが低く、それによって腫瘍細胞増殖および/または転移を阻害する、有効量の抗体の投与を含むことからなる。さらに、EphA2抗体を単独でまたは1種もしくは複数の癌治療に有用な他の薬剤と組み合わせて含む医薬組成物の投与からなる。
(もっと読む)
1,3−ブタンジオールの産生のための生物
非天然微生物には、1,3-ブタンジオール(1,3-BDO)を産生するのに十分な量で発現する1,3-BDO経路酵素をコードする少なくとも1つの外来性核酸を有する1,3-BDO経路を有する微生物を含む。経路には、2-アミノ-4-ケトペンタノアート(AKP)チオラーゼ、AKP脱水素酵素、2-アミノ-4-ヒドロキシペンタノアートアミノトランスフェラーゼ、2-アミノ-4-ヒドロキシペンタノアート酸化還元酵素(脱アミノ化)、2-オキソ-4-ヒドロキシペンタノアートデカルボキシラーゼ、3-ヒドロキシブチルアルデヒド還元酵素、AKPアミノトランスフェラーゼ、AKP酸化還元酵素(脱アミノ化)、2,4-ジオキソペンタノアートデカルボキシラーゼ、3-オキソブチルアルデヒド還元酵素(ケトン還元)、3-オキソブチルアルデヒド還元酵素(アルデヒド還元)、4-ヒドロキシ-2-ブタノン還元酵素、AKPデカルボキシラーゼ、4-アミノブタン-2-オンアミノトランスフェラーゼ、4-アミノブタン-2-オン酸化還元酵素(脱アミノ化)、4-アミノブタン-2-オンアンモニア-リアーゼ、ブテノンヒドラターゼ、AKPアンモニア-リアーゼ、アセチルアクリラートデカルボキシラーゼ、アセトアセチル-CoA還元酵素(CoA‐依存性、アルデヒド形成)、アセトアセチル-CoA還元酵素(CoA‐依存性、アルコール形成)、アセトアセチル-CoA還元酵素(ケトン還元)、3-ヒドロキシブチリル-CoA還元酵素(アルデヒド形成)、3-ヒドロキシブチリル-CoA還元酵素(アルコール形成)、4-ヒドロキシブチリル-CoAデヒドラターゼ、及びクロトナーゼから選択される酵素を含む。1,3-BDOを産生する方法には、1,3-BDOを産生する条件下及び十分な時間で、このような微生物を培養することを含む。 (もっと読む)
マルトース−1−リン酸生成酵素
【課題】マルトオリゴ糖、デキストリン及び澱粉等のグルコース重合度5以上のα−1,4グルコシル結合を含むオリゴ糖又は多糖を原料とし、大量のマルトース−1−リン酸の生成を可能とするマルトース−1−リン酸生成酵素を提供する。
【解決手段】コリネバクテリウム属に属する細菌由来のマルトース−1−リン酸生成酵素を用い、グルコース重合度5以上のα−1,4グルコシル結合を含むオリゴ糖又は多糖及びリン酸類又はその塩からマルトース−1−リン酸を生成する方法。
(もっと読む)
インフルエンザ赤血球凝集素の組成物とその使用
本発明は医学、公衆衛生、免疫学、分子生物学及びウイルス学の分野にある。本発明はインフルエンザの治療、寛解、及び/又は予防のための組成物、ワクチン組成物及び薬学的組成物を提供する。本発明の組成物、ワクチン組成物及び薬学的組成物はRNAバクテリオファージのウイルス様粒子及び少なくとも一つの抗原を含み、前記少なくとも一つの抗原はインフルエンザウイルス赤血球凝集タンパク質の外部ドメイン又はインフルエンザウイルス赤血球凝集タンパク質の前記外部ドメインの断片である。動物、好ましくはヒトに投与される場合、前記組成物、ワクチン組成物及び薬学的組成物は効果的に免疫応答、特に抗体応答を誘導し、典型的にかつ好ましくは前記抗体応答はインフルエンザウイルスに対する。従って、本発明はインフルエンザウイルス感染の治療、寛解、及び/又は予防の方法を更に提供する。 (もっと読む)
タンパク質のグリコシル化の制御、ならびにそれに関する組成物および方法
【課題】タンパク質のグリコシル化を制御するための新規な方法、およびそれによって産生させたタンパク質の提供。
【解決手段】グリコシル化阻害剤の存在下で宿主細胞を培養することによって、グリコシル化部位を含むタンパク質を産生させるステップを含み、生成したタンパク質はグリコシル化部位において、より少ないグリカンまたはより少ない糖を含む、タンパク質の製造方法。タンパク質の生物学的特徴がグリコシル化レベルの減少によって変化し、例えばタンパク質とその標的リガンドとの結合が改変される。
(もっと読む)
2,061 - 2,080 / 10,397
[ Back to top ]