Fターム[4C057AA20]の内容
Fターム[4C057AA20]の下位に属するFターム
Fターム[4C057AA20]に分類される特許
1 - 20 / 33
改変タンパク質
【課題】グリコシルトランスフェラーゼによりペプチドおよびタンパク質を結合させる方法を提供する。
【解決手段】治療用タンパク質の便利な合成または半合成を可能にする手段および方法であって、改変の導入が上記の問題に対処している手段および方法。可溶性糖タンパク質誘導体の循環半減期を延長して、治療または予防のための循環する糖タンパク質の治療的有効レベルを維持するために必要な、注射剤の量および注射の頻度を減少させる方法。一定の治療的に活性な糖タンパク質の短いインビボ血漿半減期は、治療または予防に必要とされる可溶性タンパク質の頻度および量に起因して望ましくないものである。糖タンパク質構造を効果的に変化させ、また生物学的活性を実質的に維持して、このような糖タンパク質の循環半減期を延長するための手段。
(もっと読む)
プリンヌクレオシドの合成
【課題】HCVウイルスの強力な抑制剤であるプリンホスホルアミデート化合物及びその製造方法の提供。
【解決手段】化合物Iもしくはその塩または化合物IIもしくはその塩。化合物I、IIもしくはその立体異性体、その塩(酸または塩基付加塩)、水和物、溶媒和物、または結晶形態である、ヌクレオシド誘導体のホスホルアミデートプロドラッグまたは環状リン酸塩プロドラッグを、調製するためのプロセス。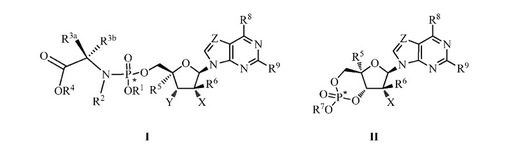 (もっと読む)
(もっと読む)
オリゴヌクレオチドの合成
【課題】本発明の目的は、先行技術の欠点の少なくとも一部を克服するオリゴヌクレオチドを調製するための方法を提供することである。
【解決手段】オリゴヌクレオチドを調製するための方法であって、a)式(A)を有するヒドロキシル基含有化合物を提供する工程、b)式Iを有する活性体(活性体I)の存在下で前記化合物をリン酸化剤と反応させてリン酸化化合物を調製する工程、c)活性体Iとは異なる活性体IIの存在下で、単離していない前記リン酸化化合物を式(A)を有する第二の化合物と反応させる工程を含む、方法。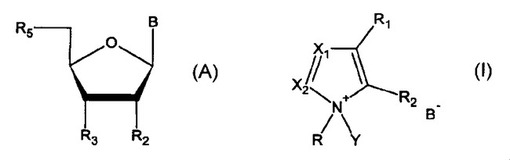 (もっと読む)
(もっと読む)
ヌクレオシドホスホルアミデート
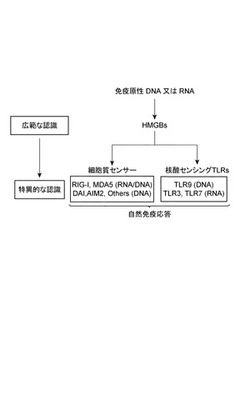
核酸により活性化される自然免疫応答の抑制剤及びスクリーニング方法
【課題】核酸により活性化される自然免疫応答の抑制剤及びスクリーニング方法を提供する。
【解決手段】塩基フリーホスホロチオエートデオキシリボースホモポリマー又はその誘導体からなる群から選択される化合物からなる、核酸により活性化される自然免疫応答の抑制剤、及び、被検物質の存在下及び非存在下で、固相化されたHMGBタンパクを放置するステップと、HMGBタンパクに標識核酸を接触させるステップと、HMGBタンパクに結合した標識核酸を定量するステップと、被検物質の存在下で放置したHMGBタンパクに結合した標識核酸が、被検物質の非存在下で放置したHMGBタンパクに結合した標識核酸よりも少ない場合に、被検物質が、核酸により活性化される自然免疫応答の抑制剤であると判定し、多い場合に、被検物質が、核酸により活性化される自然免疫応答の促進剤であると判定する判定ステップと、を含む、スクリーニング方法。
(もっと読む)
癌及びウイルス感染の治療のためのプリンヌクレオシド一リン酸プロドラッグ
本発明は、ヒト患者又はそのほかの動物宿主における癌、又はウイルス感染、特に、HIV、HCV、ノロウイルス、サポロウイルス、HSV−1、HSV−2、デング熱ウイルス、黄熱病ウイルス、及びHBVによる感染を治療する又は予防するための化合物、組成物、及び方法を指向する。前記化合物は、6−置換されたプリン一リン酸、及び薬学上許容可能なその塩、プロドラッグ又はそのほかの誘導体である。特に、前記化合物は、HIV−1、HIV−2、HCV、ノロウイルス、サポロウイルス、HSV−1、HSV−2、デング熱ウイルス、黄熱病ウイルス、及びHBVに対する強力な抗ウイルス活性を示す。 (もっと読む)
ウラシルシクロプロピルヌクレオチド
その任意の可能な立体異性体を包含する式(I):
【化1】
[式中:R1は水素もしくはハロであり;R4は1リン酸、2リン酸もしくは3リン酸エステルであるか;またはR4は式(II)
【化2】
の基であり;R7は場合により置換されていてもよいフェニル;ナフチル;インドリルもしくはN−C1〜C6アルキルオキシカルボニル−インドリルであり;R8は水素、C1〜C6アルキル、ベンジルであり;R8’は水素、C1〜C6アルキル、ベンジルであるか;またはR8およびR8’はそれらが結合している炭素原子と一緒になってC3〜C7シクロアルキルを形成し;R9はC1〜C10アルキル、ベンジルもしくは場合により置換されていてもよいフェニルである]
の化合物;またはその製薬学的に許容しうる塩もしくは溶媒和物、製薬学的製剤およびHCV阻害剤としての化合物Iの使用。 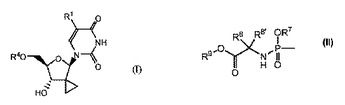 (もっと読む)
(もっと読む)
1−リン酸化糖誘導体のアノマーの選択的な製造法並びにヌクレオシドの製造法
【課題】フラノースやピラノースといった糖の骨格の違い、デオキシ糖といった置換基の有無、あるいは天然型や非天然型といった糖の種類に影響されることの無い、汎用性の高い、アノマー選択的な1−リン酸化糖誘導体ならびにヌクレオシドの製造方法を得ること。
【解決手段】1−リン酸化糖誘導体のアノマー混合物を加リン酸分解および異性化し、一方を結晶化することで平衡を傾け、選択的に望む異性体のみを製造する。さらに、ヌクレオシドホスホリラーゼの作用により、得られた1−リン酸化糖誘導体と塩基より、高い立体選択性と収率でヌクレオシドを製造する。
(もっと読む)
糖1−リン酸化合物の製造方法
【課題】糖1-リン酸化合物のアノマー位の立体異性体を選択的に製造する方法を提供する。
【解決手段】 式(I):R〜X-P(R1)(R2)〔Rは糖化合物から1位水酸基を除いた残基を示し、R1及びR2はアルキル基、アルコキシ基などを示し、Xは酸素原子などを示す〕で表される糖1-リン酸化合物の製造方法であって、式(II):R-Y(Yはヨウ素原子などを示しYはα結合である)で表される糖化合物と式(III):X=PH(R1)(R2)で表されるリン化合物とをDMANなどの塩基の存在下に反応させる工程を含む方法。
(もっと読む)
シクロプロピルポリメラーゼ阻害剤
式I:
【化1】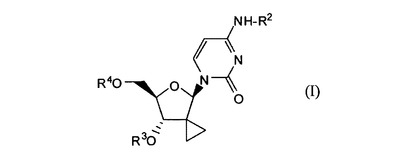
[式中:R2は水素又はC1−C4アルキルであり;R3及びR4は水素、−C(=O)R5又は−C(=O)CHR6−NH2であるか;あるいはR3は水素であり、そしてR4はモノホスフェート−、ジホスフェート−もしくはトリホスフェートエステルであるか、あるいはR3は水素、−C(=O)CHR5又は−C(=O)CHR6−NH2であり、そしてR4は(式2)であり、各R5は水素、C1−C6アルキル又はC3−C7シクロアルキルであり;R6は水素又はC1−C6アルキルであり;R7は、場合により置換されていることができるフェニル;ナフチル;又はインドリルであり;R8は及びR8は水素、C3−C7アルキル、ベンジルであるか;あるいはR8及びR8は一緒になってC3−C7シクロアルキルを形成し;R9はC1−C6アルキル、ベンジル又は場合により置換されていることができるフェニルであり;但しR2、R3及びR4はすべてが水素であることはない]
の化合物;あるいはその製薬学的に許容され得る塩又は溶媒和物;化合物Iを用いる製薬学的調製物;R2、R3及びR4がすべて水素である式Iの化合物を含む化合物IのHCV阻害剤としての使用。 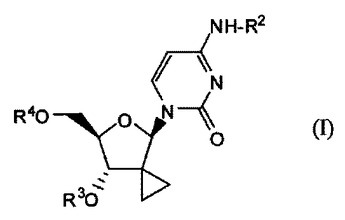 (もっと読む)
(もっと読む)
核酸固相合成用担体
【課題】高純度の核酸を高収量にて合成することができる核酸合成用固相担体を提供する。
【解決手段】本発明によれば、分子中に2個以上のビニル基を有する多官能性単量体単位と分子中に1個のビニル基を有するビニル単量体単位からなる多孔質共重合体粒子からなり、アセトニトリル中に浸漬したときの膨潤体積が3.5mL/g以上であり、レーザー散乱式粒度分布測定法によるメジアン粒径が50〜120μmの範囲にある核酸固相合成用担体が提供される。
(もっと読む)
オリゴヌクレオチドN3’→P5’ホスホルアミデート:合成および化合物;ハイブリダイゼーションおよびヌクレアーゼ耐性特性
【課題】本発明の目的は、N3’→P5’ホスホルアミデートの化合物および組成物、合成法ならびにオリゴヌクレオチドN3’→P5’ホスホルアミデートを用いるハイブリダイゼーションおよびヌクレアーゼ抵抗性方法を提供することである。詳細には、ホスホジエステラーゼ消化に対する著しく高められた抵抗性を有する改変されたオリゴヌクレオチド、3’−NHP(O)(O−)O−5’ホスホルアミデートを固体支持体上で合成することである。
【解決手段】ヌクレオシドサブユニットであって、ここで、DMTはジメトキシトリチル基であり、そしてBzはベンゾイル基である、ヌクレオシドサブユニット。
(もっと読む)
新規なマルトースホスホリラーゼ、その製造方法、およびその利用方法
【課題】組み合わせるべきトレハロースホスホリラーゼと最適温度が重複しており、最適温度の範囲が殺菌効果を期待できる温度域にあって、なおかつトレハロースの製造に適した温度安定性を有し、適度な温度で失活可能である、新規なマルトースホスホリラーゼおよびその利用方法を提供する。
【解決手段】最適温度および温度安定性の範囲が50.0〜58℃の間にあり、65℃、15分間の熱処理で90%以上失活する、新規なマルトースホスホリラーゼ、および該酵素を用いたトレハロースの製造方法。
(もっと読む)
機能性分子、機能性分子合成用アミダイド、及び標的物質解析方法
【課題】異なる置換基を有する複数種の修飾ヌクレオチド単位を含んでいても、PCR等による増幅を容易に行うことのできる機能性分子、及び前記機能性分子の合成に使用される機能性分子合成用アミダイド、並びにそれらを用いた標的物質解析方法を提供すること。
【解決手段】置換基が塩基から脱離可能であるように導入された修飾ヌクレオチド単位を含む機能性分子;置換基が塩基から脱離可能であるように導入されてなる、前記機能性分子の製造に用いられる機能性分子合成用アミダイド;機能性分子のランダムプールを作製するランダムプール作製工程と、所望の機能性分子を選別する選別工程と、選別された機能性分子を増幅する増幅工程とを含む標的物質解析方法であって、前記増幅工程前に、前記選別された機能性分子から置換基を脱離する脱離工程を含む標的物質解析方法;である。
(もっと読む)
修飾糖類
対応する未変性莢膜糖の単糖単位の内の少なくとも1個にヒドロキシル基位置でブロック基を含む修飾莢膜糖類であって、ここで前記ブロック基が、式(Ia)又は(Ib):−O−X−Y(Ia)又は−O−R1(Ib)(式中、Xは、C(O)、S(O)又はSO2であり;Yは、NR1R2又はR3であり;R1は、ヒドロキシル基、スルフヒドリル基及びアミン基から独立して選択される1、2又は3個の基によって置換されるC1−6アルキル基であり;R2はH又はC1−6アルキル基であり;及びR3はC1−6アルキル基である)である、修飾莢膜糖類;ブロック基を有する莢膜糖を修飾するためのプロセス;修飾莢膜糖を含む糖−タンパク質複合体;糖−タンパク質複合体を作製するためのプロセス、修飾莢膜糖及び/又は糖−タンパク質複合体を含む医薬組成物;及びその方法と使用。 (もっと読む)
官能性ベータ1,6グルコサミン二糖類およびその製造方法
本発明は、式(1)のβ-(1->6)-結合型グルコサミン二糖類の化学合成のための新規な方法およびその方法に関係する(中間体)化合物に関する。さらなる態様では、発明は化合物を含む組成物ならびに二糖類および医薬の合成における化合物の使用に関する。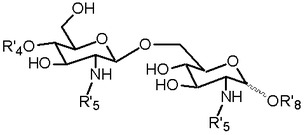
(1) 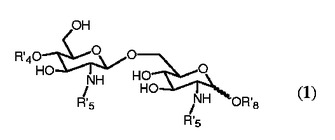 (もっと読む)
(もっと読む)
非天然塩基
【課題】 天然塩基とミスマッチを起こすことが少なく、安定に複製することを可能とし、さらに酵素による取り込み効率の高い、非天然塩基を含む核酸を製造する。
【解決手段】 二本鎖核酸または二本鎖PNAの主鎖に大きな歪みを生じさせないような塩基対を形成する非天然型塩基等を提供する。
(もっと読む)
糖または糖誘導体のリン酸エステルの製造方法
【課題】
従来に比べ簡便で新規な糖または糖誘導体のリン酸エステルを製造する方法を提供する。
【解決手段】
糖または糖誘導体とリン酸供与体とを酸性ホスファターゼ存在下で反応させることにより糖または糖誘導体のリン酸エステルを製造する方法。
また、糖または糖誘導体が第一級の水酸基を持つ化合物であり、リン酸供与体がポリリン酸又はその塩であり、酸性ホスファターゼがShigella属に由来する酸性ホスファターゼである、前記の製造方法。
(もっと読む)
可逆的停止ヌクレオチドを利用する配列決定法および遺伝型解析法
本発明は、2’位において修飾された可逆的ターミネーターヌクレオチドを用いた標的核酸のヌクレオチド配列
を決定する方法を提供する。
(もっと読む)
カチオン性オリゴヌクレオチド、同ヌクレオチドの自動調製法およびそれらの使用
本発明は、自動ホスホロアミダイト化学を介して合成され得る、オリゴヌクレオチド部分Aiおよびオリゴカチオン部分Bjを有するオリゴヌクレオチド−オリゴカチオン分子AiBjHであって、Aiは、i−merのオリゴヌクレオチド残基であり、i=5〜50であり、ヌクレオチドAは、天然または非天然に発生する核酸塩基および/またはペンタフラノシル基および/または生来のホルホジエステル結合を有するオリゴマー、例えば、デオキシリボ、リボ、ロック(LNA)ヌクレオチドから選択され、並びにそれらの化学改変体または置換体、例えばホスホロチオアート、2’−フルオロ、2’−O−アルキルまたはマーカー基、例えば、蛍光剤であり、Bjは、j−merの有機オリゴカチオン部分であり、j=1〜50であり、Bは、・-HPO3-R1-(X-R2)n1-X-R3-O-(ここで、R1、R2およびR3は、同一または異なって、低級アルキレンであり、XはNHまたはNC(NH2)2であり、nは1〜5であり、n1=2〜20である)、・-HPO3-R4-CH(R5X1)-R6-O-(ここで、R4は低級アルキレンであり、R5およびR6は、同一または異なって、低級アルキレンであり、X1はプトレッシン、スペルミジンまたはスペルミン残基である)、・-HPO3-R7-(aa)n2-R8-O-(ここで、R7は低級アルキレンであり、R8は低級アルキレン、セリン、天然アミノアルコールであり、(aa)n2は、カチオン性側鎖を有する天然アミノ酸、例えば、アルギニン、リシン、オルニチン、ヒスチジン、ジアミノプロピオン酸を含むペプチドであり、n2=2〜20である)を含む群から選択されるものに関する。 (もっと読む)
1 - 20 / 33
[ Back to top ]