Fターム[4C069CC13]の内容
ピロール系化合物 (8,574) | 製法 (628) | 化学的方法 (523) | 複素環の形成を伴わないもの (410) | 置換基の形成導入 (324)
Fターム[4C069CC13]の下位に属するFターム
Fターム[4C069CC13]に分類される特許
41 - 60 / 115
脱アセチル化酵素Bのヒドロキサメートを基にした阻害剤
本教示は、式Iの化合物、ならびにその医薬上許容される塩、水和物、エステル、およびプロドラッグに関する: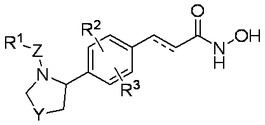
I
A
(ここで、R1、R2、R3、Y、Z、および(A)は、本明細書に定義されたとおりである)。
本教示は、式Iの化合物を調製する方法、ならびに脱アセチル化酵素により全体または部分的に媒介される病理学的症状または障害を処置、阻害、または予防する際に、式Iの化合物を使用する方法も提供する。 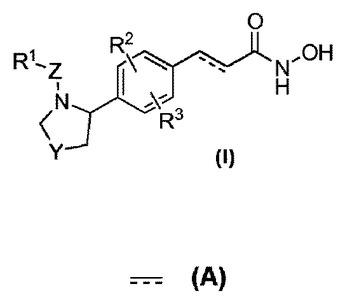 (もっと読む)
(もっと読む)
新規な方法
本発明は、NEP阻害剤またはそのプロドラッグ、特に、γ−アミノ−δ−ビフェニル−α−メチルアルカン酸、もしくは酸エステルの主鎖を含むNEP阻害剤を製造する新規な方法に関する。詳細には、本発明による新規な方法は、最終的に、上記NEP阻害剤、すなわち、式(1)(式中、R1およびR2は、互いに独立して、水素または窒素保護基であり、R3は、カルボキシル基またはエステル基、好ましくはカルボキシル基またはアルキルエステルである)の化合物またはその塩を調製するための中間体の合成に関する。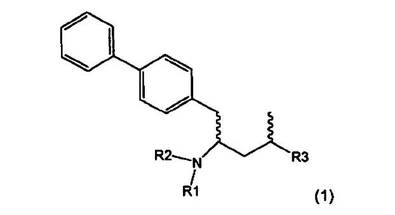
(もっと読む)
ヒスタミン−3受容体拮抗薬
【課題】ヒスタミンH3受容体に拮抗することにより治療することができる障害を治療する方法の提供。
【解決手段】式Iの化合物。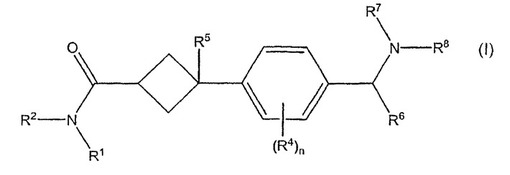
[式中、R1およびR2は、水素、置換されていてもよいアルキルなど、または、それらが結合している窒素と一緒に、4、5、6、または7員の飽和または不飽和脂肪族環を形成していてもよく、R5は、OH、−O(C1〜C3)アルキルなど、R6、R7、R8は、水素、置換されていてもよいアルキルなどであり、R7およびR8は、それらが結合している窒素と一緒に、4、5、6、または7員の複素環を形成していてもよい]
(もっと読む)
レニン阻害剤
本発明は、一般式(1)の新規なレニン阻害剤、これらの合成に関与する新規な中間体、これらの医薬的に認容し得る塩及びこれらを含有する医薬組成物に関する。本発明はまた、一般式(1)の化合物、これらの互変異性型、これらの医薬的に認容し得る塩、これらを含有する医薬組成物及びこれらの合成に用いる新規な中間体の調製方法に関する。 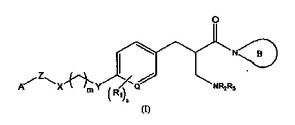 (もっと読む)
(もっと読む)
疼痛治療のためのカンナビノイド受容体のリガンドとしてのプロリン類似体
本発明は、カンナビノイド受容体に対するリガンドであるプロリン類似体化合物と、プロリン類似体化合物および薬学的に許容される担体を含む組成物と、そのようなプロリン類似体化合物を生成する方法と、それを必要とする動物に、プロリン類似体化合物の有効量を投与することを含む、状態を治療または予防するための方法とに関する。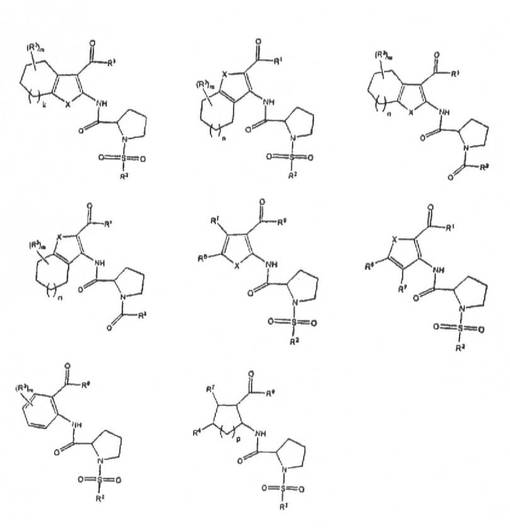
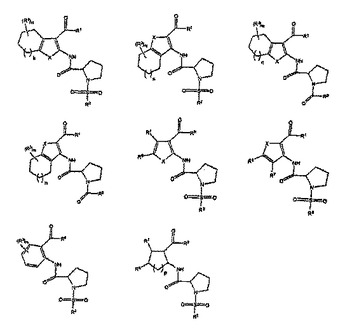 (もっと読む)
(もっと読む)
ピリド[2,1−a]イソキノリン誘導体の製造方法
本発明は、式(I)[式中、R2、R3及びR4は、それぞれ独立に、水素、ハロゲン、ヒドロキシ、低級アルキル、低級アルコキシ及び低級アルケニル(ここで、低級アルキル、低級アルコキシ及び低級アルケニルは、場合により、低級アルコキシカルボニル、アリール及びヘテロシクリルよりなる群によって置換されていてもよい)よりなる群から選択される]で示されるピリド[2,1−a]イソキノリン誘導体、及びその薬学的に許容しうる塩の新規な製造方法に関する。本発明の式(I)で示されるピリド[2,1−a]イソキノリン誘導体は、DPP IVに関連する疾患の治療及び/又は予防に有用である。 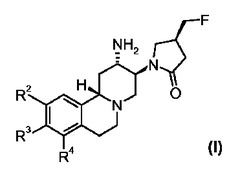 (もっと読む)
(もっと読む)
アミノアセチルピロリジンカルボニトリル誘導体の製造方法
【課題】DPP−IV阻害剤として有用なアミノアセチルピロリジンカルボニトリル誘導体の効率的な製造法を提供する。
【解決手段】アミノアセチルピロリジンカルボキサミド誘導体に、塩基存在下、塩化ピバロイルを作用させることを特徴とする、式(2):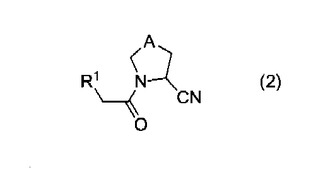
(式中、A、R1は前記と同意義を示す。)で示されるアミノアセチルピロリジンカルボニトリル誘導体の製造方法。
(もっと読む)
β位がアルキル化されたピロール類の製造方法
【課題】化学合成により簡便にピロール類のβ位を選択的にアルキル化して、β位がアルキル化されたピロール類を製造する方法を提供する。
【解決手段】下記一般式(1)で表されるピロール類と、下記一般式(2)で表される化合物と、ヒドリド供与体とを反応させることを特徴とする下記一般式(3)で表される化合物の製造方法(式中、R1は水素原子、脂肪族基、芳香族基又はトリアルキルシリル基であり;R2は置換基を有していても良いアルキル基、アリール基又は複素環式基である。)。
[化1]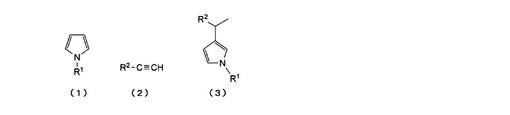 (もっと読む)
(もっと読む)
フェニルピロリジン化合物
本発明は、一般式(I)の新しいフェニルピロリジン化合物、メラトニン作動性障害を治療又は予防するためのそれらの使用及びその組成物を提供する。  (もっと読む)
(もっと読む)
神経ペプチドY2受容体のモジュレーターとしての置換ピペラジンおよびピペリジン
本発明は遊離塩基形または酸付加塩形の式(I)
[式中、置換基は本明細書に記載のとおりである]で示される化合物;その製造、医薬としてのその使用およびそれを含む医薬に関する。  (もっと読む)
(もっと読む)
三官能性擬ペプチド試薬、ならびにその使用および適用
本発明は、三官能性擬ペプチド試薬、特に生物発光試薬、または必要に応じて蛍光バイオコンジュゲートを調製するためのその様々な使用、固体支持体に官能化するための前記試薬およびバイオコンジュゲートの使用、ならびにそうして官能化した固体支持体を問題分子の検出に使用することに関する。 (もっと読む)
二重作用性降圧剤
本発明は、式: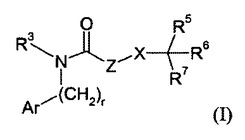
(式中、Ar、r、R3、Z、X、およびR5〜7は明細書中に定義の通りである)を有する化合物またはその薬学的に許容可能な塩に関する。これらの化合物は、AT1受容体アンタゴニスト活性およびネプリライシン阻害活性を有する。本発明はまた、かかる化合物を含む薬学的組成物、かかる化合物の使用方法、ならびにかかる化合物を調製するためのプロセスおよび中間体に関する。同一分子中にAT1受容体アンタゴニスト活性およびNEP阻害活性の両方を有する化合物を提供することは非常に望ましいであろう。これらの両活性を保有する化合物は、単一の分子薬物動態を有しながら2つの独立した作用様式によって降圧作用を示すと思われるので、治療薬として特に有用であることが期待される。 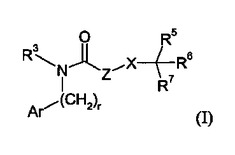 (もっと読む)
(もっと読む)
光学活性プロリンエステル誘導体およびN−ホルミル光学活性プロリン誘導体の製造方法
【課題】光学分割のような煩雑な処理をすることなく、トリクロロシランの活性化触媒となる特定配位子化合物を化学反応のみで製造しうる方法の提供。
【解決手段】N−アラルキルオキシカルボニル光学活性プロリンエステル誘導体を、水素還元して得られる光学活性プロリンエステル誘導体をホルミル化剤を用いてホルミル化した後、加水分解し、cis−N−ホルミル−α’−(2,4,6−トリエチルフェニル)−L−プロリンのような下記式(III)
(但し、R1は炭素数6〜12のアリール基を示す。)で示されるN−ホルミル光学活性プロリン誘導体を製造する。
(もっと読む)
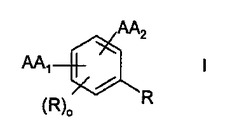
チロシナーゼ阻害剤
本発明は、式I(式中、置換基AA1、AA2、oおよびRは、請求項1で示した意味を有する)の化合物、ならびにその塩および溶媒和物および混合物、その調製方法、調製物ならびにその使用に関する。
 (もっと読む)
(もっと読む)
TAARリガンドとしての2−アゼチジンメタンアミン及び2−ピロリジンメタンアミン
本発明は、式(I)[式中、R1は、水素、場合によりハロゲンで置換されている、低級アルキルもしくはベンジル、又は低級アルコキシであり;R2は、水素、ハロゲン又はORであり、ここで、Rは、低級アルキル、アリール又は場合によりハロゲンで置換されている低級アルキルであり;R3は、水素又はフッ素であり;Arは、フェニルであり;nは、0又は1であり;oは、0、1又は2である]で示される化合物、及びその薬学的に活性な塩に関する。式(I)で示される化合物がトレースアミン関連受容体(TAAR)、特にTAAR1に対して良好な親和性を有することが見出されている。本化合物は、うつ病、不安障害、双極性障害、注意欠陥多動性障害(ADHD)、ストレス関連障害、精神障害、例えば統合失調症、神経障害、例えばパーキンソン病、神経変性障害、例えばアルツハイマー病、てんかん、偏頭痛、高血圧症、物質乱用及び代謝障害、例えば摂食障害、糖尿病、糖尿病合併症、肥満症、脂質代謝異常、エネルギーの消費及び同化の障害、体温恒常性の障害及び機能不全、睡眠及び概日リズムの障害及び心血管障害の処置に使用できる。 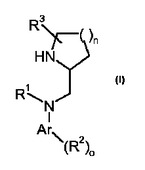 (もっと読む)
(もっと読む)
ヒストンデアセチラーゼ阻害剤としての4−カルボキシベンジルアミノ誘導体
本発明は新規類の4−カルボキシベンジルアミノ誘導体に関する。4−カルボキシベンジルアミノ化合物は癌を治療するために使用することができる。4−カルボキシベンジルアミノ化合物はヒストンデアセチラーゼを阻害することもでき、新生細胞の最終分化と細胞増殖停止及び/又はアポトーシスを選択的に誘導することにより、前記細胞の増殖を抑制するために使用するのに適している。従って、本発明の化合物は新生細胞の増殖を特徴とする腫瘍をもつ患者を治療するのに有用である。本発明の化合物は自己免疫疾患、アレルギー性疾患及び炎症性疾患等のTRX介在性疾患の予防及び治療と、神経変性疾患等の中枢神経系(CNS)疾患の予防及び/又は治療にも有用であると思われる。本発明は更に4−カルボキシベンジルアミノ誘導体を含有する医薬組成物と、遵守し易く、治療有効量の4−カルボキシベンジルアミノ誘導体がインビボで得られるこれらの医薬組成物の安全な投薬レジメンも提供する。 (もっと読む)
N−(ω−フルオロアルキル)環状アミン化合物の製法、並びに新規なN−(4−フルオロブチル)環状アミン化合物及びその製法
【課題】 本発明の課題は、簡便な方法により、N-(ω-フルオロアルキル)環状アミン化合物を得ることができる、工業的に好適なN-(ω-フルオロアルキル)環状アミン化合物の製法を提供することにある。本発明の課題は、又、新規なN-(ω-フルオロアルキル)環状アミン化合物であるN-(4-フルオロブチル)環状アミン化合物及びその製法を提供することにもある。
【解決手段】 本発明の課題は、フルオロアルカン化合物、環状アミン化合物及び塩基を反応させることを特徴とする、N-(ω-フルオロアルキル)環状アミン化合物の製法によって解決される。
(もっと読む)
ピペリジン/ピペラジン誘導体
本発明は、(A)
【化1】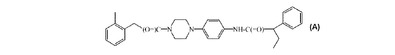
を除くことを条件として、如何なる立体化学異性体形態も包含する式(I)
【化2】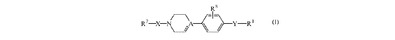
[式中、AはCHまたはNを表し、破線はAが炭素原子を表す場合の任意の結合を表し、Xは−C(=O)−、−O−C(=O)−、−C(=O)−C(=O)−、−NRx−C(=O)−、−Z1−C(=O)−、−Z1−NRx−C(=O)−、−C(=O)−Z1−、−NRx−C(=O)−Z1−、−S(=O)p−、−C(=S)−、−NRx−C(=S)−、−Z1−C(=S)−、−Z1−NRx−C(=S)−、−C(=S)−Z1−、−NRx−C(=S)−Z1−を表し、YはNRx−C(=O)−Z2−、−NRx−C(=O)−Z2−NRy−、−NRx−C(=O)−Z2−NRy−C(=O)−、−NRx−C(=O)−Z2−NRy−C(=O)−O−、−NRx−C(=O)−Z2−O−、−NRx−C(=O)−Z2−O−C(=O)−、−NRx−C(=O)−Z2−C(=O)−、−NRx−C(=O)−Z2−C(=O)−O−、−NRx−C(=O)−O−Z2−C(=O)−、−NRx−C(=O)−O−Z2−C(=O)−O−、−NRx−C(=O)−O−Z2−O−C(=O)−、−NRx−C(=O)−Z2−C(=O)−NRy−、−NRx−C(=O)−Z2−NRy−C(=O)−NRy−、−C(=O)−Z2−、−C(=O)−Z2−O−、−C(=O)−NRx−Z2−、−C(=O)−NRx−Z2−O−、−C(=O)−NRx−Z2−C(=O)−O−、−C(=O)−NRx−Z2−O−C(=O)−、−C(=O)−NRx−O−Z2−、−C(=O)−NRx−Z2−NRy−、−C(=O)−NRx−Z2−NRy−C(=O)−、−C(=O)−NRx−Z2−NRy−C(=O)−O−を表し、R1は場合によりシアノ、C1−4アルキルオキシ、C1−4アルキルオキシC1−4アルキルオキシ、C3−6シクロアルキルもしくはアリールで置換されていてもよいC1−12アルキル;C2−6アルケニル;C2−6アルキニル;C3−6シクロアルキル;アダマンタニル;アリール1;アリール1C1−6アルキル;Het1;またはHet1C1−6アルキルを表すが、但しYが−NRx−C(=O)−Z2−、−NRx−C(=O)−Z2−NRy−、−NRx−C(=O)−Z2−C(=O)−NRy−、−C(=O)−Z2−、−NRx−C(=O)−Z2−NRy−C(=O)−NRy−、−C(=O)−NRx−Z2−、−C(=O)−NRx−O−Z2−または−C(=O)−NRx−Z2−NRy−を表す場合にはまたR1が水素を表してもよいことを条件とし、R2は水素、C1−12アルキル、C2−6アルケニルまたはR3を表すが、但しXが−O−C(=O)−を表す場合にはR2がR3を表すことを条件とする]で表されるDGAT阻害剤、これのN−オキサイド、製薬学的に許容される塩または溶媒和物に関する。本発明は、更に、前記化合物を製造する方法、前記化合物を含有して成る製薬学的組成物ばかりでなく前記化合物を薬剤として用いることにも関する。
(もっと読む)
アズレン誘導体の製造方法及びアズレン誘導体
【課題】2位の電子吸引基、及び/又は、6位の電子供与性基の置換基のみを有しているアズレン誘導体を提供する。
【解決手段】アズレン又はアズレン誘導体の1位及び3位に置換基を付加する置換基付加工程と、置換基付加工程で置換基が付加されたアズレン誘導体の6位に臭素を付加する臭素付加工程と、6位に付加した臭素を電子供与性基に置換する置換工程と、を備え、下記構造式に示すアズレン誘導体を
【化1】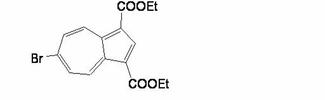
合成する。ここで、上記式において、P2は電子供与性基を示し、R1〜R7は、それぞれ独立して、水素原子又は任意の置換基を示す。
(もっと読む)
(メタ)アクリル酸エステルの製造方法
【課題】(メタ)アクリル酸エステルを簡易かつ高収率で得るための製造方法を提供する。
【解決手段】(メタ)アクリル酸またはそのエステルと、炭素数2〜4のアルキレン基を有するN置換ピロリドン誘導体とを、固体触媒の存在下で反応させて、エステル基末端にピロリドン基を有する(メタ)アクリル酸エステルを合成する段階を有する、(メタ)アクリル酸エステルの製造方法である。該固体触媒がイオン交換樹脂であることが好ましい。
(もっと読む)
41 - 60 / 115
[ Back to top ]



