Fターム[4H045GA10]の内容
Fターム[4H045GA10]に分類される特許
281 - 300 / 301
液体因子VII組成物のウイルス濾過
本発明は、液体因子VII組成物、特に活性因子VIIポリペプチド(因子VIIaポリペプチド)を含む組成物のウイルス安全性を向上させる新しい方法に関する。 (もっと読む)
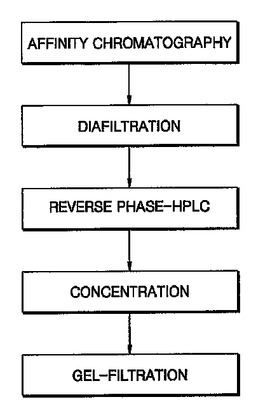
インターフェロン−βの精製方法
本発明は、親和性クロマトグラフィ工程および逆相高速液体クロマトグラフィ(RP−HPLC)工程を含む組換えヒトインターフェロン−β含有培養液からのヒトインターフェロン−βの精製方法であって、親和性クロマトグラフィ工程が、平衡化された親和性クロマトグラフィカラムにインターフェロン−β含有培養液を加えて吸着させた後、平衡用緩衝溶液で洗浄する段階と、30〜60重量%のプロピレングリコールを含有するpH6.5〜7.5の洗浄用緩衝液A、および10〜30重量%のプロピレングリコールおよび1〜2MのNaClを含有するpH6.5〜7.5の洗浄用緩衝液Bでカラムを洗浄する段階と、40〜60重量%のプロピレングリコールおよび1〜2MのNaClを含有するpH6.5〜7.5の緩衝溶液でヒトインターフェロン−βを含有する画分を溶出させる段階とを含む、ヒトインターフェロン−βの精製方法を提供する。
 (もっと読む)
(もっと読む)
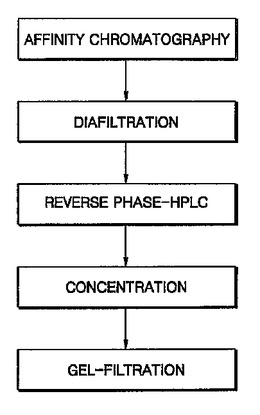
インターフェロン−βの精製方法
本発明は、親和性クロマトグラフィ工程および陽イオン交換クロマトグラフィ工程を含む組換えヒトインターフェロン−β含有培養液からのヒトインターフェロン−βの精製方法であって、親和性クロマトグラフィ工程が、平衡化された親和性クロマトグラフィカラムにインターフェロン−β含有培養液を加えて吸着させた後、平衡用緩衝溶液で洗浄する段階と、30〜60重量%のプロピレングリコールを含有するpH6.5〜7.5の洗浄用緩衝液A、および10〜30重量%のプロピレングリコールおよび1〜2MのNaClを含有するpH6.5〜7.5の洗浄用緩衝液Bでカラムを洗浄する段階と、40〜60重量%のプロピレングリコールおよび1〜2MのNaClを含有するpH6.5〜7.5の緩衝溶液でヒトインターフェロン−βを含有する画分を溶出させる段階とを含む、ヒトインターフェロン−βの精製方法を提供する。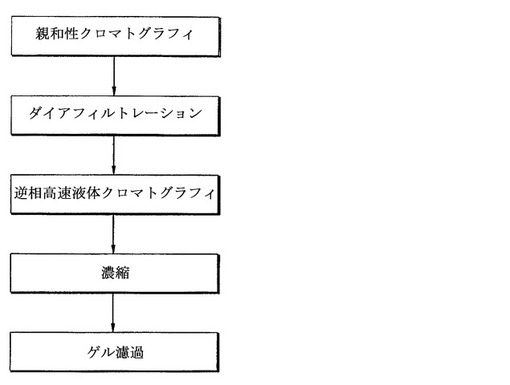
 (もっと読む)
(もっと読む)
IL−18結合タンパク質の精製方法
本発明は、疎水性電荷誘起クロマトグラフィーを含む、液体からのIL−18結合タンパク質(IL−18BP)の精製方法に関する。 (もっと読む)
グリコペプチドホスホン酸誘導体の塩酸塩
約2.4重量%〜4.8重量%の塩素イオン含量を有するテラバンシン塩酸塩が、開示される。開示された塩は、他の塩酸塩と比較して周辺温度での安定性を改善した。またそのような塩を調製するためのプロセスもまた、開示される。1つの実施形態では、本発明は、約2.4重量%〜約4.8重量%の塩素イオン含量を有するテラバンシン塩酸塩に関する。さらに別の実施形態では、本発明は、テラバンシン塩酸塩および水性溶媒系を含み、その組成物のpHが、約2.5〜約5.0の範囲にある組成物に関する。 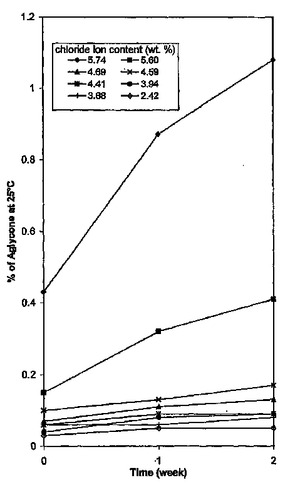 (もっと読む)
(もっと読む)
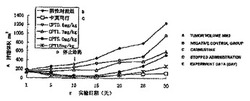
抗癌作用を有する組換えタンパク質、それをコードする遺伝子、及びそれらの使用
【課題】抗癌作用を持つ組換えタンパク質、そのコード遺伝子、およびそれらの用途を提供すること。
【解決手段】(1)配列番号2のアミノ酸配列を有するタンパク質と、(2)配列番号2との配列相同性が90%を超え、同等の活性を有する、配列番号2に由来するタンパク質と、(3)配列番号2のアミノ酸配列のN末端での15個以下のアミノ酸残基の付加または欠失によって得られ、同等の活性を有する、配列番号2に由来するタンパク質と、(4)配列番号2のアミノ酸配列のC末端での15個以下のアミノ酸残基の付加または欠失によって得られ、同等の活性を有する、配列番号2に由来するタンパク質と、(5)配列番号2のアミノ酸配列にある1個または数個のアミノ酸残基の置換、欠失、または付加によって得られ、同等の活性を有する、配列番号2に由来するタンパク質とからなる群から選択される組換えタンパク質である。
(もっと読む)
カルボキシペプチダーゼUの阻害が有用な疾患を治療するための環状アナベノペプチン型のペプチドの使用、新規アナベノペプチン誘導体、および、それらの中間体
カルボキシペプチダーゼUの阻害が有用である状態を治療または予防するための医薬品を製造する方法における、式(I):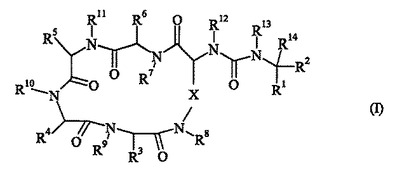
で示される化合物;具体的な式(I)で示される化合物、および、式(I)で示される化合物を含む組成物、および、製薬上許容できるアジュバント、希釈剤またはキャリアーの使用。 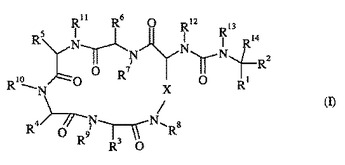 (もっと読む)
(もっと読む)
活性炭処理
本発明は、活性炭処理を用いる化合物の精製方法に関する。本発明に係る方法では、マトリックス中に固定された活性炭の入ったいくつかのフィルターユニットは、逐次的にかつ向流モードで動作する。好適な体積の供給物を通した後、第1のシリーズのフィルターユニットから特定の位置番号のフィルターユニットを取り外しかつ追加のフィルターユニットを他の特定の位置番号に結合することにより次のシリーズのフィルターユニットを得て、それに次の体積の供給物を通して処理を継続させる。この方法により、従来の活性炭処理時に見られたような精製化合物の収率損失の問題が克服される。 (もっと読む)
粒状金属酸化物を用いるプリオン排除
ヒュームド金属酸化物および/または粒状二酸化珪素を生物学的物質に加えてヒュームド金属酸化物および/または粒状二酸化珪素並びに生物学的物質の混合物を含んでなる溶液を得、そしてヒュームド金属酸化物および/または粒状二酸化珪素を混合物から分離して生ずる溶液を形成せしめることにより生物学的物質を含有する溶液を製造する方法であって、生物学的物質を汚染する可能性のある病原性プリオン蛋白質を生ずる溶液中で実質的に減少させる方法。  (もっと読む)
(もっと読む)
インターフェロンβ複合体
本発明は、高い生物活性を有するインターフェロンβとポリエチレングリコールとの複合体、及びこれを高効率で製造するための方法に関する。すなわち、本発明は、糖単位の数が5以下の少糖類及び単糖類、これらの糖アルコール、並びに炭素数2乃至6の多価アルコールから成る群より選ばれる少なくとも1種の添加剤存在下で、インターフェロンβとポリエチレングリコールとを結合させることを特徴とするインターフェロンβ複合体の製造方法、及び該方法によって製造される、インターフェロンβのアミノ酸配列の19番目、あるいは134番目のリジンに特異的にポリエチレングリコールが結合したインターフェロンβ複合体に関する。 (もっと読む)
組換えルブリシン分子およびその使用
組換えルブリシン分子およびその使用。新規の組換えルブリシン分子、ならびに、例えば、滑膜関節部、半月板、腱、腹膜、心膜および胸膜のための潤滑剤、抗付着剤および/または関節内助剤としてのそれらの使用を提供する。 (もっと読む)
亜麻タンパク質単離物の調製方法
亜麻油種子をそこから粘液を除去するため最初に抽出した後、粉砕して油を回収し、粕を生成する手順で、亜麻タンパク質単離物を得る。次いで、この亜麻タンパク質粕を処理して、そこから亜麻タンパク質単離物を回収する。 (もっと読む)
癌及び感染症の免疫療法のための組成物及び方法
本発明は、対象における免疫応答を刺激するための、及びインターロイキン12(IL−12)治療の代替として使用するための、原発性腫瘍疾患、転移性腫瘍疾患及び感染症の予防及び治療のための組成物及び方法を提供する。詳細には本発明は、免疫刺激活性を有することから、癌及び感染症の治療及び予防並びに免疫変調に用途を有するアピコンプレックス関連タンパク質(ARP)を提供する。ARPを含む組成物が提供される。インターロイキン12(IL−12)治療の代替として使用するための、及び対象における免疫応答を誘発するための、癌及び/又は感染症を予防及び/又は治療するためのARPの使用方法も提供される。 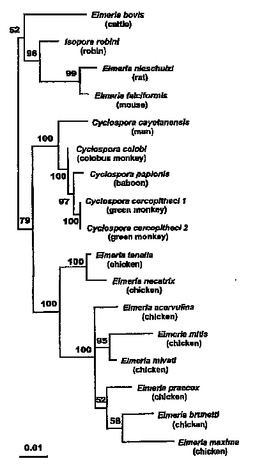 (もっと読む)
(もっと読む)
HER−2変異体の精製
【課題】HER-2変異体の精製
【解決手段】本発明は、昆虫細胞の培養物から得られたEGFR ファミリータンパク質を精製する新規の方法を提供する。該方法は、a) ダイアフィルトレーション及び培養培地のバッファーによる交換、b)固定化金属親和クロマトグラフィー(IMAC)、C)サイズ排除クロマトグラフィー(SEC)、及び、d)陰イオン交換クロマトグラフィー(AIE)、という一連の工程を具備する。該方法はまた、前記精製方法が特に適した、HER-2タンパク質の免疫原性変異体のための方法を提供し、並びに、該変異体の製剤のための方法を提供する。
(もっと読む)
アンジオテンシン変換酵素阻害ペプチド含有組成物
天然原料よりACE阻害活性に優れたペプチド及びその製造法を提供する。 大豆中の微量蛋白質である大豆ホエー蛋白質を基質にしてプロテアーゼで分解することにより、大豆の主要な貯蔵蛋白質であるβ−コングリシニンやグリシニンを基質としたペプチドよりもACE阻害活性が高いペプチドを得られることを見出し、これに基づき本発明を完成するに至った。 (もっと読む)
グループ1ダニポリペプチド変異型
本発明は、変異型の成熟ポリペプチドが下記から成る位置または前記位置に対応する1または2以上の突然変異を含んでなる、グループ1ダニポリペプチドの変異型に関する: 配列番号1のA10、A12、E13、G29、G30、G32、A46、Y47、S54、L55、D64、A66、S67、G73、T75、I80、Q84、N86、G87、S92、Y93、Y96、A98、R99、E100、Q101、R104、R105、P106、Q109、R110、F111、G112、I113、A132、I144、K145、D146、D148、R151、I158、I159、Q160、R161、D162、N163、G164、Y165、Q166、N179、A180、G182、V183、D184、A205、I208または成熟Der p 1ポリペプチドの10、12、13、29、30、32、46、47、54、55、64、66、67、73、75、I80、84、86、87、92、Y93、96、98、99、100、101、104、105、106、109、110、111、112、113、132、144、145、146、148、151、158、159、160、161、162、163、164、165、166、179、180、182、183、184、205、208。 (もっと読む)
薬剤製品のための抽出プロセス
海洋無脊椎動物から可溶天然コラーゲンを単離する一つのプロセスであって、以下のステップ、1)天然コラーゲン原線維を可溶化するために、海洋無脊椎動物のコラーゲン含有部分を弱酸液で処理し、2)組織微粒子を除去するために生成スラリーを遠心分離し、3)塩基の追加でコラーゲンを沈殿させるために上澄のpHを調節し、4)沈殿コラーゲンを収集し、5)沈殿コラーゲンを再懸濁し、また、6)限外濾過膜を使用して水に対する緩衝液交換を実施する、ことより成るプロセス。 (もっと読む)
がん治療のためのペプタボディ
本発明は、単離された組み換え融合ペプタボディに関し、該ペプタボディは、特定の腫瘍細胞の成長阻害に有用な上皮成長因子受容体のメンバーに結合する。また、前記単離された組み換え融合ペプタボディをコードする核酸、前記単離された組み換え融合ペプタボディを活性物質として含むキットおよび医薬組成物が開示される。さらに、前記単離された組み換え融合ペプタボディの製造方法、ならびに、がんを治療または予防するための薬剤の調製のための使用が提供される。 (もっと読む)
ヘモシアニンの単離プロセス
軟体動物ヘモシアニンの実質的に単一の安定した溶液を獲得するためのプロセスであって、ここで前記プロセスが、(1)軟体動物からの血液の回収、(2)血清画分を獲得するために行う、細胞物質と他の微粒子を除去するための回収された血液の遠心分離、(3)限外ろ過膜を使用した、血清液を陽イオン交換平衡バッファーと置換するための血清画分のダイアフィルトレーション、(4)pHが4.0から6.5の間、平衡バッファーの存在下での血清画分の強陽イオン交換樹脂への接触、それにより血清画分のタンパク質成分がカラムに保持される、(5)高塩濃度溶出バッファーを用いたカラムからの保持されたタンパク質成分の溶出、(6)溶出液の濃縮と、ダイアフィルトレーションバッファーの存在下での限外ろ過膜を通した溶出液の再循環による、溶出バッファーのpH中性/低塩ダイアフィルトレーションバッファーへの交換、のステップを含むことを特徴とするプロセス。 (もっと読む)
長い生体内半減期を有する生理活性ポリペプチド結合体
【課題】 生理活性ポリペプチドの活性減少を最小化しながらも、生体内半減期を延長させ、免疫反応を誘発しないタンパク質結合体の提供。
【解決手段】 i)生理活性ポリペプチド、ii)非ペプチド性重合体、およびiii)免疫グロブリンを含む、前記生理活性ポリペプチドの生体内半減期が延長されたタンパク質結合体は、免疫反応の誘発可能性を減らしながらも、向上した生体内安定性および延長された血中半減期を有するためポリペプチド薬物の開発に有用である。
(もっと読む)
281 - 300 / 301
[ Back to top ]