Fターム[2G054GB02]の内容
化学反応による材料の光学的調査・分析 (27,357) | 検出手段 (1,447) | 蛍光光度計 (517)
Fターム[2G054GB02]に分類される特許
441 - 460 / 517
サイトメガロウイルスの検出および定量方法
【課題】 一定温度、一段階操作で、迅速にCMV由来のβ2.7遺伝子のmRNAを増幅、検出することを特徴とする、CMVの検出および定量方法の提供。
【解決手段】 CMV由来のβ2.7遺伝子のmRNAを、特異的に増幅可能なオリゴヌクレオチドプライマーの組み合わせを利用し、これらのオリゴヌクレオチドプライマーの組合せからなるRNA増幅工程を、インターカレーター性蛍光色素で標識されたオリゴヌクレオチドプローブを用いて測定する検出法によって、前記課題を解決する。
(もっと読む)
慢性C型肝炎患者における肝臓線維化進行速度を予測するための方法およびキット
個体が肝臓線維化の早い進行速度を示す素因を有するかどうかを明らかにする方法およびキットが提供される。肝臓線維化の早い進行を防止するのに有用な薬剤および医薬組成物、並びに肝臓線維化を加速または誘導させる薬物分子を同定する方法も提供される。 (もっと読む)
ハイブリダイゼーションなどの相互作用を検出する方法及び検出部、該検出部を備えるバイオアッセイ用基板、ハイブリダイゼーションなどの相互作用を検出する装置、並びに試薬キット
【課題】
(1)反応領域内の固相表面に対する核酸・インターカレーターなどの非特異的吸着の防止、(2)ハイブリダイゼーションの検出に用いるインターカレーターの結合特性の長時間保持、(3)ハイブリダイゼーション検出の際の洗浄工程の省略。
【解決手段】
反応領域R内に、塩を含むHEPES緩衝液Sを貯留又は保持させる相互作用検出方法を提供する。緩衝液Sの塩濃度を調整することにより、正に帯電した固相表面11aに対する、核酸(D、T)、インターカレーターの非特異的吸着を防止する。また、反応領域Rと、反応領域R内に貯留又は保持され、塩を含むHEPES緩衝液Sを含有する媒質Mと、を少なくとも備える相互作用検出部1、該相互作用検出部1を備えるDNAチップを含むバイオアッセイ用基板、及び、ハイブリダイゼーションなどの相互作用を検出する装置を提供する。その他、塩を含むHEPES緩衝液などを含む試薬キットを提供する。
(もっと読む)
悪性腫瘍の診断のための試薬および診断方法
【課題】
がん特異抗原のタンパク質を測定するがんマーカーは、臓器特異的で悪性腫瘍として一括して診断できない。多数のタンパク質を同時に検出し複数のがんを一括診断する診断チップもあるが、複数のタンパク質を測定する必要があり、扱い方が煩雑で、肉腫等のがんとは発生の母地が異なる悪性腫瘍について測定できない。がん被検体の体内で発生する主要な酵素を目印とするタンパク質を指標にした試薬もあるが、酵素は活性を失い易く、肉腫等は測定できない。本発明はこのような問題点を課題とする。
【解決手段】 本発明は、抗PCNAポリクロ−ナル抗体と特異的に相互作用する、SDS−PAGE上での分子量がPCNAよりも大きなタンパク質またはその改変体、ならびにそれに特異的に相互作用する因子、それらを使用した、キット、組成物、方法を提供する。
(もっと読む)
生体関連物質用試験片の製造方法、及び試験装置
【課題】 本発明は、試験片ごとにプローブ固相化率が異なる複数の試験片を使用する場合であっても、プローブに対して特異的に反応する試料物質を精度良く検出、定量することを可能にする生体関連物質用試験片の製造方法を提供することを課題とする。
【解決手段】 反応用のプローブとあわせて固相化する、固相化率検査用のプローブの固相化率についての情報を、試験片の情報保存部に保存する。
(もっと読む)
遺伝子検査方法
【課題】 安価かつ簡便な操作で複数変異領域(SNP)の検査が可能な遺伝子検査方法を提供し、臨床現場における遺伝子診断を現実のものとすること。
【解決手段】 検出すべき配列(SNP領域)に相補的な配列を含むプローブを表面に固定した支持体に対し、5’末端にアンカー配列を有する試料核酸をハイブリダイズさせる工程と、前記試料核酸を鋳型として前記プローブの相補鎖伸長反応を行う工程と、前記伸長反応で合成された前記プローブ伸長鎖から前記試料核酸を解離させ、除去する工程と、解離した前記プローブ伸長鎖を鋳型として、前記アンカー配列と同じ配列を有するプライマーを用いて、相補鎖伸長反応を行う工程と、前記プライマーの伸長反応によって生じるピロリン酸を生物化学発光により検出することにより、前記試料核酸のSNP型を判定する。
(もっと読む)
複数のドナー及びアクセプターを有する蛍光標識試薬
容易に調製し得る色素構築ブロックに基づき、またそれから合成した新規分類の蛍光共鳴エネルギー移動(FRET)標識試薬を提供する。この標識試薬は「カセット」の形状をとり、広範囲の多様な生体物質その他に結合し得る。標識試薬は少なくとも2つの蛍光色素部分を含んでなり、その色素部分はリンカー基を介して共有結合しており、また、試薬を標的に結合させる標的結合基をもつ。エネルギー移動標識試薬は共有結合又は非共有結合により標的物質に結合し得る。色素は、第一(又はドナー)色素の発光スペクトルが第二色素の吸収スペクトルと重なり合い、それによって両色素間にエネルギー移動が起こるようにする。色素構築ブロックは、構造(I)の4′,5′−ビス−アミノメチル−フルオレセイン及び/又はその5(6)−カルボン酸である。単一ドナーと単一アクセプター蛍光色素からなる本発明の態様に加えて、本発明による蛍光エネルギー移動標識試薬は、さらに1個以上の第三の蛍光色素を含んでもよく、各々第一又は第二蛍光色素に共有結合して第三の吸収及び発光を示す。 (もっと読む)
ウイルス感染の検出のための方法と装置
この出願は、一般に、複合化技術、例えば、スライドに基づく、マイクロタイタープレートに基づく、及び膜に基づく、マイクロアレイ及びビーズの技術を用いた、ウイルス感染の高処理量の、再現性のある、そして安価な検出のための装置及び方法に関する。上記装置と方法は、多数の試験サンプル中の多重ウイルス感染の同時検出を許容する。 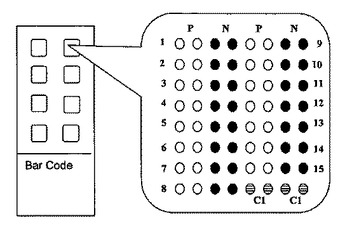 (もっと読む)
(もっと読む)
マクロおよびミクロマトリックスの迅速な検出および定量方法および装置
【課題】サンプル中の検体の存在を迅速に検出する方法と装置を提供すること。
【解決手段】検体と検体代謝産物を検出可能なマーカーを有し検体と検体代謝産物に迅速に結合する試薬を含む容器に導入し、ついでサンプルを載置領域12、分離領域14および読取領域16を有する検定装置10の載置領域に導入し、好ましくは毛管作用により読取領域に移動する。検出手段が検体および検体代謝産物を検出する。サンプルを制御された漸進的断片化のための力適用手段にかけて好ましくは病原体であるサンプルを複数の断片にする。試薬を収容した検定装置は結合試薬を含有する試験点を読取部分に印刷してある。断片が試験点に結合すると、検体断片の存在が既知の方法で決定できる。試験点は細菌等の病原体である検体または検体による代謝産物を含んでいてもよい。レーザー回折による背景干渉は除去する。
(もっと読む)
蛍光分析を用いて有機染料の光触媒分解を測定する方法
【課題】本発明は、蛍光分析によって光触媒活性の表面における有機染料の光触媒分解を定量化する方法に関する。
【解決手段】本発明の目的を達成するために、検査される光触媒及び光触媒非活性参照物は、有機染料によってコーティングされる。そして、このサンプルは、強度及びスペクトル分布既知の紫外線又は可視光線に照射される。蛍光強度は、照射の前後及び機械の構成によって照射中にも、蛍光スキャナ、チップリーダー又は蛍光顕微鏡によって検出される。染料にもコーティングされ、光触媒非活性参照物(例えば、石英)に比べて、染料にコーティングされた光触媒のその後の蛍光減少が、検査されているサンプルの光触媒効率の量的な測定値としてみなされる。
(もっと読む)
微小球におけるウィスパリングギャラリーモードを使用するバイオセンサー
標的分析物の存在を検出するためのバイオセンサーが開示される。バイオセンサーは、微小回転楕円状粒子から形成され、その表面上に固定される標的分析物に対する結合パートナーを有した。結合パートナーは、ヌクレオチド;ペプチド、タンパク質、酵素、抗体などであり得る。分析物がそのパートナーに結合する場合、微小回転楕円状粒子のウィスパリングギャラリーモード(WGM)プロファイルは、プロファイルピークが赤または青シフトするように変化する。固定化結合パートナーは、それらが蛍光、リン光、白熱光などを放出するように、フルオロフォアなどを含み得る。これらのフルオロフォアは、ナノ結晶または量子ドットの形態を取り得る。 (もっと読む)
細胞内病原体の検出法および定量化法
本発明は、生物学的試料において、クラミジア科(Chlamydiaceae)の細菌を検出するための方法および組成物を提供する。方法には、例えばクラミジア感染血液細胞の表面上に提示されるクラミジア抗原に特異的に結合する抗体と、生物学的試料を接触させる工程;および蛍光顕微鏡観察またはフローサイトメトリーを用いて試料を分析して、結合している抗体を検出する工程が含まれる。 (もっと読む)
RNAリガンドを含むナノ粒子
金属および/または半導体原子を含有するコアを有し、そのコアが、RNAリガンドを含む複数のリガンドと共有結合しているナノ粒子を作製するための材料および方法を提供する。RNAリガンドはsiRNAまたはmiRNAを含み得る。また、治療および診断におけるこれらのナノ粒子の使用も提供する。 (もっと読む)
医療デバイスの細胞結合特性を定量する方法
本発明は、医療デバイスの細胞結合特性を定量するための方法を提供する。この方法を実施する際、少なくとも1つの型の結合因子を有する医療デバイスが、その医療デバイスにおけるその結合因子について親和性を有するリガンドを発現する細胞とともにインキュベートされる。上記医療デバイスに結合する細胞は、少なくとも1つのマーカーで標識される。このマーカーが、検出され、そして上記医療デバイスに結合している細胞の量が、決定される。あるいは、上記少なくとも1つの型の結合因子に対する親和性を発現する少なくとも1つの型のリガンドを有する標識された細胞が、提供され得、この細胞は、上記医療デバイスとともにインキュベートされる。上記結合因子に対する親和性を有する細胞株上での上記リガンドの相対的発現もまた、決定される。  (もっと読む)
(もっと読む)
単分子増幅及びDNA長の検出
核酸の検出、定量及び統計分析のために単分子増幅を実施するための方法及びシステムを提供する。対象核酸長を判定及び定量するための方法及びシステムも提供する。 (もっと読む)
完全自動化したモノクローナル抗体による広範な識別法
この生物試料中の細胞集団を計数するのに有用な方法は、単一反応混合物中で試料、第一の発光スペクトルを有する蛍光色素で標識した第一の抗体、および追加の抗体を反応させるステップを含む。この第一の抗体は、白血球および非白血球上で違った形で発現される抗原決定基と結合する。この追加の抗体は、成熟および未熟顆粒球または骨髄細胞上で違った形で発現する抗原決定基と結合し、上記第一の蛍光色素か、または上記第一の発光スペクトルと識別できる発光スペクトルを有する追加の蛍光色素のいずれかで標識される。この反応混合物は、第一または追加の発光スペクトルの一方と部分的に重なり合う発光スペクトルを有する核酸色素と混ぜ合わせることができる。この反応混合物は、非有核赤色血液細胞をそれぞれ違った形で溶血し、かつ白血球を保存する溶血系で処理することができる。血液学的細胞の集団は、それぞれの集団について少なくとも2つのパラメータ(蛍光、光学的、および電気的)を用いて検出され、計数される。 (もっと読む)
ヒト化FcγRIIB特異的抗体とその利用法
本発明は、FcγRIIAと結合するよりも高い親和性でヒトFcγRIIBと結合するヒト化FcγRIIB抗体、そのフラグメントおよび変異体に関する。本発明は、本発明のヒト化抗体を、Fc受容体介在性シグナル伝達のバランスの低下に関連した疾患(例えば癌、自己免疫疾患、および炎症性疾患)を治療するために使用することを包含する。本発明は、治療用抗体のエフェクター機能を高めるために本発明のヒト化抗体を投与することにより治療用抗体の治療効果を増大する方法を提供する。本発明はまた、本発明のヒト化抗体をワクチン組成物とともに投与することによりワクチン組成物の効力を増大する方法も提供する。本発明は、自己免疫疾患を治療する方法およびFcγRIIBを発現する癌細胞を除去する方法を包含する。 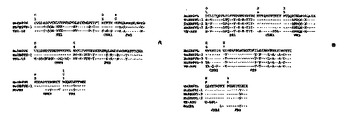 (もっと読む)
(もっと読む)
分子相互作用を検出する装置および方法
本発明はプローブ分子と標的分子との間の特異的相互作用を検出する装置および方法に関する。特に、本発明は、a)装置の第1の表面上に配置され、プローブ分子がアレイ要素上に固定化された、基材を有するマイクロアレイと、b)マイクロアレイがその上に配置された第1の領域と第2の表面との間に画定された反応チャンバとを備え、マイクロアレイと第2の表面との間の距離が修正可能である、プローブ分子と標的分子との間の分子相互作用を定性的および/または定量的に検出する装置に関する。  (もっと読む)
(もっと読む)
ランタニド・キレートと、バイオアッセイにおけるその使用
本発明は、バイオ分子の定性及び定量測定のための蛍光分析法に用いられる、新規な化学化合物に関する。本発明の目的は、このような化合物を同定し、その適合性を実証することである。該目的は、式(1)で示される化合物[式中、R1はアンテナ官能基であり、R2は、共役ランタニド(III)イオンを含有するキレート形成剤であり、Xは、−OH又は、アミド結合によってキレート形成剤のカルボキシレート基に結合した、バイオ分子に対するアフィニティ基であり、Yは、−H又は、アンテナ官能基にカップリングした、バイオ分子に対するアフィニティ基である]によって達成される。
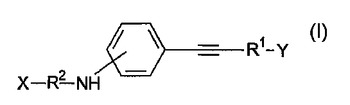 (もっと読む)
(もっと読む)
ncRNAを検出する方法
ncRNA分子の新規な検出方法を記載する。開示する方法は、検出miRNA及びsiRNAに特に有用である。この方法は、試料中に存在するncRNA分子のプロファイルを作成するのに使用し得る。また、本開示の方法を用いて、所与の疾病又は症状に対するncRNA固有性を創成し得る。ncRNA固有性は、診断目的、治療目的及び創薬目的、並びに他の用途に使用し得る。  (もっと読む)
(もっと読む)
441 - 460 / 517
[ Back to top ]