Fターム[4B063QQ79]の内容
酵素、微生物を含む測定、試験 (178,766) | 検体,検出物 (39,509) | 酵素,核酸以外の有機物質 (4,619) | 蛋白質,ペプチド,その構成成分,その誘導体 (2,970)
Fターム[4B063QQ79]の下位に属するFターム
アミノ酸 (75)
Fターム[4B063QQ79]に分類される特許
1,921 - 1,940 / 2,895
哺乳類における炎症を軽減するための乳酸菌の選択及び使用
腸疾患などの炎症を軽減する能力のために選択された乳酸菌の菌株、かかる菌株を選択する方法及びかかる菌株を含む生成物。 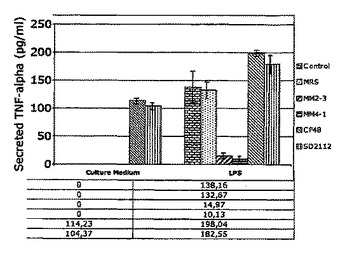 (もっと読む)
(もっと読む)
DNA結合性物質の同定方法及び検査対象物質のDNA結合能検定方法
【課題】新規なDNA結合性物質を迅速に同定し、また、公知のDNA結合性物質におけるDNA結合能を迅速に評価する方法を提供する。
【解決手段】ゲノム配列を断片化したDNA断片を基板上に固定してなるビーズに、プローブをハイブリダイズさせる工程と、検査対象物質を含む溶液を上記ビーズに接触させる工程と、上記ビーズを洗浄する工程と、上記DNA断片と上記プローブとハイブリダイズした領域に上記検査対照物質が結合してなるビーズを、上記検査対象物質が結合してないビーズとを分離する工程とを含むDNA結合物質の同定方法。
(もっと読む)
癌関連遺伝子(PRLR)
本発明は、癌関連遺伝子の分野にある。特に、本発明は、PRLR遺伝子またはタンパク質の発現の存在または不存在に基づいて癌または癌発現の可能性を検出する方法に関する。本発明は、PRLR遺伝子発現およびPRLRタンパク質活性をアップレギュレートまたはダウンレギュレートするための方法および分子も提供する。1つの実施形態において、本発明は、PRLR遺伝子の配列または発現レベルを決定する工程を含む、生体サンプル内で癌性細胞を検出する方法を提供する。この方法では、生物学的サンプルは、乳房、前立腺、肺または皮膚組織を含む。 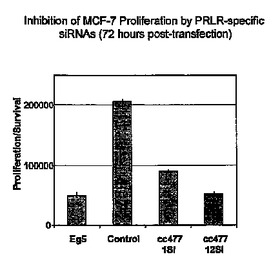 (もっと読む)
(もっと読む)
スクリーニングアッセイ
本発明は、タンパク質、ペプチドまたはそれらのフラグメントの不均質サンプルを分析するための方法を提供し、この方法は、(a)アレイ上の間隔をあけて離れた規定された位置に各クラスのメンバーを結合させることによって、タンパク質もしくはペプチドまたはそれらのフラグメントの不均質サンプルを不均質なクラスに分離するステップであって、各クラスのメンバーが、そのクラスに共通するモチーフを有するステップ;および(b)各クラス中のタンパク質またはペプチドもしくはそれらのフラグメントを特性決定するステップを含む。 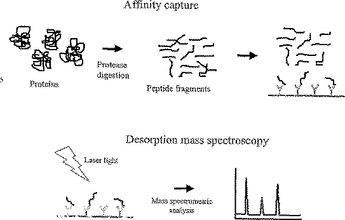 (もっと読む)
(もっと読む)
抗カビ剤のスクリーニング方法
【課題】シグナル伝達系作動性抗真菌剤の高速かつ高効率なスクリーニング系評価系を提供すること。
【解決手段】真核糸状真菌におけるMAPキナーゼ経路の活性化作用又は阻害作用を有する試験物質のスクリーニング方法であって、真核糸状真菌をMAPキナーゼ経路が活性化される通常の条件下で試験物質に暴露させ、該暴露によるMAPキナーゼ経路に関連する遺伝子の転写量の変化を検出し、該MAPキナーゼ遺伝子の転写量の増加又は減少が該試験物質のMAPキナーゼ経路の活性化作用又は阻害作用を示すものである、前記方法、及び、該スクリーニング方法を実施するために使用する各種キット。
(もっと読む)
分子細胞遺伝学的方法を用いる癌連鎖遺伝子および治療標的の確認
特定の遺伝子、とりわけ特異的な染色体領域に地図化される遺伝子の発現について潜在的な治療薬の調節に基づいて、抗腫瘍薬などの潜在的治療薬を同定する方法が開示される。更にこのような遺伝子の発現、または発現パターンの結果として、癌または潜在的癌状態を診断する方法も開示され、これは癌検出、およびまたは診断するために、前記遺伝子またはセットの遺伝子群での遺伝子コピー数水準およびまたは増幅水準での変化を検出することを含む。機能的に関連する遺伝子を検出または測定する方法並びにそのような遺伝子の発現産物の標的化に基づく癌を処置し、癌過程に伴なう遺伝子を決定する方法、および処置に対する癌患者の成功、応答率および生存統計も本発明に含まれる。更に各種癌組織型で確認遺伝子/薬剤標的としてこれらの遺伝子の同定に基づく臨床試験/処置の発生前に、薬力学/薬理遺伝学/代理マーカーとしてまたは患者プロファイリングのために、これら対象領域(ROIs)の発現調節を測定することに関連する方法も含まれる。 (もっと読む)
腎機能測定剤
【課題】 腎疾患患者において腎硬化性病変の進行に関与する腎内RAS活性を知るための臨床的指標として、さらには、同疾患患者にAII阻害薬を投与する際にその至適投与量を知る臨床指標として有用なヒト尿中アンジオテンシノーゲンの測定剤の提供。
【解決手段】ヒトレニンを含む、ヒト尿中アンジオテンシノーゲン測定剤。
(もっと読む)
骨芽細胞分化に関連する遺伝子発現
本発明はプレ骨芽細胞性細胞が分化を起して成熟骨芽細胞になる時に発現パターンが変化する遺伝子を確認する。この確認された遺伝子は分化プロセスのマーカーとして使用できる。本発明はまた分化のプロセスを変調することのできる試薬をスクリーニングする方法も提供する。本発明はまた確認された遺伝子1個又はそれ以上の発現を分析することによって骨形成を刺激する治療剤を確認する方法も提供する。 (もっと読む)
グレリン結合核酸
本発明は、好ましくはグレリンに結合する核酸に関し、この場合、核酸は、
第一のストレッチBoxAおよび第二のストレッチBoxBを含み、ここで、第一のストレッチBoxAは約25個の連続ヌクレオチドを含み、第二のストレッチBoxBは約6〜8個の連続ヌクレオチドを含み、ここで、第一のストレッチBoxAのヌクレオチドの3’末端ストレッチは、第二のストレッチBoxBとハイブリダイズし、このハイブリダイゼーションでは、第一の二本鎖構造が形成され、そしてそのような第一の二本鎖構造がバルジを含む。 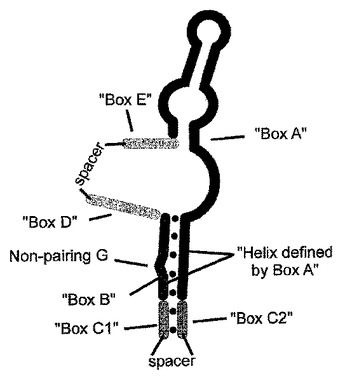 (もっと読む)
(もっと読む)
POP2NFkB阻害ポリペプチド、核酸および使用方法
本発明は新規のpyrin-only蛋白質(POP2)、ポリペプチド、これらをコードする核酸、およびこれらを製造および使用する方法を提供する。本発明のポリペプチドは核因子kB(NF-kB)調節活性を有する。NF-kBは、細胞周期制御、サイトカインおよび接着分子遺伝子のトランス活性化に重要であり、多くの癌、神経変性障害において異常な制御がなされている。Pyrinおよび/またはカスパーゼリクルートメント(CARD)ドメインを有する蛋白質は、アポトーシス、先天性免疫および炎症において役割を果たす。多くのpyrinドメイン蛋白質は、NF-kB活性を調節し、核周辺の「アポトーティックスペック」およびプロIL1β/IL-18転換インフラマソーム複合体の両方の集合に参加する。「Pyrin-only」蛋白質は、pyrinドメインが仲介する機能の負のレギュレーターとして魅力的であり、そのような蛋白質のうちの1つとしてPOP1が報告されてきた。本発明者は、第二のPyrin-only蛋白質(POP2)を示すものである。POP2は、97アミノ酸蛋白質をコードし、ヒト3番染色体に位置する294ntの単一エキソン遺伝子であり、その他のpyrinドメインと構造的類似性を有すると予測される。CATERPILLER(CLR、NLR、NALP)ファミリー蛋白質中のpyrinドメインに非常に類似しているPOP2は、原型のPyrinおよびASC pyrinドメインではないようである。POP2は主に末梢血白血球において発現しており、トランスフェクションを行った細胞において細胞質および核両方の発現パターンを示す。TNFα刺激性およびp65(RelA)誘導性のNF-kB依存的遺伝子転写は、NF-kBの核内輸送または分布の変化に関連するメカニズムによって、インビトロでPOP2により阻害される。核周辺スペックにおいてASCと一緒に位置するが、POP2はまたCLR蛋白質CIAS1/NALP3によるスペックの形成も阻害する。これらの観察は、POP2が、Pyrinドメイン依存的複合体の集合に影響を及ぼし得るNF-kB活性の負のレギュレーターであることを示唆するものである。  (もっと読む)
(もっと読む)
金属表面修飾セラミックス系スキャフォールドとその用途
【課題】多様な細胞種に適応可能なスキャフォールドの提供
【解決手段】セラミックスからなる基材とその表面に固定化された金属粒子とを有するスキャフォールド;該スキャフォールドの作製方法;該スキャフォールドを用いた細胞および組織の培養方法;細胞に結合し得る物質のスクリーニング方法;試料から特定の細胞を回収する方法等を提供する。
(もっと読む)
癌に関連した遺伝子(PTPε)
本発明は、癌関連遺伝子の分野に属する。特に、tm−PTPε遺伝子またはこの遺伝子によってコードされるタンパク質の存在または不在に基づき、癌または癌を発症する可能性を検出するための方法に関する。本発明はまた、tm−PTPε遺伝子を上方調節するまたは下方調節するための方法および分子を提供する。1つの実施形態において、本発明は、tm−PTPε遺伝子の配列または発現レベルを決定することを含む、生物学的試料において癌細胞を検出するための方法を提供する。 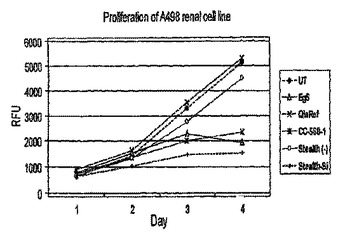 (もっと読む)
(もっと読む)
多重結合アッセイ用オリゴヌクレオチド対
本発明は、被検体の選別、検出および同定に有用なオリゴヌクレオチド利用アッセイシステムおよびキットである。本システムは、それぞれの対の一方のオリゴヌクレオチドが固体支持体に固定化され、他方のオリゴヌクレオチドは被検体結合剤が付着した、相補的なオリゴヌクレオチドの対を利用する。異なるオリゴヌクレオチドの対が、実質的に同一の速度でハイブリダイゼーションを起こし、実質的に同一のTmを有し、異なる対の間でのクロス・ハイブリダイゼーションを最小限にするように設計されたヌクレオチド配列を有し、検出可能なクロス・ハイブリダイゼーションを起こすことなく、周囲温度で比較的迅速にハイブリダイゼーションを起こす。 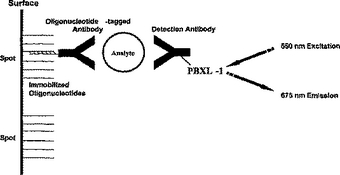 (もっと読む)
(もっと読む)
インターフェロンαの産生促進又は抑制物質のスクリーニング方法
【課題】 インターフェロン制御因子7(IRF7)と相互作用するインターロイキン1受容体結合キナーゼ1(IRAK−1)のToll様受容体7(TLR7)又はToll様受容体9(TLR9)シグナル伝達経路を介するインターフェロンαの産生促進又は抑制する物質のスクリーニング方法を提供すること。
【解決手段】 IRAK−1IRF7とを、被検物質が存在する細胞内で発現させ、IRAK−1とIRF7との会合の程度を測定したり、IRAK−1によるIRF7のC末端のリン酸化の程度を、被検物質の存在下にインビトロで測定したり、TLR7リガンド又はTLR9リガンド不応答性のモデルマウスや該マウス由来の細胞に、被検物質とTLR7リガンド又はTLR9リガンドを投与又は刺激し、モデルマウスや由来の細胞におけるインターフェロンαの産生量やIRF7の活性化の程度を測定する。
(もっと読む)
共通のToll様受容体を通じて媒介される細胞活性の選択的活性化
共通のTLRによって媒介される細胞活性を選択的に調節する化合物を同定する方法が提供される。一般に、この方法はTLRによって媒介される第1の細胞活性の調節を検出するアッセイを提供するステップと、TLRによって媒介される第2の細胞活性の調節を検出するアッセイを提供するステップと、試験化合物を使用して各アッセイを実施するステップと、試験化合物が第2のTLR−媒介細胞活性を調節するのとは異なる程度に第1の細胞活性を調節する場合、共通のTLRによって媒介される複数の活性の少なくとも1つの細胞活性を選択的に調節する化合物として、試験化合物を同定するステップとを含む。このような方法によって同定される化合物、このような化合物を含む医薬品組成物、およびこのような医薬品組成物を対象に投与することで病状を処置する方法もまた提供される。 (もっと読む)
物質が有する骨格筋毒性誘発能力の検定方法
【課題】
物質が有する骨格筋毒性誘発能力をより正確にかつ簡便に検定するための方法等を提供可能とすること。
【解決手段】
物質が有する骨格筋毒性誘発能力の検定方法において、
(1)骨格筋由来培養細胞に、被験物質及び標識GGPPを接触させる第一工程、
(2)第一工程後の前記培養細胞の細胞ホモジネート中に存在し、かつ、当該細胞ホモジネートをSDS-PAGEにより分離して得られうる物質であり、当該SDS-PAGEにおいて分子量20kd及び25kdの間に電気泳動されるバンドに含まれる物質への標識GGPPの取り込みの有無又はその量を測定する第二工程、
(3)第二工程により測定された標識GGPPの取り込みの有無又はその量と、対照における標識GGPP取り込みの有無又はその量とを比較することにより得られる差異に基づき前記被験物質の骨格筋毒性誘発能力の有無又はその程度を評価する第三工程
を有することを特徴とする検定方法等。
(もっと読む)
部分的proANPペプチドを同定するためのサンドイッチイムノアッセイ
NT-proANPの中間領域(NT-proANPのアミノ酸53からアミノ酸83に広がる領域)の部分的な配列に特異的に結合する2つの抗体を用いた、心臓病及び敗血症の診断における、部分的なproANPペプチドを同定するための改善されたサンドイッチイムノアッセイを開示する。  (もっと読む)
(もっと読む)
装置および循環腫瘍細胞および他の粒子の濃縮および変更のための方法
本発明は、循環腫瘍細胞および他の粒子を検出、富化および分析するための装置および方法を特徴とする。本発明は、さらに、被験体由来の細胞サンプルを分析することによって、被験体の状態(例えば、癌)を診断するための方法を特徴とする。本発明の方法は、以下の工程を包含する:a)第1の方向に癌細胞が濃縮される第1出力のサンプルを生成するように癌細胞を導き、そして第2の方向に第2の細胞が濃縮される第2出力のサンプルを生じるように一つ以上の第2の細胞を導く構造を有するチャネルを含んでいる装置に、細胞サンプルを導入する工程;ならびに、b)第1出力のサンプルにおいて癌細胞の有無を検出する工程。 (もっと読む)
インターロイキン8(IL−8)に対するヒトモノクローナル抗体
IL-8(例えばヒトIL-8)に結合する単離されたヒトモノクローナル抗体を開示する。本ヒト抗体は、V-D-J組換え及びアイソタイプ・スイッチングを起こすことにより複数のアイソタイプのヒトモノクローナル抗体を産生することのできる、ハイブリドーマ、トランスフェクトーマ、又は、トランスジェニック・マウスなどの非ヒトトランスジェニック動物で産生させることができる。更に、本ヒト抗体を含む医薬組成物、本ヒト抗体を産生する非ヒトトランスジェニック動物、ハイブリドーマ、及びトランスフェクトーマや、本ヒト抗体を用いるための治療法及び診断法も開示されている。 (もっと読む)
Bmal1の発現誘導を促進するRORα
【課題】
概日リズムの調節メカニズムのうち、未解明な部分を明らかにすること。
【解決手段】
本発明者らは、RORα(retinoic acid binding−receptor alpha、以下同じ)が、Bmal1の発現誘導を促進すること、及び、低酸素状態において、Bmal1の発現誘導が促進されること、を新規に見出した。このことは、低酸素状態などで、RORαの発現が促進されると、Bmal1の発現誘導が促進され、Bmal1の発現誘導が促進されると、BMAL1とCLOCKとの結合が促進され、Per遺伝子又はCry遺伝子の発現誘導が促進される、という概日リズムの調節メカニズムの存在を強く示唆する。従って、本発明に係る本発明は、時差ぼけ調整剤、抗がん剤として、適用できる可能性がある。
(もっと読む)
1,921 - 1,940 / 2,895
[ Back to top ]



