Fターム[4B063QS26]の内容
酵素、微生物を含む測定、試験 (178,766) | 処理,操作 (34,251) | 測定,試験における各種前処理,中間処理 (13,775) | 検出物,試薬等の増量,増幅(←増殖) (8,475) | 酵素的サイクリング (265)
Fターム[4B063QS26]に分類される特許
241 - 260 / 265
組み合わせた指数関数的および直線的増幅
核酸の感度良い検出および定量のための方法および組成物が提供される。さらに、遺伝子型決定のための方法および組成物が提供される。本発明のプローブにより、一本鎖、二本鎖ポリヌクレオチドおよびピロホスフェート(PPi)に関する標的開始増幅が可能になる。DNA酵素仲介検出法もまた、一本鎖最終産物の検出のために提供される。  (もっと読む)
(もっと読む)
受容体リガンド同定法
【課題】 本発明の課題の1つは、核内受容体を調節する化合物を同定することにある。
【解決手段】 上記課題は、核内受容体を調節する化合物を同定する方法であって、該方法は:A)候補化合物を提供する工程;およびB)該候補化合物が、該核内受容体中のシステインと共有結合するかどうかを判定する工程であって、共有結合すると判定された候補化合物を、核内受容体を調節する化合物であると同定する、工程を包含する、方法を提供することによって解決される。
(もっと読む)
化合物同定用の代謝法
本発明は、フレーバーまたは香料としての、それらの前駆体としての、または香料もしくはフレーバーの知覚のモジュレーターとしての、化合物の同定に関する。本方法は、化合物を、鼻、口または気道中で発現される代謝酵素と反応させること、およびその後に、該化合物またはその代謝産物を、フレーバーもしくは香料として、それらの前駆体として、またはそれらの知覚もしくはそれらの対応する手掛かりの知覚のモジュレーターとして、同定することを含む。 (もっと読む)
プレmRNAのスプライシングを修飾するための方法および組成物
本発明は、プレmRNA分子のスプライシング事象を抑制するためにプレmRNAおよび/またはスプライシング機構のエレメントを本明細書中に記載の方法によって同定した小分子化合物と接触させるステップを含む、プレmRNA分子中のスプライシング事象を抑制する方法を提供する。さらに、プレmRNA分子のスプライシング事象を誘導するためにプレmRNAおよび/またはスプライシング機構のエレメントを本明細書中に記載の方法によって同定した小分子化合物と接触させるステップを含む、プレmRNA分子中のスプライシング事象を誘導する方法を提供する。さらに、プレmRNA分子中の選択的スプライシングまたは異常なスプライシング事象を抑制するために治療有効量の本明細書中に記載の方法によって同定された化合物を患者に投与し、それにより患者を治療するステップを含む、プレmRNA分子の選択的または異常なスプライシング事象に関連する障害を有する患者の治療方法を本明細書中に提供する。 (もっと読む)
プロテオーム解析
メタロプロテアーゼを解析するための活性ベース組成物が開示される。この組成物は、ヒドロキサマート部分およびベンゾフェノン部分を含む化合物を含む。これらの化合物を合成するための方法、ならびにメタロプロテアーゼに対する、活性化合物を含む組成物の生物活性を求めるために、およびメタロプロテアーゼに対する阻害剤の効力を求めるために、これらの化合物を使用する方法も開示される。 (もっと読む)
アセチルCoAカルボキシラーゼインヒビターの同定のための組換えビオチンカルボキシラーゼドメイン
ビオチン結合ドメインが欠失され、カルボキシトランスフェラーゼドメインが欠失され、且つ機能的なビオチンカルボキシラーゼ(BC)ドメインを有するアセチルCoAカルボキシラーゼ(ACCアーゼ)を含むペプチドを記載する。上記ペプチドをコードする核酸および前記核酸を含み、且つコードしたペプチドを発現する組換え宿主細胞もまた記載する。アセチルCoAカルボキシラーゼインヒビター、殺真菌薬、および除草剤の同定方法も本明細書中に記載する。 (もっと読む)
再構成ヒストンメチルトランスフェラーゼ複合体及びそのモジュレーターの識別方法
本発明は、EEDと、EZH2と、SUZ12とを包含する再構成複合体を提供し、ここで再構成複合体はヒストンH3のリジン27(H3−K27)に対してヒストンメチルトランスフェラーゼ(HMTase)活性を有する。再構成複合体は、RbAp48、AEBP2、あるいはそれらの両方をさらに含むことができる。再構成複合体の製造方法、再構成複合体のHTMase活性を阻害する化合物を識別する方法、及び、癌を治療するための候補化合物を識別する方法も開示する。再構成複合体を包含する試薬及びキットも更に提供される。  (もっと読む)
(もっと読む)
IGFR経路のモディファイヤーとしてのC20ORF23及び使用方法
ヒトC20ORF23遺伝子はIGFR経路のモジュレーターとして同定されており、したがってこれらは欠陥IGFR機能に関連する疾患の治療上の標的である。C20ORF23の活性を調節する作用剤をスクリーニングすることを含む、IGFRのモジュレーターを同定する方法が提供される。 (もっと読む)
アディポネクチン受容体発現制御剤
絶食および再摂食下マウスを用い、AdipoR1/R2 が栄養状態およびインスリンに対する代謝感受性の制御因子であることを明らかにした。STZ処理によるAdipoR1/R2 mRNAレベル増強、および、該増強のインスリンによる回復を示した。インスリンが筋細胞中等のAdipoR1/R2 mRNAを減少させることを、in vitroで確認した。インスリン抵抗性モデルではAdipoR1/R2発現が下方制御されていること、アディポネクチンによるAMPキナーゼ活性化が減少しているを確認した。インスリンシグナル経路阻害剤を用い、インスリンによるアディポネクチン受容体下方制御は、PI3-キナーゼ/Foxo1経路を介していることを発見した。 (もっと読む)
ATP7Aの使用による、神経変性疾患の治療
本発明は、神経生成(neurogenerative)疾患治療用の薬剤組成物を調製するためのATP7A相互作用分子の使用に関する。これによって、ATP7A相互作用分子は、好ましくはATP7Aの阻害剤であり、そして特に、該分子は、ガンマ−セクレターゼおよび/またはベータ−セクレターゼの活性を調節する能力を有する。さらに、本発明は、ガンマ−セクレターゼおよび/またはベータ−セクレターゼの調節剤を同定する方法であって:a.既定の試験化合物がATP7A相互作用分子であるかどうか決定することによって、ATP7A相互作用分子を同定し、b.工程a)のATP7A相互作用分子がガンマ−セクレターゼおよび/またはベータ−セクレターゼの活性を調節可能であるかどうか決定する工程を含む、前記方法に関する。 (もっと読む)
血糖を検出するためのシステム及び方法
血液サンプル中の血糖値を測定するシステムは、テストストリップ及び測定器を含む。テストストリップは、サンプル室又は他の試験領域、作用電極、対極、充填−検出電極及びオートオンコンダクタを含む。試験領域には試薬層が配置されている。オートオンコンダクタは、テストストリップが測定器に挿入されると、測定器を起動させ、テストストリップシーケンスを実行させる。測定器は、作用電極及び対極を用いて試験領域の血液サンプルを検出し、充填−検出電極を用いて血液サンプルが試薬層で混合されたかを確認する。測定器は、作用電極と対極との間に分析評価電圧を印可して発生電流を測定する。測定器は、測定した電流及びメモリに保存したテストストリップに関連するリムーバブルデータストレージデバイスからの較正データに基づき血糖値を算出する。 (もっと読む)
核酸およびポリペプチドを選択する系ならびに方法
本発明は、一般に、配列が知られているもしくは未知であるmRNAをその翻訳されたタンパク質と連結して同族対を形成することによる、所望のタンパク質または核酸分子を同定かつ選択するための系および方法に関する。同族対は、タンパク質または核酸の所望の特性に基づいて選択される。また、この方法には、選択された同族対の核酸部分を増幅すること、核酸に変異を導入すること、核酸を翻訳すること、核酸をそのタンパク質に結合させて第2の同族対を形成すること、および所望の特性に基づいてこの同族対を再選択することによる、所望のタンパク質または核酸分子の進化が含まれる。tRNAに架橋結合する働きをする修飾されたmRNAも提供する。ソラレンモノ付加体または架橋結合の生成方法も提供する。mRNAライブラリおよびワクチンの産生方法も提供する。 (もっと読む)
バイオチップ及びそれを用いた試料溶液の機能性検査方法
血液などの酵素活性や免疫学的特性を網羅的に測定して病理学的診断を行う際のデータの取り扱い性や信頼性に優れ、化学処理が容易でしかも検出部の集積度を高められ微量の検体溶液でも酵素活性及びその傾向を取得できるバイオチップを提供する。
チップ基板11に導入される試料溶液中の酵素を検出するバイオチップであって、全体が渦巻き状やツリー状、放射状などの流路パターンで前記チップ基板上に形成された試料溶液流路12と、試料溶液流路12に所定順で複数配置され所定の酵素に対してそれぞれ異なる活性を有する酵素活性検知部13と、を備える。
(もっと読む)
アルツハイマー病の進行に関連するNTRK1遺伝子マーカー
アルツハイマー病の進行に関連するNTRK1遺伝子のハプロタイプが、開示される。これらのNTRK1ハプロタイプを検出するための組成物および方法が、開示される。この方法は、個体が進行マーカーIを有するかまたは進行マーカーIIを有するかを決定するための方法であって、この方法は、この個体が(i)ハプロタイプ、(ii)連鎖ハプロタイプ、および、(iii)置換ハプロタイプのうちのいずれかの2コピーを有するか、または(i)〜(iii)のうちの1コピーを有するかもしくはいかなるコピーも有さないかを決定する工程を包含する。 (もっと読む)
糖化蛋白質の測定方法
フルクトシルリジン類の影響を軽減し、かつ簡便で効率の良い糖化蛋白質、フルクトシルペプチド又はフルクトシルアミノ酸を測定する方法及び測定用試薬を提供する。 フルクトシルペプチド又はフルクトシルアミノ酸にpH4.0〜7.0でフルクトシルペプチド又はフルクトシルアミノ酸の測定用酵素を特異的に作用させ、得られる生成物をpH4.0〜7.0にて測定することを特徴とする、試料中のフルクトシルペプチド又はフルクトシルアミノ酸の測定におけるフルクトシルリジン類の影響の軽減方法、及びそれを用いた糖化蛋白質の測定方法。 (もっと読む)
グルコース脱水素酵素とシトクロームとの融合蛋白質
ピロロキノリンキノングルコース脱水素酵素(PQQGDH)とシトクロームとの融合蛋白質が開示される。PQQGDHとしては、例えば、Acinetobacter calcoaceticus由来の水溶性PQQGDHを用いることができる。シトクロームとしては、例えば、Comamonas testosteroniのキノヘモ蛋白質エタノールデヒドロゲナーゼの電子伝達ドメインを用いることができ
る。本発明の融合蛋白質においては、酸化還元中心のPQQからシトクロームに分子内電子移動が生ずるため、電子メディエータを必要としない直接電子伝達型のグルコースセンサーの製造が可能である。
(もっと読む)
CREBL1、ATF6およびHNF−4αのうちの少なくとも1のHtrA2による分解を阻害することによる糖尿病の治療方法
HtrA2と相互作用するCREBL1およびHNF−4αを見出し、さらに活性型HtrA2によりCREBL1、ATF6およびHNF−4αが分解されることを初めて明らかにした。 そして、HtrA2の機能を阻害することを特徴とするCREBL1、ATF6およびHNF−4αのうちの少なくとも1の分解阻害手段、CREBL1、ATF6およびHNF−4αのうちの少なくとも1のHtrA2による分解を阻害することを特徴とする糖尿病の防止手段および/または治療手段、CREBL1および/またはATF6のHtrA2による分解を阻害することを特徴とする細胞死阻害手段(例えば膵臓β細胞の細胞死阻害手段)、HNF−4αのHtrA2による分解を阻害することを特徴とする2型糖尿病の防止手段および/または治療手段、並びに試薬キットを提供した。 (もっと読む)
合成チモーゲンを用いるシグナル増幅
チモーゲン、チモーゲンの使用方法、およびチモーゲンを組み込む装置が、本明細書中に記載される。該チモーゲンは基質および酵素を含む。該基質は該酵素を阻害し得、微生物によって産生されるタンパク質の標的である。微生物によって産生されるタンパク質によって基質が修飾される場合、酵素が活性化される。チモーゲンを用いて、検出アッセイを増幅し得る。 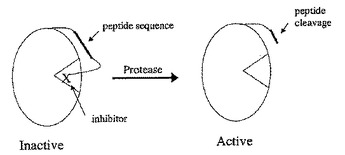 (もっと読む)
(もっと読む)
エンドセリアーゼ−2リガンド
本開示は、とりわけ、エンドセリアーゼ−2(ET2)に結合するタンパク質、例えば、高い親和性および選択性でET2を阻害する免疫グロブリンを提供する。ET2結合タンパク質は、血管新生関連障害を含む種々の障害を治療するために使用され得る。1つの態様において、本発明は、ET2(本明細書ではET2リガンドまたはET2−結合リガンドともいう)に結合するタンパク質リガンドを特徴とする。典型的には、このリガンドは、天然には存在していない。1つの実施形態において、このタンパク質リガンドは、重鎖可変ドメイン配列および軽鎖可変ドメイン配列を含む。例えば、このリガンドは、抗体または全長抗体の抗原結合フラグメント(本明細書では抗ET2抗体ともいう)である。 (もっと読む)
アロマターゼ活性の測定方法
本発明は、アロマターゼ活性の測定に有用な化合物に関する。本発明は、アロマターゼ活性を測定し、アロマターゼ活性を調節する試験薬剤をスクリーニングするための方法をさらに提供する。そうしたスクリーニング法で使用するためのキットも提供する。 (もっと読む)
241 - 260 / 265
[ Back to top ]