Fターム[4B064DA01]の内容
微生物による化合物の製造 (77,679) | 利用分野、有用性 (15,472) | 医薬;予防、治療 (7,299)
Fターム[4B064DA01]の下位に属するFターム
抗生物質 (306)
抗腫瘍性 (590)
脂質、コレステロール低下性 (26)
糖質低下性 (21)
消炎用、鎮痛用 (83)
Fターム[4B064DA01]に分類される特許
6,181 - 6,200 / 6,273
ヒト成長ホルモングリコシル化突然変異体の組成と調合法
本発明は組み換え産生ポリペプチドが天然に存在のヒト成長ホルモンとは明確に異なる一つ又は複数の新規導入N−連結又はO−連結グリコシル化部位を含有するヒト成長ホルモンの突然変異体に関する。突然変異体用配列コード化ポリペプチド、コード化配列含有発現カセット、突然変異体発現細胞及び突然変異体生成法も又開示する。更に突然変異体含有薬剤組成とこの突然変異体の使用法も開示されている。  (もっと読む)
(もっと読む)
反復配列タンパク質ポリマー活性剤結合体、方法および使用
反復配列タンパク質ポリマーと少なくとも1つの活性剤との結合生成物を含む、生体分子結合体を提供する。他の態様はこれらの製造法、ならびにさまざまな産業および消費者用途を提供する。 (もっと読む)
線虫類抽出抗凝血薬タンパク質(NAP)を製造するためのプロセス
本発明は、精製された線虫類抽出抗凝血タンパク質(NAP)を製造するためのプロセスを提供する。ここで、請求されたプロセス方法により製造されるNAPは、NAP薬物製品として製剤化することができるNAP薬物物質である。本発明は、本明細書に開示されるプロセスによって製造されるNAP薬物物質およびNAP薬物製品を提供する。1つの態様において、本発明は、rNAPc2/プロリン薬物物質およびrNAPc2/プロリン薬物製品を製造するためのプロセスを提供し、本明細書に開示されるプロセスによって製造されるrNAPc2/プロリン薬物物質を提供する。 (もっと読む)
β−ラクタマーゼ阻害剤中間体を合成するための方法
本発明は、式(II)および(III)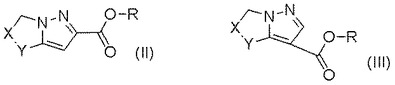
[式中、X、YおよびRは明細書中に定義されたとおりである]
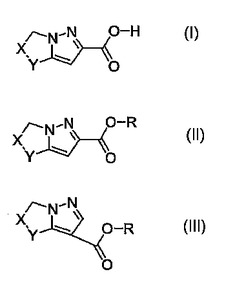
で示される位置異性体の加水分解可能なエステルの混合物の選択的酵素加水分解によるβ−ラクタマーゼ阻害剤の調製に有用な式(I)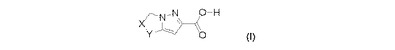
[式中、XおよびYは明細書中に定義されたとおりである]
で示される中間体、二環式ヘテロアリール−2−カルボン酸の酵素的製法に関する。
 (もっと読む)
(もっと読む)
アンジオテンシン変換酵素阻害ペプチド含有組成物
天然原料よりACE阻害活性に優れたペプチド及びその製造法を提供する。 大豆中の微量蛋白質である大豆ホエー蛋白質を基質にしてプロテアーゼで分解することにより、大豆の主要な貯蔵蛋白質であるβ−コングリシニンやグリシニンを基質としたペプチドよりもACE阻害活性が高いペプチドを得られることを見出し、これに基づき本発明を完成するに至った。 (もっと読む)
ドメイン交換結合分子、その使用方法および製造方法
本明細書において、高親和性ドメイン交換結合分子のランダムまたは合理的設計のための方法およびその使用法を提供する。同様に、そのような複数のドメイン交換結合分子を含むライブラリーも提供する。 (もっと読む)
APO−2Lレセプター結合ペプチド及びその使用
Apo−2Lレセプター分子に結合するペプチドを提供する。これらペプチドは、例えば、Apo−2L及び/又はDR5等のApo−2Lレセプター分子の生物学的活性の調節が望まれる方法に用いることができる。 (もっと読む)
IL−18結合タンパク質の活性変異体とその医学的応用
本発明は、IL-18結合タンパク質の活性断片、そのような活性断片を含む医薬組成物と、医学におけるその利用法に関する。 (もっと読む)
植物細胞における色素体標的タンパク質の生成方法
予め決定した植物の細胞で、対象のタンパク質を生成する方法であって、(i)融合タンパク質を色素体内にターゲティングする輸送ペプチド、及びそれに隣接して(ii)前記対象のタンパク質をN末端からC末端に含む前記融合タンパク質をコードするベクターを前記細胞内に導入することを含み、前記輸送ペプチドC末端の3個のアミノ酸X−3X−2X−1及び前記対象のタンパク質N末端のアミノ酸Zが、色素体で前記対象のタンパク質を放出するためにX−1とZとの間で前記融合タンパク質を開裂するための開裂部位X−3X−2X−1−Zを形成し、前記対象のタンパク質の予め決定したアミノ酸Zに対して、アミノ酸配列X−3X−2X−1が、植物の色素体を標的とする融合タンパク質で天然に存在するZに隣接するアミノ酸配列X−3X−2X−1の組から選択され、それにより前記開裂部位を形成する方法。 (もっと読む)
膜タンパク質におけるフリンプロテアーゼ開裂部位の挿入およびその使用法
フリンプロテアーゼの開裂部位を、膜糖タンパク質のドメイン間に挿入する。トランスゴルジネットワークにおけるフリンによる開裂の際に、タンパク質は、その天然構造を保持した個別の膜を含まないドメインへと分離される。このプロトコールを用いて、構造解析用およびワクチンとしての試験用のウイルス膜タンパク質ドメインを産生できる。 (もっと読む)
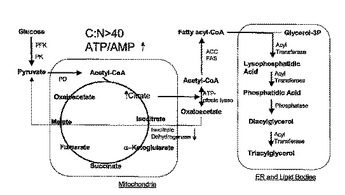
油性酵母菌における多不飽和脂肪酸の生成
本発明は、油性酵母菌におけるω−3および/またはω−6脂肪酸の生成方法に関する。したがってARAおよびEPAの合成のために、リノール酸(LA)からγ−リノレン酸(GLA)、α−リノール酸(ALA)からステアリドン酸(STA)、GLAからジホモ−γ−リノール酸(DGLA)、STAからエイコサテトラエン酸(ETA)、DGLAからアラキドン酸(ARA)、ETAからエイコサペンタエン酸(EPA)、DGLAからETA、EPAからドコサペンタエン酸(DPA)、およびARAからEPAへの転換を触媒できるデサチュラーゼおよびエロンガーゼが、ヤロウイア(Yarrowia)のゲノムに導入された。
 (もっと読む)
(もっと読む)
抗CS1抗体の治療的使用
本発明は、CS1に結合してCS1の少なくとも1つの生物活性を中和するCS1のアンタゴニストに関する。本発明はまた、このような抗体またはその抗原結合フラグメントを含む薬学的組成物を含む。本発明はまた、有効量のこのようなアンタゴニストを被験体に投与する工程を含む、必要とする被験体の病態(自己免疫障害および癌が含まれる)の予防または治療する方法を提供する。本発明はまた、種々の障害(例えば、自己免疫障害および種々の定義した癌性病態(種々の形態の骨髄腫が含まれる))の新規の治療方法を提供する。このような障害の診断および予後評価方法ならびにこのような病態を調整する組成物のスクリーニング方法も提供する。 (もっと読む)
オリゴ糖キトサンの製造方法及びオリゴ糖キトサン
本発明は、オリゴ糖キトサンの製造方法、及びオリゴ糖キトサンに関し、医薬、化粧品及び食品工業において使用し得る。本発明の目的は、オリゴ糖キトサンの製造方法及びオリゴ糖キトサン自体を開発することである。本発明のオリゴ糖キトサンは、その広範囲のイオン結合した誘導体がさらなる特性を有する最終生成物を提供し且つさらなる使用中に当該特性の安定性を確保することを可能にすることに特徴を有する。上記目的は、パパイン及び酢酸の存在下にキトサンの発酵的オリゴマー化を実施し、そのようにして発酵的にオリゴマー化した生成物をスプレー乾燥させ、その後、そのようにして得られた生成物を水に少なくともさらに2回溶解し、引続き、生成物を再度スプレー乾燥させることからなる本発明のオリゴ糖キトサンの製造方法によって達成される。そのようにして形質転換した生成物を、酸基を含有する物質と一緒に水に溶解し、オリゴ糖キトサンの塩結合を溶媒工程中に実施し、溶媒工程はオリゴ糖キトサンのイオン結合した誘導体が得られるまで実施し、その後、再度乾燥させる。また、上記目的は、イオン結合した酢酸を含有し且つ少なくとも1つのタイプのイオン結合した酸基含有物質をさらに含有するオリゴ糖キトサンを製造することによっても達成される。本発明のオリゴ糖キトサンは、57.0〜92.0質量%のオリゴ糖キトサン、2.3〜3.7質量%のイオン結合した酢酸を含有し、残余が酸基を含むイオン結合した物質である。 (もっと読む)
癌の処置および検出において有用な109P1D4と称される、核酸および対応タンパク質
新規遺伝子109P1D4およびそのコードタンパク質、ならびにこれらの改変体が、記載され、ここで、109P1D4は、正常な成人組織中で組織特異的な発現を示し、表Iに列挙される癌において異常に発現される。結果として、109P1D4は、癌に対する、診断標的、予後標的、予防標的および/または治療標的を提供する。109P1D4遺伝子またはそのフラグメント、あるいはそのコードタンパク質、またはその改変体、またはそのフラグメントは、体液性免疫応答または細胞性免疫応答を誘発するために使用され得;109P1D4と反応性である抗体またはT細胞は、能動免疫または受動免疫において使用され得る。  (もっと読む)
(もっと読む)
ストレプトコッカス・アガラクティエ抗原I+II
本発明は、ストレプトコッカス・アガラクティエからの過免疫血清反応性抗原またはその断片をコードする単離核酸分子および過免疫血清反応性抗原またはその断片、かかる抗原の単離方法およびその特定の使用を開示する。 (もっと読む)
グリコペギレ−ション法およびその方法により生成されたタンパク質/ペプチド
【課題】 貧血症、腎臓透析患者を治療するに有効なペプチドをグリコペギレーション法(グリコPEG化)により提供することである。
【解決手段】 一つもしくはそれ以上のグリコシル基をペプチドに付加もしくは除去すること、および/または修飾基をペプチドに付加する方法により、ペプチド分子を改造する。
(もっと読む)
CNGH0010特異的ポリヌクレオチド、ポリペプチド、抗体、組成物、方法および使用
新規ポリペプチド(CNGH0010)および抗体(少なくとも1つのそのようなCNGH0010ポリペプチド、そのバリアントまたはフラグメントに特異的なその特定した部分またはバリアントを含む)、ならびにそのようなCNGH0010ポリペプチドおよび抗体をコードする核酸、相補的核酸、ベクター、宿主細胞およびそれらの作成および使用法は、治療用、診断用製剤、投与およびデバイスに有用である。前述のポリペプチドはヒト、霊長類、齧歯類、哺乳動物、キメラ、ヒト化および/またはCDR−移植化抗−CNGH0010抗体を生成するために使用することができる。CNGH0010ポリペプチドおよび抗体は、細胞、組織、臓器、動物または患者中の少なくとも1つのCNGH0010−関連疾患のモジュレートまたは処置に使用される。そのような疾患には限定するわけではないが、乾癬、慢性関節リウマチ、気腫、喘息、糖尿病、自己免疫性甲状腺炎、クローン病および潰瘍性大腸炎を含む炎症性腸疾患、アレルギー性皮膚炎、接触皮膚炎を含む種々の皮膚炎、紫外線角膜炎、損傷治癒、瘢痕形成、種々の腎臓疾患、種々の呼吸疾患、子宮内膜炎のような種々の生殖器疾患、黒色腫、偏平上皮癌、卵巣癌、乳癌、肺癌、結腸癌、前立腺癌、腎臓細胞癌、グレーヴズ病および他の炎症性および過剰増殖性疾患を含むことができる。 (もっと読む)
細胞毒性が低減された免疫原性ヒトTNFαアナログおよびそれらの製造方法
本発明は、ヒトTNFαの免疫原性アナログを提供する。ここで、該アナログは免疫原化されたモノマーTNFαポリペプチドまたはTNFαダイマーもしくはトリマーを含み、該アナログはY87S、D143NまたはA145R(番号付けは、ヒトTNFαのN-末端のバリンから設定される)からなる群より選択される毒性減少または毒性破壊突然変異をさらに含む。本発明は、該アナログをコードする核酸断片ならびに該アナログの製造に有用なベクターおよび形質転換細胞も提供する。TNFαをダウンレギュレーションすることが必要な対象においてTNFαをダウンレギュレーションする方法も開示される。 (もっと読む)
トランスジェニック植物細胞に由来する安定な免疫予防的および治療的組成物ならびにその産生方法
本発明は、一般的に免疫学の分野に関し、免疫保護組成物およびトランスジェニック植物細胞からそのような組成物を調製する方法を提供する。本発明はまた、タンパク質産生(例えば、酵素、毒素、細胞受容体、リガンド、シグナル伝達物質、サイトカイン、またはトランスジェニック植物細胞培養物において発現される他のタンパク質の組換えによる産生)の分野に関し、これらのタンパク質を含む組成物を提供する。 (もっと読む)
グループ1ダニポリペプチド変異型
本発明は、変異型の成熟ポリペプチドが下記から成る位置または前記位置に対応する1または2以上の突然変異を含んでなる、グループ1ダニポリペプチドの変異型に関する: 配列番号1のA10、A12、E13、G29、G30、G32、A46、Y47、S54、L55、D64、A66、S67、G73、T75、I80、Q84、N86、G87、S92、Y93、Y96、A98、R99、E100、Q101、R104、R105、P106、Q109、R110、F111、G112、I113、A132、I144、K145、D146、D148、R151、I158、I159、Q160、R161、D162、N163、G164、Y165、Q166、N179、A180、G182、V183、D184、A205、I208または成熟Der p 1ポリペプチドの10、12、13、29、30、32、46、47、54、55、64、66、67、73、75、I80、84、86、87、92、Y93、96、98、99、100、101、104、105、106、109、110、111、112、113、132、144、145、146、148、151、158、159、160、161、162、163、164、165、166、179、180、182、183、184、205、208。 (もっと読む)
6,181 - 6,200 / 6,273
[ Back to top ]