Fターム[4H006AC83]の内容
有機低分子化合物及びその製造 (186,529) | 反応 (20,822) | 光学活性化合物の分離;光学分割 (327)
Fターム[4H006AC83]に分類される特許
301 - 320 / 327
アミノ化合物の光学分割剤および光学分割法
【課題】 充分な物理的性質の差異を生じるジアステレオマーを形成することができ、さらに、ジアステレオマーから温和な条件で目的のエナンチオマーを再生することができる、キラルなアミノ化合物用の光学分割剤を提供する。
【解決手段】 下記の式(I−1)または式(I−2)で表わされるシクロヘキサジエン−無水ジカルボン酸化合物による。式(I−1)および式(I−2)中、R1およびR2は互いに別異の原子または官能基を表わす。キラルなアミノ化合物(例えばアミノ酸)のラセミ体に式(I−1)または式(I−2)の化合物を反応させてアミド化合物のジアステレオマーを生成させた後、該ジアステレオマーを分離精製し、さらに、そのジアステレオマーを弱酸性条件下に加水分解することにより、アミノ化合物を再生、単離することができる。
【化1】
【化2】 (もっと読む)
(もっと読む)
鏡像異性体に関して純粋なアトモキセチンとトモキセチンマンデル酸塩
本発明により、鏡像異性体に関して純粋な(R)-(-)-トモキセチン(S)-(+)-マンデル酸塩とアトモキセチンHClが提供される。本発明によりさらに、ラセミ・トモキセチンから調製した、鏡像異性体に関して純粋な(R)-(-)-トモキセチン(S)-(+)-マンデル酸塩が提供される。本発明により、(R)-(-)-トモキセチン(S)-(+)-マンデル酸塩から調製した、鏡像異性体に関して純粋なアトモキセチンHClも提供される。 (もっと読む)
タキキニンインヒビターおよび/またはセロトニン再取込みインヒビターとしてのN−ベンジル−フェニル−ヘテロシクリル−プロピオンアミド化合物
本発明は、式(I)
【化1】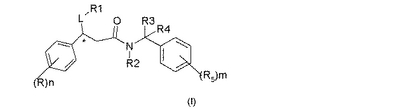
[式中、R1は、5員または6員のヘテロアリール基(5員のヘテロアリール基は、酸素、硫黄、または窒素から選択される少なくとも1個のヘテロ原子を含有し、そして6員のヘテロアリール基は、1から3個の窒素原子を含有する)を表すか、またはR1は、4員、5員、または6員の複素環基を表し、ここで、該5員または6員のヘテロアリール基、または4員、5員、または6員の複素環基は、(CH2)PR6(ここで、pは、0、または1から4の整数である)から選択される1から3個の置換基(同一または異なっていてもよい)により置換されていてもよく、そしてR、およびR2〜R6は、それぞれ明細書において定義されている]の複素環式誘導体、およびその医薬的に許容される塩および溶媒和物;その製造方法、およびタキキニンにより、および/またはセロトニン再取込み輸送タンパク質の選択的阻害により仲介される状態の処置での使用に関する。 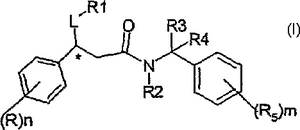 (もっと読む)
(もっと読む)
アクツミンおよびアクツミン化合物、合成、および使用
本発明は、アクツミンおよびその化合物ならびに式(I)(式中、R1およびR2は、各々、水素原子を示すか、または、一緒に更に結合を形成し、R3は、水素原子またはアルコキシ基を示し、R3は、水素または塩素原子を示し、R6は、水素原子またはアルキル、アルキルカルボニル、もしくはアミル基を示し、R7およびR10は、各々、アルコキシ基を示し、RIOは、アルコキシ基を示し、R4、R8、R9、R11、R12、R13、およびR14は、明細書に定義した通りである)の化合物に関する。  (もっと読む)
(もっと読む)
イソフラバン誘導体の光学分割方法
【課題】光学活性なイソフラバン誘導体を製造するための光学分割方法を提供すること。
【解決手段】一般式(I)
【化1】
(式中、R1、R2、R3、R4、R5、R6、R7、R8、R9およびR10は、水素原子、保護基によって保護されていてもよい水酸基、置換基を有していてもよいアルキル基、アルケニル基、アラルキル基またはアリール基を表し、R1からR6のうちの2つ、R7とR8およびR9とR10は、それぞれ結合して環構造を形成していてもよい。)で示されるイソフラバン誘導体のエナンチオマー混合物の光学分割方法であって、光学活性化合物を有効成分とする分離剤によって光学分割することを特徴とする、イソフラバン誘導体の光学分割方法。
(もっと読む)
チュブリン阻害剤の合成に有用な中間体の合成方法
本発明は、癌の治療に有用なチュブリン阻害剤の製造に有用な中間体である、式I:
【化1】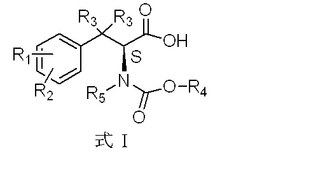
[式中、R1、R2、R3、R4およびR5は、明細書の記載と同意義である]
で示される化合物の製造方法に関する。 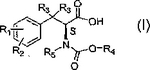 (もっと読む)
(もっと読む)
クロピドグレルの立体選択的な製造方法
本発明は、式(II)
【化1】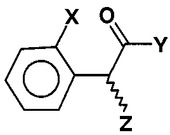
(II)
(式中、Xはハロゲン原子であり、Y及びZは、それぞれ独立して、脱離基を表す)の化合物を光学活性アミノアルコールと反応させてジアステレオマーの第1混合物を生成させることを特徴とする、一般式(Ia)
【化2】
(Ia)
(式中、Xは上記した通りである)の化合物の製造方法に関する。 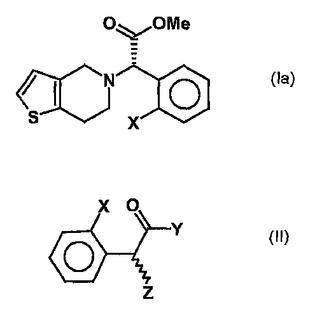 (もっと読む)
(もっと読む)
シクロペンテンニトリル誘導体の製造方法
【課題】本発明は、高価な試薬や化合物を使用せずに少ない工程数でシクロペンテンニトリル誘導体、就中、光学分割可能なシクロペンテンニトリル誘導体が、収率良く得られる、α,β−不飽和ケトンへのニトリル誘導体の共役付加反応を利用したシクロペンテンニトリル誘導体の合成法を提供することを目的とする。
【解決手段】本発明は、α,β−不飽和ケトンと、α位にアルキル基又はアリル基を有していてもよい4−アルコキシ−3−ブテンニトリル、例えば、4−メトキシ−3−ブテンニトリルとの共役付加反応により得られた化合物を無水酢酸又はクロロ炭酸エステル等を用いてエノールエステルとして捕捉した後、これを例えば強酸で処理することにより5員環を形成させてシクロペンテンニトリル誘導体とする、新規で且つ収率の良いシクロペンテンニトリル誘導体の製造法に関する。
(もっと読む)
ウッディな香気を付与可能な香料成分
本発明は香料分野に関し、かつ1,8a−メタノ−2,4a,8,8−テトラメチルデカヒドロ−2,3−ナフタレンジオールのジエーテルまたは1,3−ジオキソラン誘導体およびその香料成分としての使用に関する。さらに本発明は、前記化合物に関連する香料組成物または付香製品に関する。 (もっと読む)
エスシタロプラムの製造に使用できる中間体の分離方法
本発明は、4-[(S)-4-ジメチルアミノ-1-(4-フルオロフェニル)-1-ヒドロキシ-ブチル]-3-ヒドロキシメチルベンゾニトリルおよびそのアシル化誘導体の、カルボン酸基を含む4-[(S)-4-ジメチルアミノ-1-(4-フルオロフェニル)-1-ヒドロキシ-ブチル]-3-ヒドロキシメチルベンゾニトリルの誘導体を形成する化合物との反応により、4-[(S)-4-ジメチルアミノ-1-(4-フルオロフェニル)-1-ヒドロキシブチル]-3-ヒドロキシメチルベンゾニトリルのアシル化誘導体を分離および単離する方法に関する。カルボン酸基を含むアシル化誘導体が形成されるとそれが沈殿し、容易に反応混合物から分離することができる。 (もっと読む)
キラル無機−有機複合多孔性物質及びその製造方法
本発明は、電荷バランス陽イオンを含む多孔性無機物において、陽イオン性キラル有機分子が電荷バランス陽イオンとして存在することを特徴とするキラル無機−有機複合多孔性物質及び、イオン交換方法によるキラル無機−有機複合多孔性物質の製造方法を提供する。本発明のキラル無機−有機複合多孔性物質は、安定性、選択性及び耐久性などに優れており、キラル選択性触媒または異性体混合物の分離物質として使用可能である。  (もっと読む)
(もっと読む)
EP2受容体アゴニスト
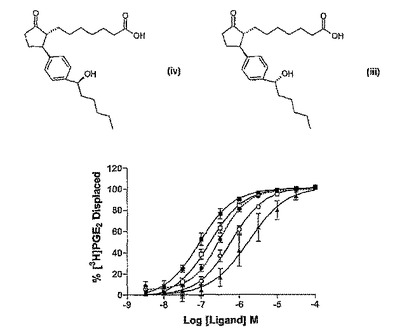
式(iv)または式(iii)から選択される化合物:(iv)(1R,2S)−2−[4−(1−(S)−ヒドロキシヘキシル)フェニル]−5−オキソ−シクロペンタンヘプタン酸メチルエステル[RSS]または(iii)(1R,2S)−2−[4−(1−(R)−ヒドロキシヘキシル)フェニル]−5−オキソ−シクロペンタンヘプタン酸メチルエステル[RSR];またはその塩、溶媒和物、化学的に保護された形態もしくはプロドラッグ、およびEP2受容体のアゴニズムにより緩和される疾患におけるその使用。 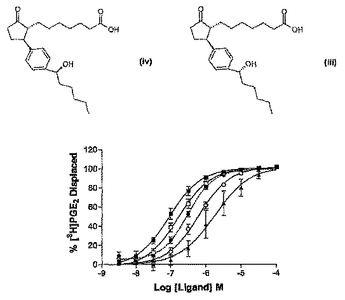 (もっと読む)
(もっと読む)
トルテロジン、その組成物及び使用、及びその製造方法
結晶形態における、ラセミ体のトルテロジンの遊離塩基、向上した純度を有するトルテロジン、それらの組成物及び使用、及びそれらの製造方法。 (もっと読む)
エナンチオ濃縮されたアミノ酸の製造方法
本発明は、α−アミノ酸誘導体の分割方法に関する。特に本発明は、エナンチオマー的に純粋なN−非保護β−アミノ酸誘導体を用いての晶出による、N−保護アミノ酸のエナンチオマー混合物の分割に関する。 (もっと読む)
キラルな塩基環状アミドとの塩形成による、場合により置換されたマンデル酸を分割するための方法
本発明は、キラルな塩基環状アミドとの塩形成によるラセミマンデル酸誘導体混合物からマンデル酸誘導体の分割のための新規方法;分割されたマンデル酸環状アミド塩(たとえば、式IIaを参照されたい)およびマンデル酸誘導体のある種の別の金属およびアミン塩、ならびに、たとえば医薬化合物の大規模製造に適した中間体としての分割されたマンデル酸誘導体の使用に関する;式(IIa)では、RはCHF2、H、C1〜6アルキル、CH2F、CHCl2およびCClF2から選択され;そしてここでnは0、1または2であり;R1はHまたはC1〜6アルキルであり、そしてXはH、ハロまたはC1〜6アルキルである。 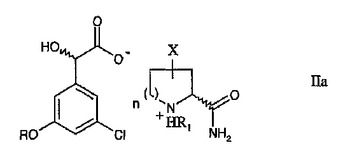 (もっと読む)
(もっと読む)
光学活性3−(4−ヒドロキシフェニル)プロピオン酸類の製造方法
【課題】本発明は、短工程で収率及び光学純度よく医薬中間体として有用な所望の光学活性3−(4−ヒドロキシフェニル)プロピオン酸類の製造方法を提供することを目的とする。
【解決手段】一般式(1)
【化1】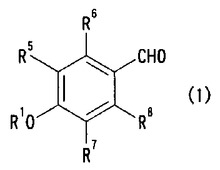
(式中、R1は保護基を示し、R5〜R8は夫々独立して水素原子又は置換基を示す。)で表されるベンズアルデヒド類と一般式(2)
【化2】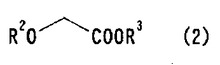
(式中、R2はアルキル基を示し、R3は炭化水素基を示す。)で表されるグリコール酸誘導体とを反応させた後、加水分解して一般式(4)
【化3】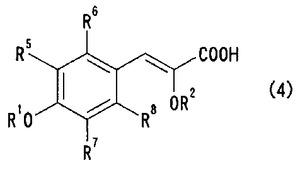
(式中、R1、R2及びR5〜R8は前記と同意義を有する。)で表されるけい皮酸類又はその塩を製造し、得られたけい皮酸類(4)又はその塩を不斉水素化反応に付して一般式(5)
【化4】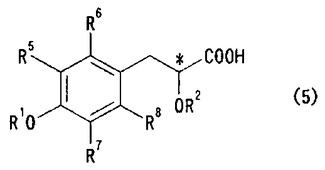
(式中、*は不斉炭素を示し、R1、R2及びR5〜R8は前記と同意義を有する。)で表される光学活性フェニルプロピオン酸類又はその塩を製造し、次いで脱保護することを特徴とする、一般式(6)
【化5】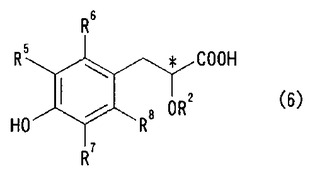
(式中、R2、R5〜R8及び*は前記と同意義を有する。)で表される光学活性3−(4−ヒドロキシフェニル)プロピオン酸類又はその塩の製造方法。
(もっと読む)
(+)−(2S,3S)−2−(3−クロロフェニル)−3,3,3−トリメチル−2−モルホリノール調製のための分割方法
動的速度論分割による、(+)−(2S,3S)−2−(3−クロロフェニル)−3,5,5−トリメチル−2−モルホリノールおよび(+)−(2S,3S)−2−(3−クロロフェニル)−3,5,5−トリメチル−2−モルホリノール塩酸塩のごとき医薬上許容される塩の調製方法が開示される。 (もっと読む)
光学的に純粋な2−モルフィノール誘導体を調製する新規な方法
本発明は、(+)−(2S,3S)−2−(3−クロロフェニル)−3,5,5−トリメチル−2−モルホリノールおよび(−)−(2R,3R)−2−(3−クロロフェニル)−3,5,5−トリメチル−2−モルホリノールの混合物から、光学的に純粋な(+)−(2S,3S)−2−(3−クロロフェニル)−3,5,5−トリメチル−2−モルホリノール、および医薬上許容される塩および溶媒和物を調製する方法に関する。この方法はマルチカラムクロマトグラフィー(MCC)、VARICOLおよびCyolojetなどの技法を含む、連続クロマトグラフィーを利用する。 (もっと読む)
3−アミノ・アルキルニトリルの光学分割
本発明は、光学的に活性なβ−アミノ・アルキルニトリルのキラルN−アセチル−アルファ−アミノ酸に、そして光学分割剤としてキラルN−アセチル−アルファ−アミノ酸を使用してラセミ体β−アミノ・アルキルニトリルを光学分割することによる光学活性なβ−アミノ・アルキルニトリルの製造方法にも関する。 (もっと読む)
癌の治療に使用の4−(ピラゾール−3−イルアミノ)ピリミジン誘導体
インスリン様増殖因子1受容体活性をヒトのような温血動物において変調させることに使用するための式(I)[式中、置換基は本文に定義される通りである]の化合物。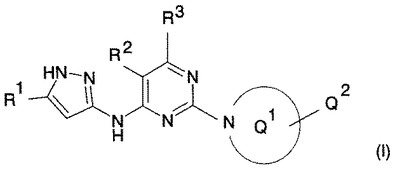
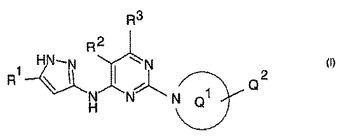 (もっと読む)
(もっと読む)
301 - 320 / 327
[ Back to top ]



