Fターム[2G043KA09]の内容
蛍光又は発光による材料の調査、分析 (54,565) | 使用波長及び特性 (7,100) | レーザ (1,911)
Fターム[2G043KA09]に分類される特許
1,861 - 1,880 / 1,911
生物学的サンプルにおける蛍光検出のための装置および方法
標本に起因するのではなく光学系に起因する発光の不均一性が、特殊な光学素子を使用することによって補正される、生物学的サンプルの蛍光検出のための装置および方法。この装置は、光源(105)を備え、この光源は、二色性ビームスプリッタ(110)を照射し、この二色性ビームスプリッタは、第一の光学素子(130)を通して、サンプル(122)のトレイを備えるサンプル領域(120)へと励起光を反射させる。この発光は、第一の光学素子(130)およびビームスプリッタ(110)を通り、検出器(125)へと再指向される。第一の光学素子(130)は、この発光を平行化し、そしてこの発光の不均一性を低下させる。 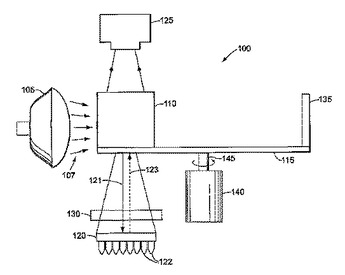 (もっと読む)
(もっと読む)
ダイナミックレンジを拡大する方法及びシステム
システムのダイナミックレンジの拡大の方法及びシステムを提供する。1つの方法は、粒子によって放射された蛍光を異なる強度を有する多重光路に分割し、多重信号を発生するための種々のチャネルを用いて多重光路内の蛍光を検出し、チャネルのどれがリニア範囲で動作しているかを多重信号に基づいて判定する。本方法は、異なる強度に対して補正するためにリニア範囲で動作中のチャネルによって発生された信号を変更する。別の方法は、異なる強度を有する光で多重照射域の粒子を照射し、多重信号を発生させるための多重照射域に位置している間に粒子によって放射された蛍光を別個に検出する。本方法は、信号のいずれがリニア範囲に位置するかを判定し、異なる強度に対して補正するためにリニア範囲にある信号を変更する。 (もっと読む)
ラマン分光法を使用して生物試料のタンパク質プロファイルを得る方法
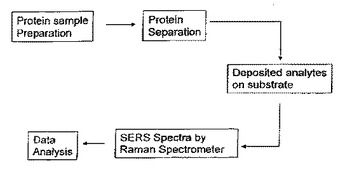
本発明は、例えば、特定の個人によって提供される試料のタンパク質プロファイルを得るために、生物試料のタンパク質含有量を分析するための方法を提供する。試料中のタンパク質およびタンパク質断片を化学的および/または物理的特性に基づいて分離し、固体基板上または流動中の液体の流れの離散的な位置に分離された状態で維持する。次いで、離散的な位置からのスペクトルが、離散的な位置の1つ以上の特定のタンパク質または断片の構造または識別についての情報を提供するように、離散的な位置において分離された状態のタンパク質または断片によって形成されるのでラマンスペクトルが検出される。離散的な位置のタンパク質または断片は、金または銀などの金属をコーティングされてもよいおよび/または分離されたタンパク質は、SERSスペクトルを提供するように化学的エンハンサーと接触されてもよい。本発明を実施する方法およびキットも提供されている。
 (もっと読む)
(もっと読む)
分子複製中のヌクレオチドの取り込みのラマン・モニタリングによる核酸配列決定
本明細書に開示された方法および装置は、ヌクレオチド、ヌクレオシド、および塩基の検出、ならびに核酸配列決定のために有用である。本方法は、表面増強ラマン分光法(SERS)を使用した、ヌクレオチド、ヌクレオシド、または塩基の検出を含む。検出は、核酸配列決定反応のような核酸重合反応の間のデオキシヌクレオチド三リン酸の取り込みを検出する核酸配列決定反応の一部であり得る。合成された新生鎖の核酸配列および鋳型鎖の相補配列が、重合反応の間のヌクレオチドの取り込みの順序を追跡することにより決定され得る。 (もっと読む)
網膜毒性のスクリーニング法
本発明は、蛍光検出可能なαvβ3及びαvβ5インテグリン特異的な作用物質及び網膜色素上皮細胞を用いる、被験物質を特徴付けする方法に関する。本発明はさらに、網膜色素上皮由来の細胞、インテグリンマーカー及び包装材料を含むキットに関する。 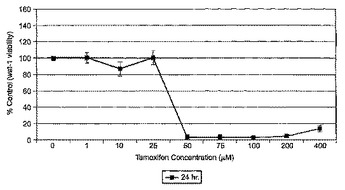 (もっと読む)
(もっと読む)
分子複製中のヌクレオチドの取り込みのラマン・モニタリングによる核酸配列決定
本明細書に開示された方法および装置は、ヌクレオチド、ヌクレオシド、および塩基の検出、ならびに核酸配列決定のために有用である。本方法は、表面増強ラマン分光法(SERS)または表面増強コヒーレント・アンチ・ストークス・ラマン分光法(SECARS)を使用した、ヌクレオチド、ヌクレオシド、または塩基の検出を含む。検出は、核酸配列決定反応のような核酸重合反応の間のデオキシヌクレオチド三リン酸の取り込みを検出する核酸配列決定反応の一部であり得る。合成された新生鎖の核酸配列および鋳型鎖の相補配列が、重合反応の間のヌクレオチドの取り込みの順序を追跡することにより決定され得る。塩基を糖部分から切断することによるヌクレオチドまたはヌクレオシドのSERSシグナルを増強する方法が提供される。さらに、単一塩基の繰り返しを検出する方法が提供される。 (もっと読む)
生体試料をアッセイするためにラマン活性プローブ構築物を使用するための方法および装置
体液中のタンパク質含有分析物などの生体試料中の分析物を検出するためのラマン活性またはSERS活性プローブ構築物を使用する種々の方法が提供される。本発明の方法が、試料中のタンパク質含有分析物または断片のアミノ酸組成についての情報を提供できるように、ラマン活性構築物におけるプローブ部分は、生体試料中の特定の公知の分析物に結合し、同定するように選択されるか、またはプローブ部分は、一定のアミノ酸に共通に見いだされる官能基と化学的に相互作用するようにデザインされる。患者試料のタンパク質プロフィールを作製することができるように、場合によっては、ラマン活性またはSERS活性プローブ構築物は、本発明の方法に使用したときに、特定のタンパク質含有分析物またはこのような分析物の型を同定することができる。ラマンのデータベースまたは正常な試料のSERSスペクトルと比較したときに、開示された方法を使用して患者の疾病状態を同定することができる。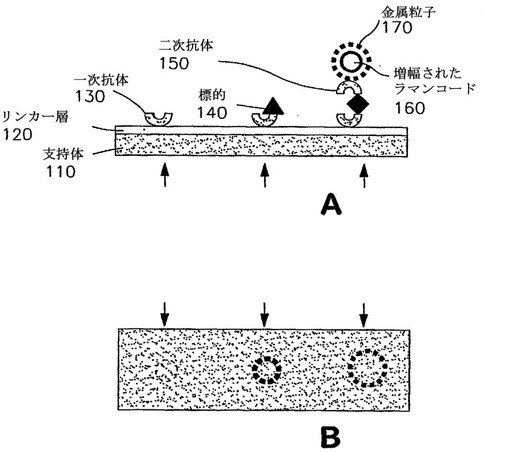
 (もっと読む)
(もっと読む)
表面増強ラマン分光法(SERS)活性複合体ナノ粒子、前記の製造の方法及び前記の使用の方法
ナノ粒子、これを準備する方法及びナノ粒子の実施形態を使用してターゲット分子を検出する方法が開示される。例示するナノ粒子の一つの実施形態は、とりわけ、表面増強ラマン分光法活性複合体ナノ構造を含む。表面増強ラマン分光法活性複合体ナノ構造は、コアと、少なくとも一つのレポーター分子と、カプセル化物質を含む。レポーター分子は、コアに結合されている。レポーター分子は、イソチオシアン酸塩染料、多硫化有機染料、多ヘテロ硫化有機染料、ベンゾトリアゾール染料及びこれらの組み合わせから選択される。カプセル化物質はコア及びレポーター分子の上に配置される。カプセル化物質によるカプセル化の後に、レポーター分子は測定可能な表面増強ラマン分光法形跡を有する。 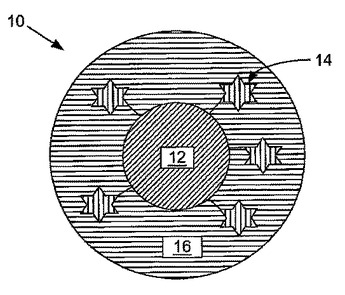 (もっと読む)
(もっと読む)
光学分析系、血液分析系、及び主成分の振幅を決定する方法
光学分析系(20)は、光信号の主成分の振幅を決定するように、配置される。その光学分析系(20)は、スペクトルの重み付けの関数によってその光信号を重み付けするための多変量光学素子(5,6)及びその重み付けされた光信号を検出するための検出器(7,8)を含む。その光信号は、その主成分及びそのスペクトルの重み付けの関数を設計するとき占められなかったさらなる成分を含む。従って、その検出された重み付けされた光信号は、その主成分の振幅に関係する部分及びそのさらなる成分のさらなる振幅に関係するさらなる部分を含む。その光学分析系(20)は、その検出された重み付けされた光信号を変調するための変調器素子(13)をさらに含む。その変調された検出された重み付けされた光信号とその検出された重み付けされた光信号との間の差は、その主成分の振幅に関係すると共に、このように、正確な方式でその主成分の振幅を決定することを許容する。血液分析系(40)は、このような光学分析系(20)を含む。主成分の振幅を決定する方法は、その光学分析系(20)を使用する。 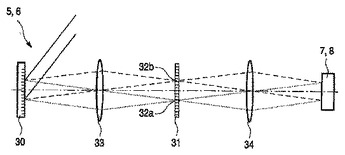 (もっと読む)
(もっと読む)
病原微生物検出のための広視野法
病原微生物は、当該病原微生物からのラマン光分散光と供にそのスペクトル・パターンのデジタル・パターン認識により、広視野で検出され、そして分類される。 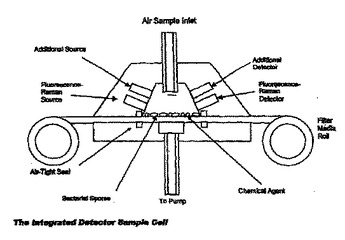 (もっと読む)
(もっと読む)
光量分布補正方法およびバイオチップ読取装置
【課題】一様な蛍光分布を呈する一様蛍光板を用いて励起光の基準光量分布画像を測定し、その画像により測定サンプルの画像を除算することにより、画像全体のシェーディングの影響を除去し、光量の非一様性を補正するようにした光量分布補正方法およびバイオチップ読取装置を提供する。
【解決手段】光ビーム照射により測定サンプルの画像を読取るバイオチップ読取装置において、一様な蛍光分布を呈する一様蛍光板を測定して得た画像の光量分布により、測定サンプルを測定して得た測定画像の対応する位置の画素の光量値を除算することにより、前記光ビーム照射光量の非一様性を補正する。
(もっと読む)
分光法のための方法及び装置
本発明は、分光法、特に、侵襲性又は非侵襲性血液分析のためのラマン分光法の方法を提供する。検出ボリュームから受信される戻り放射線の蛍光成分は削除され、それはパルス化励起光源用いることにより可能である。パルス長は、蛍光寿命より実質的に短い。それ故、蛍光成分の削除は、時間ゲーティング若しくは他のエレクトロニクス又は光テク手段により実行される。 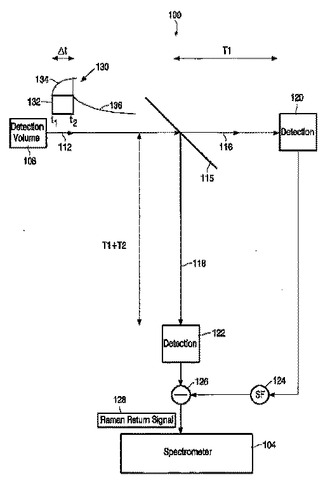 (もっと読む)
(もっと読む)
溶融金属の分析のための装置及び浸漬センサ及び方法
発光分光分析法を使用する、溶融材料、例えば鋳鉄あるいは鋼、あるいはスラグ、ガラスあるいは溶岩を分析するための方法及び装置が提供される。少なくとも一つの分光計と、被分析材料を励起させるための少なくとも一つの励起装置とを有する検出素子が使用される。被分析材料を励起させることにより被分析材料から放射物が部分的あるいは完全に発生され、発生した放射物が検出素子内の分光計により分析される。検出素子は溶融した被分析材料との接触状態に持ち来され、分光計によって供給される分析成分を含む情報を伝送する。本発明によれば浸漬センサも提供される。 (もっと読む)
多光子顕微鏡観察、分光法、および内視鏡観察などの生物学的用途のための光ファイバー送集光システム
本発明は、植物もしくは動物または他の貫通可能組織中の疾患を検出すること、または、植物もしくは動物の特定の組織を撮像することを目的として、光ファイバーを介して照射を行う方法に関する。さらに、そのような光ファイバーを介した照射を行うことにより、被検体内において蛍光および非線形散乱信号を検出および位置特定することができる。照射は、同時多光子励起を生じさせるのに有効な照射である。光ファイバーは、組織の内部領域を調べるため単独で使用するか、組織の表面下を調べるため光学生検針と併用するか、または体腔内の組織を調べるため内視鏡と併用する。本発明はまた、超短パルスモード同期レーザーから出力された照射を顕微鏡のビーム路にカップリングさせる装置にも関する。 (もっと読む)
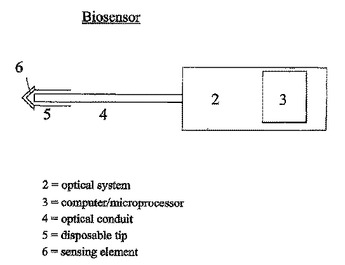
分析物を感知するための光ファイバ装置
分析物の濃度、特にグルコースの濃度を生体内または生体外で感知する装置が開示される。好ましくは光ファイバである光導管は、その近位端のところに光学系を有する。感知要素は、光導管の遠位端に付着され、少なくとも1種の標的分析物に結合するように適合された少なくとも1種の結合タンパク質を含む。この感知要素はさらに、分析物の濃度の変化とともに発光が変化する少なくとも1種のレポータ基を含む。任意選択で、感知要素は、分析物の濃度の変化によって実質的に変化しない発光特性を有する基準基を含む。
 (もっと読む)
(もっと読む)
ポリマー認証方法、認証可能ポリマー、認証可能ポリマー及び認証可能製品の製造方法、並びにそれで製造される製品
一実施形態では、試験ポリマーが認証可能ポリマーであることを認証する方法であって、認証可能ポリマーが基板ポリマーと熱変色性化合物とを含んでおり、熱変色性化合物が第一の温度及び認証波長で第一の信号を有するとともに、認証温度及び認証波長で第二の信号を有し、第一の信号と第二の信号とが異なり、認証温度が第一の温度より高い温度であり、当該方法が、試験ポリマーの一部分を認証温度に上昇させて加熱部分を生み出すのに十分な刺激に試験ポリマーを暴露し、認証波長で試験ポリマーの加熱部分の試験信号を測定し、試験信号が認証可能ポリマーの認証信号と同じであれば試験ポリマーが認証可能ポリマーであると認証することを含んでなる方法が開示される。 (もっと読む)
光アドレス可能なポリマーに基づく層構造体及び光導波路センサー
本発明は、少なくとも2つの層を含む光学層構造体、及び該層構造体に基づくセンサーに関する。層構造は、少なくとも1つの基材、少なくとも1つの(光)導波路層、及び光ビームをカップリングするカップリング素子を含んでなり、導波路層に隣接する層は、導波路層より小さい屈折率を有し、少なくとも1つの層は光アドレス可能なポリマーから作られている。 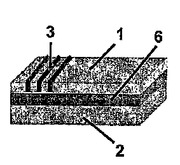 (もっと読む)
(もっと読む)
組織の蛍光発光を用いた糖化最終産物または疾病状態の尺度の決定
個体において組織状態(たとえば、糖化最終産物または疾病状態)の尺度を決定する方法が開示される。個体の組織の一部に光源サブシステム(A)からの励起光を照射し、励起光に応答した組織内化学物質の蛍光により組織によって放出される光を検出サブシステム(C)によって検出する。検出光を、組織の状態を決定するために蛍光を組織状態の尺度と関連付ける、信号処理装置(D)中に保存されたモデルと組み合わせる。組織の反射などの蛍光以外の光の検出による誤差を低減するために、補正技術を使用できる。組織状態の尺度の決定を補助するために、蛍光特性とともに他の生物学的情報を併用することもできる。 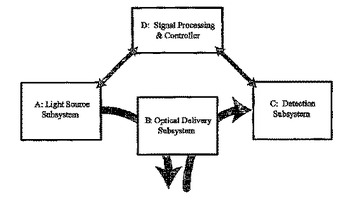 (もっと読む)
(もっと読む)
表面増感コヒーレント反ストークスラマン分光を用いた少数の分子を検出する方法および装置
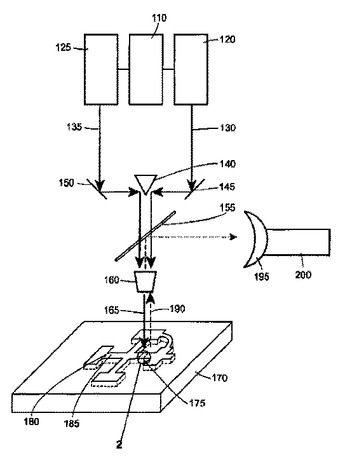
【解決手段】ここで開示されているデバイスおよび方法は、表面増感コヒーレント反ストークスラマン分光法を用いて、核酸のような複数の被分析物を高分解能および高速応答時間で、検出する段階、同定する段階、および/または、定量化する段階に関する。本発明のある実施形態によれば、核酸のような被分析物210の少量の分子試料が、マイクロ流体チャネル、マイクロチャネル、またはナノチャネル185およびラマン活性な表面を含む試料セル175を通り、表面増感コヒーレント反ストークスラマン分光法(SECARS)により検出される。本発明の他の実施形態は、被分析物の検出の装置に関する。
 (もっと読む)
(もっと読む)
流体の特性を決定する方法及び分光システム
本発明は、例えばインビボ血液分析の目的で、流体の特性を決定することを可能にする。まず、流体が流れる関心ボリュームの位置が、対物レンズを利用することによって光学的検出ステップによって決定される。好適には、光学的検出ステップは、イメージングステップである。次に、対物レンズは、対物レンズの焦点を関心ボリュームに至らせるように移動される。この位置において、光学分光ステップが実施される。これは、光学分光を実施するための測定ビームが最適な効率のために光軸に沿って進むという利点を有する。 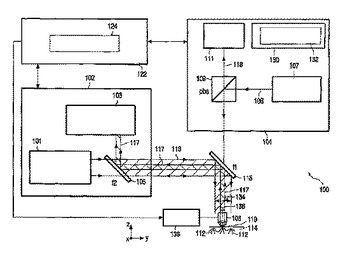 (もっと読む)
(もっと読む)
1,861 - 1,880 / 1,911
[ Back to top ]