Fターム[4H045CA11]の内容
Fターム[4H045CA11]に分類される特許
181 - 200 / 1,385
バイオフィルム破壊組成物
特定の実施形態では、本発明は、バイオフィルムを破壊するための化合物、組成物、及び方法に関する。いくつかの実施形態では、化合物及び組成物は、不飽和長鎖アルコール及び/又はアルデヒド、又はそのような化合物の組合せを含む。更なる実施形態では、本発明は、バイオフィルムがいったん破壊された後にバイオフィルムにおける細菌を低減及び/又は根絶することを助ける治療活性物質を含有する。 (もっと読む)
IgA1沈着症の治療
【課題】Ig(免疫グロブリン)A1沈着症を治療するために使用できる治療薬を提供する。
【解決手段】細菌のIgA1プロテアーゼをコードする第一DNA配列およびタグをコードする第二DNA配列を含む核酸分子であって、第二DNA配列がIgA1プロテアーゼ切断部位をコードするDNA配列の上流に位置することを特徴とする核酸分子。また、組織および器官におけるIgA1沈着を治療するための該IgA1プロテアーゼの使用。細菌のIgA1プロテアーゼはIgA1分子を特異的に切断するため、IgA1沈着を特異的に切断し、除去する。また、IgA腎症、疱疹状皮膚炎(DH)、およびヘノッホ・シェーンライン紫斑病(HS)を治療するための治療薬。
(もっと読む)
原核細胞における免疫原性多糖体生成の生合成システム
本発明は、N-グリコシル化タンパク質を含有する、バイオコンジュゲートワクチンに関する。更に本発明は、還元末端にN-アセチルガラクトサミンを有するオリゴ糖又は多糖を合成するエピメラーゼをコードしている核酸を含む、組換え原核細胞生合成システムに関する。本発明は更に、還元末端にN-アセチルガラクトサミンを有するオリゴ糖又は多糖を含むN-グリコシル化タンパク質、並びにそのようなN-グリコシル化タンパク質を生成する発現システム及び方法に関する。 (もっと読む)
マイコバクテリウム・ツベルクローシスesat−6遺伝子ファミリーベースの結核ワクチン及び診断法
【課題】esat-6遺伝子のメンバーによってエンコードされるアミノ酸配列からなるポリペプチドフラグメントを提供する。
【解決手段】esat-6遺伝子ファミリーのメンバーは、小さなタンパク質をエンコードする遺伝子として定義され、そのような2つの遺伝子は、ゲノム上に互いに隣合って配置されており、少なくとも1つの遺伝子産物がRv3874、Rv3875又はRv0288のいずれかと少なくとも15%同一のアミノ酸配列を有する。
(もっと読む)
エールリッヒア抗体の検出のためのペプチド、装置、および方法
本発明は、エールリッヒア抗原と結合する抗体の検出に有用な組成物(例えば、ペプチド組成物)を提供する。ペプチド組成物は、エールリッヒアOuter Membrane Protein1(OMP−1)タンパク質の免疫原性断片に基づくポリペプチド配列を含む。本発明はまた、そのようなペプチド組成物を含みかつエールリッヒア抗原と結合する抗体の検出および単球性エールリッヒア症の診断に有用な、装置、方法、およびキットも提供する。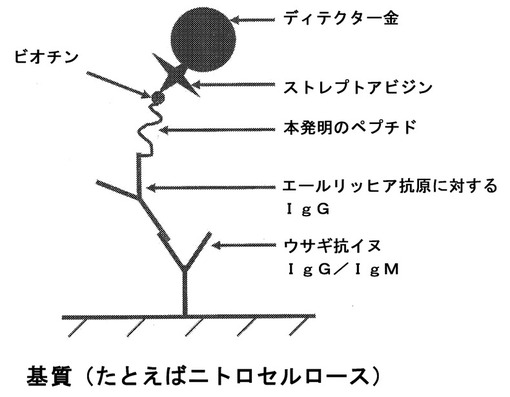
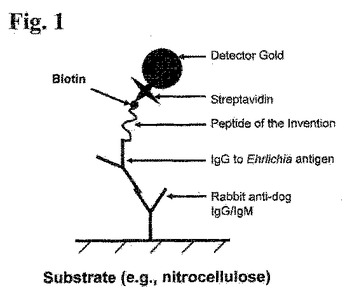 (もっと読む)
(もっと読む)
ヘテロクリティックアナログおよび関連方法
【課題】本発明は,対応する類似した野生型エピトープと比べて、免疫応答をもたらす増強された能力を有するエピトープを含むペプチドを、調製する方法を提供する。
【解決手段】クラスIエピトープのヘテロクリティックアナログは、これらのエピトープの3および/または5および/または7位で保存的または半保存的アミノ酸置換を提供することで調製される。このアナログは、対応する野生型エピトープに関連する免疫応答の誘発において有用である。本発明はまた、エピトープを含むペプチドの免疫原性を高める方法を提供する。本発明はまた、上記の方法によって得られ得るクラスIエピトープを含むペプチドを少なくとも1つ含む組成物を提供する。
(もっと読む)
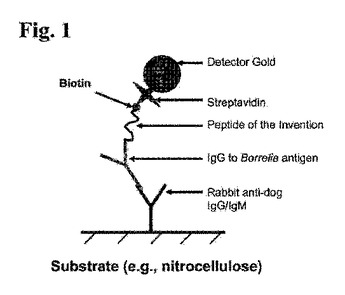
ライム病抗体の検出のためのペプチドおよび方法
本発明は、ボレリア抗原と結合する抗体の検出に有用な組成物(例えば、ペプチド組成物)を提供する。ペプチド組成物は、ボレリアVlsEタンパク質のIR6ドメイン中に変異体を含むポリペプチド配列を含む。本発明はさらに、そのようなペプチド組成物を含みかつボレリア抗原と結合する抗体の検出およびライム病の診断に有用な、装置、方法、およびキットも提供する。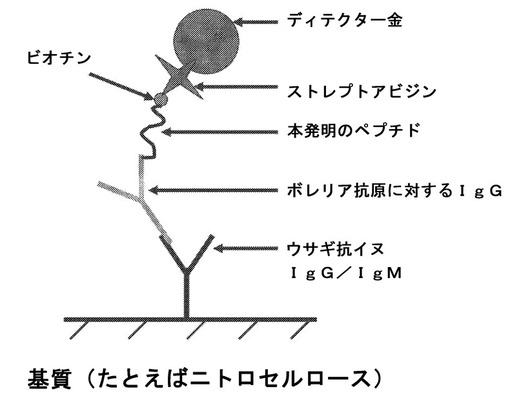
 (もっと読む)
(もっと読む)
黄色ブドウ球菌に由来する菌血症関連抗原
黄色ブドウ球菌のBAA抗原を、他の地方流行性の株および関連する株と比較してフィブロネクチンおよび他の細胞外基質タンパク質へのin vitro結合が増強された高度に菌血症性のMRSA株で同定した。BAAは、in vitroでフィブロネクチンに結合する、ファージにコードされた表面発現アドヘシンである。BAAはMRSA株のカテーテル関連菌血症の表現型の増強を引き起こし得るので、MRSA菌血症の予防のためのワクチン標的として有用である。 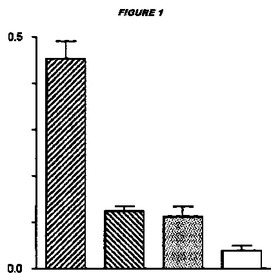 (もっと読む)
(もっと読む)
呼吸器管の治療及び予防のための方法、化合物、及び組成物
本発明は、呼吸器管の粘液レベルが高い対象の呼吸器管における粘液量を低下させる方法を提供する。この方法は、対象に、シアリダーゼ又はその有効成分と、アンカードメインを含む治療的有効量の融合タンパク質を含む化合物又は組成物を投与するステップを具える。この治療的有効量は、この化合物又は組成物を投与する前の粘液量に比べて、この化合物又は組成物を投与した後に呼吸器管の粘液量を低下させる融合タンパク質の量を含む。 (もっと読む)
ナイセリア抗原性ペプチド
【課題】Neisseria meningitidis B由来の、タンパク質、ポリペプチドおよびそのフラグメントを提供すること。
【解決手段】本発明は、Neisseria meningitidis B由来の、タンパク質、ポリペプチドおよびそのフラグメントを提供する。このタンパク質、ポリペプチドおよびフラグメントをコードする核酸、ならびにそれらに相補的な核酸(例えば、アンチセンス核酸)も提供される。本発明は、タンパク質、ポリペプチドおよび/またはフラグメントに結合する抗体を提供する。本発明は、タンパク質、ポリペプチドおよび/またはフラグメントを作製するために有用な発現ベクター、ならびにこのベクターを用いてトランスフェクトした宿主細胞を提供する。本発明は、ワクチン、診断薬、免疫原性組成物などに使用するための、タンパク質、ポリペプチド、フラグメントおよび/または核酸の組成物を提供する。
(もっと読む)
HER3結合ポリペプチド
本発明は、HER3結合モチーフ(BM)を含むHER3結合ポリペプチドを提供し、該モチーフは、
i) EX2X3X4A X6X7EIW X11LPNL X16X17X18QX20 X21AFIX25 X26LX28D、及び
ii) i)において定義される配列に対して少なくとも90%の同一性を有するアミノ酸配列
から選択されるアミノ酸配列からなり、ここで該ポリペプチドは、HER3の細胞外ドメインに結合する。HER3及びHER2に対して又はHER3及びEGFRに対して結合親和性を有し、かつ本明細書で定義されるHER3結合ポリペプチドとHER2結合ポリペプチド又はEGFR結合ポリペプチドとを含む、二重特異性リガンドも提供される。 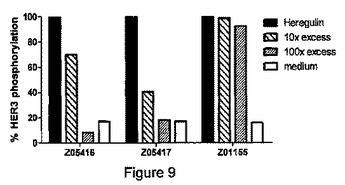 (もっと読む)
(もっと読む)
HBHAを使用した結核の検出およびMycobacteriumtuberculosisによる感染の検出
【課題】本発明は、哺乳類におけるMycobacterium tuberculosis感染のin vitro検出のための方法を提供することが目的である。
【解決手段】本発明は、潜在性の結核を示す哺乳類と活動性の結核を示す哺乳類とをin vitroで検出し区別する方法、または、健康な集団の中から潜在性の結核を示す哺乳類を同定する方法であって、a)前記哺乳類から生物学的サンプルを得ること;b)独立した方法で、前記生物学的サンプルを、天然型HBHAおよびESAT-6と接触させること;c)HBHAに特異的なIFN-γ分泌およびESAT-6に特異的なIFN-γ分泌を測定すること;ならびに、d)HBHAに特異的なIFN-γ分泌とESAT-6に特異的なIFN-γ分泌との比率を計算することを含み、潜在性の結核を示す哺乳類で得られた比率が、活動性の結核を示す哺乳類で得られた比率、またはM. tuberculosisに感染していない哺乳類で得られた比率よりも高い方法に関する。
(もっと読む)
T細胞刺激タンパク質Bおよび使用方法
N.メニンギティディスのT細胞刺激タンパク質B(TspB)に結合する抗体を誘発することができるポリペプチド、および使用方法が提供される。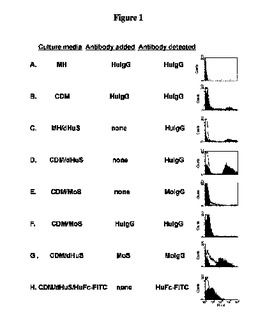 (もっと読む)
(もっと読む)
Staphylococcusaureus5型および8型の莢膜糖の精製
本発明は、S.aureus5型細胞またはS.aureus8型細胞から莢膜多糖を放出させるための方法であって、前記細胞を酸で処理するステップを含む方法を提供する。本発明は、この方法を含む、S.aureus5型細胞またはS.aureus8型細胞から莢膜多糖を精製するためのプロセスもさらに提供する。例えば核酸、タンパク質および/またはペプチドグリカン混入物を除去するための酵素処理;例えば低分子量混入物を除去するためのダイアフィルトレーション;例えば残存タンパク質を除去するためのアニオン交換クロマトグラフィー;ならびに濃縮のようなその他の処理ステップが、プロセスに含まれてよい。 (もっと読む)
コリスチンの精製方法および精製コリスチン成分
本発明は、酢酸および高エタノール濃度中のコリスチン塩基をカラムに装填する工程と低エタノール濃度で溶出する工程とが行われる、逆相クロマトグラフィーを用いるコリスチンの精製方法に関する。 (もっと読む)
2−アミノ−3−メチル−ヘキサ−5エン酸、及びバシトラシン等のペプチドの生成におけるその使用方法
本発明は、2−アミノ−3−メチル−ヘキサ−5−エン酸、バシトラシン等のペプチドの生成におけるその使用方法、及びそれを生成する方法に関する。 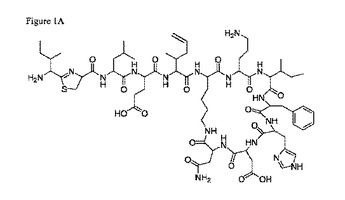 (もっと読む)
(もっと読む)
治療組成物又は美容組成物を局所的に塗布する装置及び方法
本発明は、局所的な治療組成物又は美容組成物を安全に再構成し、投与する装置及び方法に関する。本発明による局所塗布装置は、特に、毒性の高い物質を保存、再構成し、投与又は塗布するのに十分に適している。 (もっと読む)
プロセシングされていない及び部分的にプロセシングされたA型ニューロトキシンを測定するためのシステム
本発明は、ニューロトキシンの製造過程における品質管理及び安全性のためのツールに関する。特に本発明は、プロセシングされたボツリヌスニューロトキシンAポリペプチド(BoNT/A)並びに部分的にプロセシングされたBoNT/A及び/又はプロセシングされていないBoNT/Aを含む溶液中の、部分的にプロセシングされたBoNT/A及び/又はプロセシングされていないBoNT/Aの量を測定する方法であって、該溶液のサンプルを、部分的にプロセシングされたBoNT/A及びプロセシングされていないBoNT/Aと特異的に結合する捕捉抗体と、該抗体と該部分的にプロセシングされたBoNT/A及びプロセシングされていないBoNT/Aとの結合を可能にする条件下で接触させ、それにより複合体が形成されるステップと、形成された複合体の量を測定し、それにより該複合体の量が上記溶液中の部分的にプロセシングされたBoNT/A及び/又はプロセシングされていないBoNT/Aの量を示すステップとを含む方法に関する。さらに本発明は、上記方法を実施するためのデバイス及びキットに関する。 (もっと読む)
A群Streptococcusマーカーに基づくリウマチ性心疾患についての診断法および治療法
本発明は、Streptococcus pyogenes(A群Streptococcus;GAS)と関連するリウマチ性心疾患(RHD)を有する患者の同定、およびGAS感染と関連するRHDを発症するリスクがある患者の同定の分野に属する。本発明はまた、GAS感染と関連するRHDを予防および処置するための方法および組成物も提供する。一局面において、患者においてGAS感染と関連するリウマチ性心疾患(RHD)を診断する、またはGAS感染と関連するRHDを発症するリスクがある患者を同定する方法が提供され、この方法は、a)患者に由来する生物学的試料を少なくとも1つのGAS抗原と、該少なくとも1つのGAS抗原に対する、該生物学的試料中に存在する任意の抗体の結合に適した条件下で、接触させるステップなどを包含する。 (もっと読む)
ナイセリア属のタンパク質のハイブリッド発現
【課題】タンパク質の異種発現のための代替的かつ改善されたアプローチを提供すること。
【解決手段】これらのアプローチは、典型的に発現レベル、精製の容易さ、発現の細胞内局在、および/または発現タンパク質の免疫学的特性に影響する。本発明は、2つの利点を提供する。第1に、それ自体では不安定またはほとんど発現され得ないタンパク質は、その問題を克服する適切なハイブリッドパートナーを付加することによって支援され得る。第2に商業生産が簡素化される(2つの別個に有用なタンパク質を生成するために、たった1つの発現および精製しか使用される必要がない)。したがって、本発明は、2つ以上の本発明のタンパク質の同時異種発現のための方法を提供し、この方法において、その2つ以上の本発明のタンパク質は融合される(すなわち、それらは、単一ポリペプチド鎖として翻訳される)。
(もっと読む)
181 - 200 / 1,385
[ Back to top ]