Fターム[2G041LA07]の内容
その他の電気的手段による材料の調査、分析 (22,023) | 信号処理 (1,307) | データベース (491) | 物質同定用 (414)
Fターム[2G041LA07]に分類される特許
241 - 260 / 414
質量分析バイオマーカーアッセイ
本発明は、サンプル中の1つ以上のポリペプチドバイオマーカーの存在を決定する方法であって、以下のステップ:(a)サンプルを質量分光(MS)分析に供し、検出される各シグナルについて、保持時間指数と対応する質量とを記録するステップ;(b)各シグナルに対応する質量を参照データベースのバイオマーカーの質量と関連付けて、各シグナルと参照バイオマーカーとの相関関係を形成し、参照バイオマーカーの質量と相関しない質量のシグナルを棄てるステップ;(c)参照バイオマーカーと相関する質量のシグナルを保存するステップ;(d)類似性測度を用いて各シグナルのMSスペクトルをデータベース中の参照バイオマーカーのMSスペクトルとマッチングさせることにより、保存された各シグナルと参照バイオマーカーとの相関関係を確認し、正相関シグナルのセットを定義するステップ;(d)各正相関シグナルの強度を測定し、その絶対シグナル強度または相対シグナル強度を、判別関数を用いてスコア化するステップ;(e)判別関数から得られたスコア値に閾値を適用し、バイオマーカーの存在または不在を決定するステップ、
を含んでなる、上記方法を提供する。
(もっと読む)
デノボシーケンス解析方法,解析ソフト,解析ソフトを記憶した記憶媒体,試薬キット
【課題】衝突誘起解裂を備えた液体クロマトグラフ質量分析計より得られたマススペクトルからデノボシーケンス解析を行う場合、N末端を含むb系列とC末端を含むy系列の値を区別ができないため、正確なアミノ酸配列が困難である。
【解決手段】酵素消化するさいに、縮合効率の高いリジルエンドペプチダーゼ(Lys−C)酵素などを用いてC末端側に質量数の大きな官能基を導入する。導入後、質量分析計で測定するとy系列(官能基の導入されていない)と官能基が導入されているb系列を質量分析計の質量数から簡単に判別できるにする。
(もっと読む)
イオン付着質量分析方法
【課題】 少なくとも2種類の同質量・異成分の被測定ガスのガス分子を正確に区別して定性・定量分析できるイオン付着質量分析方法を提供する。
【解決手段】 このイオン付着質量分析方法は、イオン放出体18により発生させたイオンを被測定ガスの分子に付着させて付着イオンを生成し、Qポール質量分析器30で付着イオンの質量を計測し、被測定ガスの定性・定量を行う方法であり、さらに、少なくとも2種類の同質量・異成分の被測定ガスの分子に、被測定ガスの分子の各々が有するイオン付着特性の差を生じさせる所定のイオンを付着させるステップと、被測定ガスの分子の各々が有するイオン付着特性の差に基づいて被測定ガスの同質量・異成分を区別して計測するステップとを有する。
(もっと読む)
メタンから製造された芳香族炭化水素の同位体分析による同定
特定の重水素と13Cの分布を有するベンゼンとキシレンに関し、ベンゼンとキシレンの両者のδ(重水素)が−250未満であり、ベンゼンのδ(13C)が−36を超え、キシレンのδ(13C)は−24未満である。ここで、δ(重水素)=(R’sample/R’standard−1)×1000で定義され、R’sampleはベンゼンまたはキシレン中の重水素と水素の存在比、R’standardは自然界での重水素と水素の存在比であり、また、δ(13C)=(R”sample/R”standard−1)×1000で定義され、R”sampleはベンゼン/キシレン中の13Cと12Cの存在比、R”standardは、自然界での13Cと12Cの存在比である。 (もっと読む)
多発性硬化症を診断するための生物マーカー、及びその方法
本発明は、異なる型の多発性硬化症を診断及び鑑別診断するための方法を説明する。本方法は、臨床的に診断された再発寛解型又は一次性進行型の形態の多発性硬化症を罹病している患者に由来する試料内の、代謝産物と呼ばれる特定の低分子の強度を測定し、それらの強度を健常者の集団内で認められる強度と比較し、したがって多発性硬化症のマーカーを同定する。方法は、再発寛解型多発性硬化症に苦しむ被検者を、二次性進行型多発性硬化症から鑑別診断することも提供する。 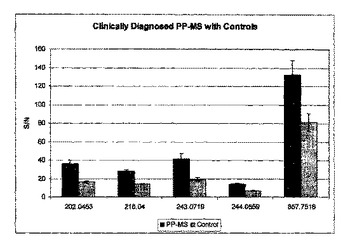 (もっと読む)
(もっと読む)
質量分析計
アナログ−デジタル変換器を備えるイオン検出器を備える飛行時間質量分析器を備えた質量分析計が開示される。アナログ−デジタル変換器からの信号がデジタル化され、イオンの到着時間および強度が決定される。各イオン到着イベントの到着時間T0および強度S0は、近接する時間ビンT(n)、T(n+1)に記憶された2つの別個の強度S(n)、S(n+1)に変換される。 (もっと読む)
質量スペクトルデータの解析
生のスペクトルデータを処理するによって、較正された連続スペクトルデータを得ること(210);較正されたライブラリーデータを形成するために処理されているライブラリースペクトルデータを得ること(240);及び生のスペクトルデータを生成した試料中の成分の濃度を測定するために(280)、較正された連続スペクトルデータと較正されたライブラリーデータの間で、好ましくは、マトリックス操作を用いて最少二乗フィッティングを実施すること(270)(式1);を含む、質量分析計からのデータを解析する方法。その方法に従って操作する質量分析計システム、変換された質量スペクトルのデータライブラリー、及びそのデータライブラリーを生成させるための方法。 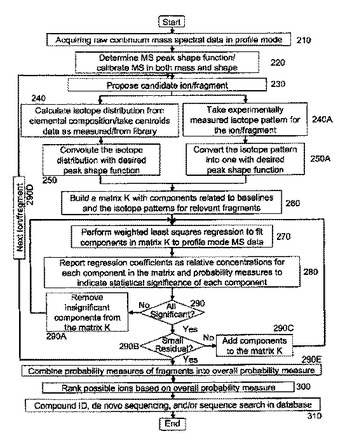 (もっと読む)
(もっと読む)
質量分析法を実施するための装置および方法
本発明の実施形態は質量分析法を実施するための装置および方法に向けられる。データ対情報がイオン検査処理を受け、ここで確認済み化合物に関連するデータ対情報はデータ対情報から取り除かれる。除去された情報は一層小さい信号を備えて存在する化合物に関するデータ対情報を一層容易に明らかにする。  (もっと読む)
(もっと読む)
細胞の迅速識別方法及び識別装置
【課題】バイオマーカーとして用いるタンパク質成分を確実に質量分析によって検出し、そのピーク質量をデータベースと比較することによって、信頼性の高い迅速な細胞識別方法と装置を提供する。
【解決手段】細胞内部から漏出させたバイオマーカータンパク質を質量分析した測定結果とデータベースとの一致性を指標として、細胞の種類を迅速に識別する。
(もっと読む)
ZAP−70相互作用分子の同定およびZAP−70の精製のための方法
本発明は、第一の局面において、(a) リン酸化ZAP-70を含有するタンパク質調製物を提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、(c) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体を所与の化合物とともにインキュベーションする段階、および(d) 化合物が固定化アミノピリド-ピリミジンリガンド24からリン酸化ZAP-70を分離できるかどうかを判定する段階を含む、ZAP-70相互作用化合物の同定法を提供する。第二の局面において、本発明は、(a) リン酸化ZAP-70を含有するタンパク質調製物を提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、所与の化合物および固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、ならびに(c) 段階(b)において形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体を検出する段階を含む、ZAP-70相互作用化合物の同定法に関する。第三の局面において、本発明は、(a) リン酸化ZAP-70を含有するタンパク質調製物の二つのアリコートを提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24と一方のアリコートを接触させる段階、(c) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、所与の化合物および固体支持体に固定化されたアミノピリド-ピリミジンリガンド24ともう一方のアリコートを接触させる段階、ならびに(d) 段階(b)および(c)において形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の量を測定する段階を含む、ZAP-70相互作用化合物の同定法を提供する。第四の局面において、本発明は、(a) リン酸化ZAP-70を含有する少なくとも一つの細胞をそれぞれ含む二つのアリコートを提供する段階、(b) 一方のアリコートを所与の化合物とともにインキュベーションする段階、(c) それぞれのアリコートの細胞を収集する段階、(d) タンパク質調製物を得るために細胞を溶解させる段階、(e) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、ならびに(f) 段階(e)においてそれぞれのアリコートで形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の量を測定する段階を含む、ZAP-70相互作用化合物の同定法に関する。
 (もっと読む)
(もっと読む)
タンパク質結合部位同定技術
【課題】抗原抗体反応のようなタンパク質間相互作用においてその結合部位を効率的に同定する手法を提供すること。
【解決手段】相互作用する第1のタンパク質と第2のタンパク質について、前記第1のタンパク質を支持体上に固定化し、前記第2のタンパク質を断片化して、前記第1のタンパク質に添加し、前記第1のタンパク質に捕捉された前記第2のタンパク質断片を分離し、分離された前記第2のタンパク質断片のアミノ酸配列を質量分析により解析して、前記第1のタンパク質に対する前記第2のタンパク質の結合部位を同定する。
(もっと読む)
微量タンパク質の同定を可能にするMALDI型質量分析装置用サンプルプレート
【課題】微量タンパク質の同定を可能にするMALDI質量分析装置用サンプルプレートを提供する。
【解決手段】本発明の表面にタンパク質消化酵素が固相化されているマトリックス支援レーザー脱離イオン化法質量分析装置用サンプルプレートを用いることにより、微量タンパク質の同定が可能になり、溶液中微量タンパク質のMALDIによる同定を、実験操作上のロスなく、簡便かつ高スループットで実施することができる。
(もっと読む)
糖鎖異性体を分離同定する質量分析法
【課題】糖鎖の異性体混合物中の各異性体の構造情報を、より簡便かつ迅速に得る質量分析法を提供すること。
【解決手段】糖鎖異性体の混合物を用いてそれぞれの糖鎖異性体を分離同定する質量分析法であって、(1)糖鎖異性体の混合物に対し、基質特異性が判明している酵素反応を行う工程、(2)酵素反応を全く行っていない糖鎖異性体の混合物および最後に行った酵素反応後の反応物を質量分析する工程、(3)酵素反応を受けたり受けなかったりした糖鎖のm/zを検出する工程、を含むことを特徴とする質量分析法、並びに、それらのデータを搭載したデータベース。
(もっと読む)
ピークの検出を向上させる濾過器具および方法
質量分析データのピークの識別を向上させるフィルタおよび方法が開示される。具体的には、本発明は、質量スペクトルデータを生成する際に使用される生物流体を精製するためにホールアレイフィルタを使用する方法を含む。本発明の方法を使用して、疾患を識別し、診断する際に使用される質量スペクトルデータの関連ピークを増強し、または特定の疾患治療に対する反応を予測することができる。 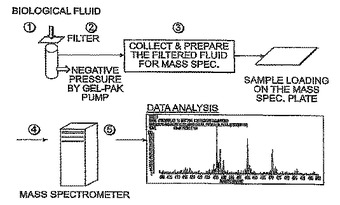 (もっと読む)
(もっと読む)
粘膜乾燥状態に関する検討
本発明は、医学的状態の診断および/または治療に関する。本発明は、被験体における粘膜乾燥状態を診断する、新規な方法に関する。この状態は、ドライアイであってもよい。本発明は、粘膜乾燥状態の治療効果をモニターする方法、粘膜乾燥状態を治療する方法、および/または粘膜乾燥状態用の診断キットも提供する。 (もっと読む)
疾患を有する患者に薬物が有効かどうかを決定するための方法およびシステム
患者から得た血清から質量分析計によって得られた試験スペクトルを取得することを含み、疾患または障害を治療するのに用いられる、疾患または障害を有する患者が薬物に応答するかどうかを決定する工程。該試験スペクトルを処理して、同一または類似の臨床段階の疾患または障害を有しており、かつ薬物に応答しているかまたは応答していないかが知られている他の患者からのそれぞれの血清から得たクラス標識したスペクトルの群に対する関係を決定しうる。該クラス標識したスペクトルの群に対する該試験スペクトルの関係に基づいて、該患者が該薬物に応答するかどうかについて決定がなされうる。  (もっと読む)
(もっと読む)
精神障害および/または腸のディスバイオシスのインビトロまたはエクスビボ診断方法
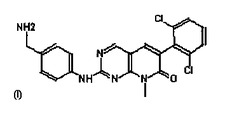
本発明は、少なくとも式(I)
(式中、n=1、Raは特に−COOHを表し、Rbは−CH3を表し、Zは特に−CH2CHOHを表し、該化合物は任意に塩の形態、または少なくとも一つの不斉炭素が存在するときには異性体単独もしくはラセミ混合物の形態であってもよい)の少なくとも一つの、精神障害および/または腸のディスバイオシスのインビトロまたはエクスビオ診断方法を実施するための生物学的標識としての使用。
(もっと読む)
子宮癌検出用マーカー
【課題】子宮癌の的確かつ簡易な検出に有用な子宮癌マーカー、および子宮癌の検出方法の提供。
【解決手段】質量 4,769±3(m/z)、6,254±4(m/z)または11,792±6(m/z)のいずれかを有する血中タンパク質からなる、子宮癌マーカーが開示されている。さらに、これら子宮癌マーカーを指標として用いる、子宮癌の検出方法が開示されている。
(もっと読む)
肺癌患者の術後予後予測のための生物マーカー及びその方法
【課題】肺癌患者の予後又は転移可能性を予測する方法を提供する。
【解決手段】ヒト肺癌患者の術後の予後又は転移可能性をインビトロで予測する方法であって、術後の予後がより良い又は転移可能性がより低い第1の患者群からの肺癌組織及び術後の予後がより悪い又は転移可能性がより高い第2の患者群からの肺癌組織の網羅的タンパク質発現プロファイルを取得すること、該網羅的タンパク質発現プロファイルについて該第1の患者群からの肺癌組織と該第2の患者群からの肺癌組織とを互いに区別可能なタンパク発現プロファイルを抽出すること、該第1の患者群と第2の患者群との間の該抽出された発現プロファイルを構成するタンパク質の相対的な発現レベルの差を指標にしてヒト肺癌患者の組織検体について術後の予後又は転移可能性を判定することを含む方法、並びにそのための組成物。
(もっと読む)
複合タンパク質混合物中の被分析タンパク質および/または被分析ペプチドを検出および/または増幅するための方法
本発明は、タンパク質および/またはペプチドを含むタンパク質混合物中の種々の被分析タンパク質および/または被分析ペプチドを検出および/または増幅するための方法に関する。この方法は、以下の工程、すなわちa)試料混合物を提供する工程、および、この混合物に含有されるタンパク質を必要に応じて規定のペプチドに断片化する工程、b)種々の被分析タンパク質および/または被分析ペプチドのうち少なくとも1種類のペプチドエピトープに特異的な第1の結合分子を提供する工程であって、このペプチドエピトープに含まれるアミノ酸が5個以下、好ましくは2〜3個である工程、c)第1の結合分子を試料混合物とともにインキュベートする工程、ならびにd)第1の結合分子に結合した種々の被分析タンパク質および/または被分析ペプチドを検出および/または増幅する工程、を含む。本発明はまた、種々の被分析ペプチドの末端ペプチドエピトープに特異的な結合分子に関し、この末端ペプチドエピトープは、遊離NH2基または遊離COOH基、プロテアーゼ特異性によって規定される1個以上のアミノ酸、および各場合において3個以下のさらなる末端アミノ酸を含む。 (もっと読む)
241 - 260 / 414
[ Back to top ]