Fターム[4B063QR16]の内容
酵素、微生物を含む測定、試験 (178,766) | 試薬 (61,469) | 試薬としての酵素 (8,175) | 加水分解酵素 (1,656) | 蛋白質,ペプチド分解酵素 (505)
Fターム[4B063QR16]に分類される特許
81 - 100 / 505
新規のペプチド、その調製プロセス、及びその使用
本発明は、一般式(I)によるペプチド、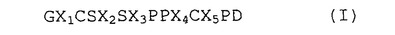
並びに、その薬剤的に許容可能な塩、エステル、及び薬剤的に許容可能なプロドラッグに関する。ここで、
X1は、Y、M、W、I、V、A、及び
X2は、R、K、及び
X3は、Y、F、I、M、L、E、D、H、及び
X4は、V、I、H、及び
X5は、I、V、Y、F、W、である。
更に、本発明は、それらを含む医薬調製物及びキット、それらを使用したスクリーニング及び単離方法、並びに医薬調製物の製造におけるそれらの使用に関する。
(もっと読む)
糖化アミンを測定するための試料の前処理方法および糖化アミンの測定方法
【課題】糖化アミンを測定対象物とする試料の前処理方法を提供し、信頼性に優れた糖化アミンの測定を可能にする。
【解決手段】試料中の糖化アミノ酸にフルクトシルアミノ酸オキシダーゼ(FAOD)を作用させて分解した後、さらに前記試料中の測定対象物である糖化アミンにFAODを作用させて、その酸化還元反応を測定することにより糖化アミンの量を測定する。糖化アミノ酸に作用させるFAODと糖化アミンに作用させるFAODとは、同じ基質特異性でも異なる基質特異性でもよい。同じFAODを使用する場合は、糖化アミノ酸にFAODを作用させて分解した後、プロテアーゼによって前記FAODを失活させると共に前記糖化アミンを分解し、この分解物に、さらに同じFAODを添加して作用させ、その酸化還元反応を測定する。
(もっと読む)
傷創感染を検出する方法
本発明は、以下の工程を含む傷創感染を検出する方法に関する:
−創傷から得られたサンプルを、リゾチーム、エラスターゼ、カテプシン Gおよびミエロペルオキシダーゼからなる群から選択される少なくとも2つの酵素に対する少なくとも2つの基質と接触させる工程、および、
−少なくとも2つの基質の該少なくとも2つの酵素による変換が測定される場合に、傷創感染が検出される工程。
(もっと読む)
糖化アミンを測定するための試料の前処理方法および糖化アミンの測定方法
【課題】糖化アミンを測定対象物とする試料の前処理方法を提供し、信頼性に優れた糖化アミンの測定を可能にする。
【解決手段】試料中の糖化アミノ酸にフルクトシルアミノ酸オキシダーゼ(FAOD)を作用させて分解した後、さらに前記試料中の測定対象物である糖化アミンにFAODを作用させて、その酸化還元反応を測定することにより糖化アミンの量を測定する。糖化アミノ酸に作用させるFAODと糖化アミンに作用させるFAODとは、同じ基質特異性でも異なる基質特異性でもよい。同じFAODを使用する場合は、糖化アミノ酸にFAODを作用させて分解した後、プロテアーゼによって前記FAODを失活させると共に前記糖化アミンを分解し、この分解物に、さらに同じFAODを添加して作用させ、その酸化還元反応を測定する。
(もっと読む)
骨粗鬆症、骨形成不全症、又は骨密度形成不良症の発症リスクを診断する方法
【課題】骨粗鬆症、骨形成不全症、又は骨密度形成不良症の発症リスクを診断する方法、並びに発現遺伝子の塩基置換を検出する方法を提供する。
【解決手段】女性の爪を検体とし、エストロゲン受容体発現遺伝子、LDL受容体関連タンパク5発現遺伝子、及びI型コラーゲン発現遺伝子の少なくとも1つの発現遺伝子における塩基置換を検出することを特徴とする、骨粗鬆症、骨形成不全症、又は骨密度形成不良症の発症リスクを診断する方法。
(もっと読む)
メタロプロテアーゼによるミオスタチンの活性化、およびミオスタチン活性の調節法
【課題】筋肉の成長および発達の調節に関与するミオスタチンの活性を調節し、筋ジストロフィー症、悪液質、および筋減少症(sarcopenia)などの筋肉消耗障害の治療に臨床的な効果方法および組成物を提供。
【解決手段】メタロプロテアーゼが媒介するミオスタチンの活性化を調節する薬剤を同定する方法と共に、このような方法で同定される薬剤により、メタロプロテアーゼによるミオスタチンプロペプチドの切断を増やすか、または減らすことで生物体の筋肉の成長を調節する方法。
(もっと読む)
草種の同定のための方法
本発明は、組成物中の少なくとも一つの草種からの抽出物の存在を決定するための、配列番号1、配列番号2、配列番号3、配列番号4、及び配列番号5からなる群から選択される配列を含む、又はからなる少なくとも一つのペプチドの使用に関する。 (もっと読む)
アポトーシスを調節する方法および組成物
【課題】小胞体膜貫通グルコース調節タンパク質78(GRP78)の活性を調節することによって、アポトーシスを調節する組成物および方法の提供。
【解決手段】アポトーシスを媒介する細胞質ゾル成分とのグルコース調節タンパク質(GRP)の相互作用を調節する薬剤に、GRPを接触させることを含む方法。前記GRPが小胞体に局在する、方法。前記GRPがGRP94またはGRP78である、方法。前記アポトーシスを媒介する細胞質ゾル成分がカスパーゼである、方法。
(もっと読む)
フルクトシルリジンの影響が低減する糖化タンパク質測定用試薬組成物
【課題】フルクトシルリジンの影響を低減させる糖化タンパク質測定用試薬組成物を提供する。
【解決手段】プロテアーゼ、フルクトシルアミノ酸オキシダーゼを含む糖化タンパク質測定用試薬組成物において、アミノ酸置換がされており、HbA1cである糖化タンパク質においてフルクトシルバリルヒスチジンに対する活性値を100とした場合、フルクトシルリジンに対する活性値が12以下であるフルクトシルアミノ酸オキシダーゼを備える薬組成物。
(もっと読む)
妊娠関連血漿蛋白−A2(PAPP−A2)
【課題】ヒト胎盤から単離され、配列決定分析により特徴付けられる核酸を提供する。
【解決手段】精製ポリヌクレオチドであって、i)受け入れ番号DSM13783下のDSMZに集積された、PAPP−A2のコード化配列に相当する、特定の配列を含むポリヌクレオチド;およびii)特定のアミノ酸配列を有するポリペプチドをエンコードするポリヌクレオチド;およびiii)ポリヌクレオチド(i)または(ii)によりエンコードされたポリペプチドのフラグメントをエンコードするポリヌクレオチド;およびそのようなポリヌクレオチドの相補鎖、からなる群から選ばれる、精製ポリヌクレオチド。
(もっと読む)
口腔用組成物の抗骨喪失および抗付着喪失作用
口腔の疾患および病気を処置するのに有用な化合物を同定するための方法を本明細書で記述する。 (もっと読む)
免疫系調節エンドペプチターゼ活性アッセイ
本明細書は、組成物を誘導するSNAP−25免疫反応、BoNT/A開裂部位切断可能結合のP1残基にカルボキシル末端を有するSNAP−25を含むエピトープに選択的に結合するα−SNAP−25抗体の作成方法、BoNT/A開裂部位切断可能結合のP1残基にカルボキシル末端を有するSNAP−25を含むエピトープに選択的に結合するα−SNAP−25抗体、再標的化エンドペプチダーゼ活性の検出方法、及び中和α−再標的化エンドペプチダーゼ抗体の検出方法を開示する。  (もっと読む)
(もっと読む)
微生物夾雑物の検出のための方法および組成物
【課題】サンプル中の微生物夾雑物の存在および/または量を決定するための試験カートリッジを提供すること。
【解決手段】本発明は、サンプル中の微生物夾雑物(例えば、細菌エンドトキシンまたはグルカン)の検出および/または定量のための方法および組成物を提供する。特に、本発明は、サンプル中の微生物夾雑物の検出および/または定量のための血球溶解物ベースのアッセイの実施において有用な試験カートリッジを提供する。さらに、本発明は、このようなカートリッジの作製方法および使用方法を提供する。さらに、本発明は、サンプル中の微生物夾雑物の検出およびまたは定量のために、迅速で、感度の高い、多工程の動的血球溶解物ベースのアッセイを提供する。さらに、本発明は、動的アッセイを行うために必要に応じて構成された種々のアッセイ形式(例えば、試験カートリッジを含む)において使用され得るグルカン特異的溶解物を提供する。
(もっと読む)
糖化ヘモグロビン測定用試料の測定方法
【課題】糖化ヘモグロビン測定用の試料を酵素法により正確に測定するための方法の提供。
【解決手段】酵素法によりヘモグロビン安定化剤が添加された糖化ヘモグロビン測定用試料を測定する方法において、該試料とチオール封鎖剤とを混合した後、酵素法による測定に付することを特徴とする糖化ヘモグロビン測定用試料の測定方法。
(もっと読む)
コアギュロゲン原料及びその製造方法、それを用いた生物由来の生理活性物質の測定方法及び測定装置
【課題】LAL試薬、あるいは、生物由来の生理活性物質に汚染されたLAL試薬等におけるコアギュロゲンの機能を維持したまま凝固酵素活性を不可逆的に不活性化し、試薬に利用可能なコアギュロゲン原料を取得する技術を提供する。
【解決手段】LAL試薬をある所定温度で所定時間に亘って加熱処理することにより、LAL試薬中の酵素活性のみを不可逆的に失活させる。その際、活性化した凝固酵素により加水分解されコアギュリンとなってゲル化や凝集反応を惹起するという、コアギュロゲン本来の活性は維持させる。
(もっと読む)
生物発光・蛍光プローブ用アンカーペプチド
【課題】従来の情報認識タンパク質のリガンドの結合により生じる立体構造変化を生物発光又は蛍光により検知し測定する可視化プローブ(蛍光・生物発光イメージングプローブ)の安定性を改善し、検出限界、検出範囲、選択性、感度などの性能を向上させる。
【解決手段】従来型の蛍光・生物発光プローブに、コリプレッサー活性化ペプチド、例えばコリプレッサー配列由来の「LXXIIXXXL」モチーフを含むペプチドをアンカーペプチドとして導入した。さらに、円順列置換(CP)を併用して各要素の結合順序を大幅に組み換える。
(もっと読む)
プラスミン活性を決定するための組成物、キットおよび方法
蛍光発生ペプチド基質を使用してプラスミン活性を決定するための組成物、キットおよび方法が提供される。 (もっと読む)
免疫グロブリングリコシル化パターン分析
本発明は、サブクラスIgG1又はIgG4のヒト免疫グロブリンあるいはサブクラスIgG2a又はIgG3のマウス免疫グロブリンのグリコシル化パターンの決定のための方法に関し、以下の工程:a)酵素IdeSを用いた酵素消化により前記免疫グロブリンをフラグメントに切断すること、b)酵素消化により得られる前記免疫グロブリンのフラグメントを、逆相高速液体クロマトグラフィーにより分離すること、c)工程b)において得られる前記免疫グロブリンの分離フラグメントを、マススペクトロメトリー分析に供すること、及びd)前記免疫グロブリンのグリコシル化パターンを、工程c)において得られるマススペクトロメトリーデータから決定すること、を含む。 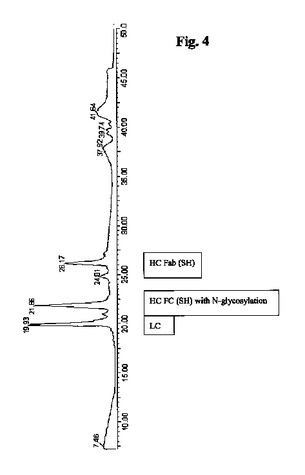 (もっと読む)
(もっと読む)
凍結乾燥ダビガトラン
本発明は、凍結乾燥状態の式Iで表わされるダビガトラン、ダビガトランエテキシラートの薬力学的効果を求めるアッセイにおけるキャリブレーターとしての前記ダビガトランの使用、ならびに、そのようなアッセイ自体に関する。凍結乾燥標準品を調製する際には、ダビガトランを酸水溶液に溶解した後に凍結乾燥を行う。
【化1】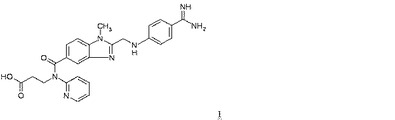
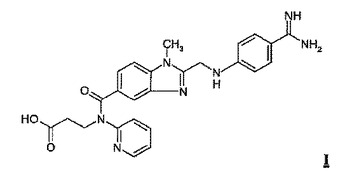 (もっと読む)
(もっと読む)
CHO細胞由来の糖タンパク質産物におけるガラクトース−α−1,3−ガラクトース含有N−グリカン
本発明は、哺乳類細胞発現系から発現されたタンパク質において特定のグリカン構造を検出するための方法および材料に関する。本発明は、チャイニーズハムスター卵巣(CHO)細胞集団を、前記細胞によって産生される末端ガラクトース−α−1,3−ガラクトース残基を含有するグリカンを測定することで、評価するための方法であって、CHO細胞が、α−ガラクトシルトランスフェラーゼコード配列を発現するよう遺伝子操作されたものではない、方法を提供するものである。 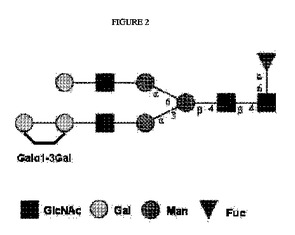 (もっと読む)
(もっと読む)
81 - 100 / 505
[ Back to top ]