Fターム[4B063QS24]の内容
酵素、微生物を含む測定、試験 (178,766) | 処理,操作 (34,251) | 測定,試験における各種前処理,中間処理 (13,775) | 検出物,試薬等の増量,増幅(←増殖) (8,475)
Fターム[4B063QS24]の下位に属するFターム
Fターム[4B063QS24]に分類される特許
1,241 - 1,260 / 1,324
増殖性疾患の治療のための組合せ法
本発明は、増殖性疾患(例えば癌)を治療する薬物の組合せを特徴としている。本発明は、癌および他の増殖性疾患の治療のために新規組合せ療法を同定する方法も特徴としている。 (もっと読む)
細胞脱分化を誘導するための組成物および方法
本発明は、系列決定済み哺乳類細胞を脱分化するための組成物および方法を提供する。
 (もっと読む)
(もっと読む)
ヒトアグレカナーゼ1遺伝子の5’フランキング領域のクローニングおよび特徴付け
Aggプロモーターを含む核酸および同一物を用いる方法を開示する。本発明はまたAggプロモーターの活性に基づく疾患を同定および処置する方法をも提供する。 (もっと読む)
血小板への雑菌混入検出を目的とするペプチドグリカンに基づく迅速アッセイ法
本発明は、サンプル中のペプチドグリカンもしくは(1−3)−β−D−グルカンを検出することにより、細菌または菌類病原体を検出するための比色法に関する。 (もっと読む)
分節化されたマイナス鎖RNAウイルスの検出のための方法および組成物
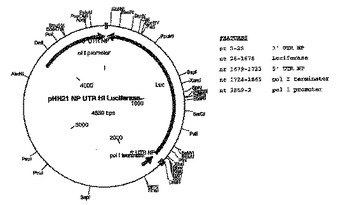
本発明は、インフルエンザウイルスのごとき分節化されたマイナス鎖RNAウイルスの存在、不存在または量の検出のための組成物および方法を提供する。好ましくは、アンチセンス配向における、分節化されたマイナス鎖RNAウイルスの5’UTRおよび3'UTRならびにレポーター遺伝子のオープンリーディングフレームを含む人工セグメントを含む遺伝子改変された脊椎動物細胞を、分節化されたマイナス鎖ウイルスを含むことが疑われる生物学的試料と接触させる。分節化されたマイナス鎖RNAウイルスでの細胞の感染の結果、そのレポーター遺伝子によりコード化されたポリペプチドを発現する。また、本発明の遺伝子改変された細胞は、人工セグメントをコードする組換えDNAを含むことができる。その組換えDNAは、人工セグメントの転写を指令するRNAポリメラーゼI用のプロモーターを含むことができる。
 (もっと読む)
(もっと読む)
バクテリオシン含有乳酸菌培養物の製造法及びそれを用いる食品の保存方法
ワイセラ属等の乳酸菌を培養することによりプロテアーゼ耐性バクテリオシンを含有する乳酸菌培養物を製造することができ、該培養物を食品に用いることで食品の保存性を高めることができる。 (もっと読む)
電位色素及びカルシウム色素を用いた新規の細胞ベースアッセイ
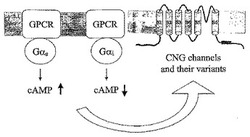
例えば、Gタンパク質共役受容体の刺激に反応した細胞内cAMP濃度の変化を検出するのに、環状ヌクレオチド作動性チャネル並びに蛍光色素及び他の指示体を利用する新規の組成物および方法を開示する。cAMPに対する感度を増強し、かつ2価カチオンによって媒介された遮断を低減する1つ又は複数のチャンネル孔変異を含むCNG変異体が、Gタンパク質共役受容体活性の検出を含めた、様々なアッセイで使用される。タンパク質相互作用の細胞ベースのアッセイに特に適した新規の色素クエンチャー調合物も開示する。 (もっと読む)
HCVNS3−NS4Aプロテアーゼ耐性突然変異体
本発明は、HCV NS3/4Aプロテアーゼの突然変異体に指向される。より詳細には、本発明は、薬剤処理に対して耐性であるHCV NS3/4Aプロテアーゼの突然変異体を同定する。 (もっと読む)
モナチンおよびモナチン前駆体の製造
グルコース、トリプトファン、インドール−3−乳酸、インドール−3−ピルビン酸および2−ヒドロキシ2−(インドール−3−イルメチル)−4−ケトグルタル酸より、モナチンまたはその塩を産生するために使用可能である方法および組成物を提供する。インドール−3−ピルビン酸および2−ヒドロキシ2−(インドール−3−イルメチル)−4−ケトグルタル酸中間体を産生するための方法も開示されている。提供される組成物には、核酸分子、ポリペプチド、化学構造物および細胞が含まれる。方法には、インビトロおよびインビボ工程が含まれ、インビトロ方法には、化学的反応が含まれる。 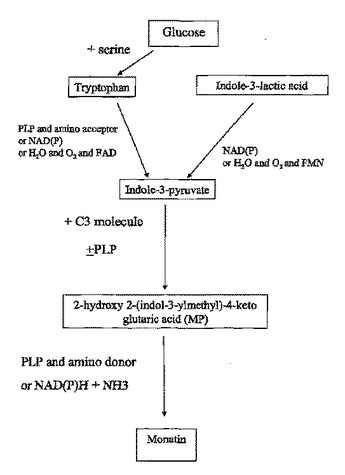 (もっと読む)
(もっと読む)
細菌の広域スペクトルの検出に有用な方法、ペプチドおよびバイオセンサー
本明細書中には、アルファ−1−プロテイナーゼ阻害剤の反応性部位ループ(RSL)ドメインの改変から誘導されるペプチド基質を試料と接触させることによる、創傷感染の検出および試料内の細菌、例えば創傷細菌の存在または非存在を検出するための方法が記載される。本発明において、我々はアルファ1タンパク質を有しないペプチド基質がペプチド基質として効率的に使用できることを証明した。細菌により産生および/または分泌される酵素によるペプチド基質の改変または改変の非存在は、試料内に細菌の存在または非存在の指標として役立つことができる。本発明は試料内の細菌の存在または非存在を検出するためのバイオセンサーも特徴とする。 (もっと読む)
比色基質、比色センサー、および使用方法
本明細書中には、ペプチドに付着された少なくとも1種の比色成分を含んでなる基質、ならびに該基質の改変を検出する方法が記載されている。また、試料と基質を接触させて、タンパク質、例えば微生物により産生されたタンパク質の存在または非存在を検出する方法が記載されている。試料が関係するタンパク質を含む場合には、基質は改変されそして目視できる色変化をもたらし、試料内のタンパク質の存在または非存在を示す。本発明は、試料内の微生物および/またはタンパク質の存在または非存在を検出するためのバイオセンサーおよびキットも特徴とする。 (もっと読む)
異なって発現される冠動脈疾患関連遺伝子
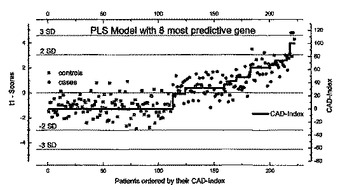
本発明は、その発現が冠動脈疾患の罹患と相関する遺伝子に関する。特に、本発明は、遺伝子発現の測定に基づく、冠動脈疾患の予後、診断およびモニタリング方法に関する。加えて、本発明は、冠動脈疾患の処置で使用するための化合物のスクリーニング方法、並びに冠動脈疾患の同定に使用するキットおよびアレイに関する。
 (もっと読む)
(もっと読む)
ゲノムDNA断片の選抜方法
植物に導入して農業上有益となる植物の改良を行うためのゲノムDNA断片の選抜方法を提供する。
本発明の方法は、(1) 植物からゲノムDNAを調製し、クローニングベクターを用いて、ゲノムDNAライブラリーを構築し;(2) ゲノムDNAライブラリーを構成する複数のゲノムクローンの各々に含まれるゲノム断片を、個別に植物に導入し、形質転換植物を作出し;
(3) 形質転換植物、または、その子孫の植物を栽培し、表現型に農業上有益となりうる変異の生じた植物を選抜し;(4) 工程(3) において選抜された植物に、工程(2) において導入されていたゲノムDNA断片を、目的とするゲノムDNA断片として選抜する;工程からなる。
(もっと読む)
受容体チロシンキナーゼ阻害剤の同定および/または確認のための方法
受容体チロシンキナーゼ阻害剤の同定および/または確認のためのin vivoでの方法が記載される。上記方法は以下の段階を特徴とする:a)受容体チロシンキナーゼのチロシンキナーゼドメインを含むペプチドをコードする核酸構築物を含む宿主細胞を提供すること、ここで上記ペプチドは膜貫通ドメインまたはその機能的フラグメントを欠如し、そして細胞質の上記チロシンキナーゼ活性は増殖阻止を導く:b)上記宿主細胞と候補化合物を接触させること、およびc)候補化合物によるチロシンキナーゼ活性の調節が細胞成長を導くような適切な条件下における上記宿主細胞の培養による上記チロシンキナーゼ活性の阻害剤の同定。 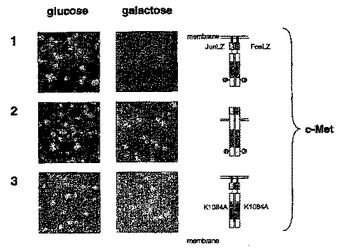 (もっと読む)
(もっと読む)
組織及び器官のインビトロでの発生
本発明は、分化組織の生成をもたらす微環境パラメータを発見する方法を提供し、その方法は、同種の多分化能細胞の少なくとも1つの集団を単離し、少なくとも1つの分化因子の存在下又は非存在下、固相スカフォールド上でその細胞を培養することを含む。本発明は、a)多分化能細胞の少なくとも1つの集団から誘導された複数のサンプルを得、b)三次元スカフォールド上で該細胞を培養し、少なくとも1つの実験パラメータが各サンプルに対して変更されており、及びc)制御された発生、自己アセンブリ又は分化に対して各サンプルを観察又は測定することを含む分化組織のスクリーニング方法を提供する。 (もっと読む)
酸化還元機能性アミノ酸のタンパク質への部位特異的組み入れ
組成物ならびに酸化還元機能性アミノ酸をタンパク質に組み入れる直交性tRNA、直交性アミノアシルtRNAシンテターゼ、およびtRNA/シンテターゼの直交性の対を含むタンパク質生合成機構の成分を産生させる方法を提供する。これらの直交性の対を使用して酸化還元機能性アミノ酸を伴うタンパク質を産生させる方法と共に、これらの直交性の対を同定する方法も提供する。 (もっと読む)
プレバイオティック効果の分析
(a)試験繊維又は試験物質による糞便細菌集団の増殖及び/又は変更に対する効果を評価するか、若しくは定量する段階と、及び(b)前記試験繊維又は試験物質の発酵によって生じる少なくとも1種類の生成物を定量する段階及び/又は前記試験繊維若しくは試験物質の同化率を定量する段階と、を含む前記繊維のプレバイオティック能力を評価するか、若しくは定量する方法又はプレバイオティック物質を同定する方法。 (もっと読む)
細胞の付着および増殖のための、共有結合によって付着したコラーゲンVI
細胞培養に有用な表面は、CAR物質が結合している支持体と、該CAR物質に結合しているコラーゲンVIまたは生物学的に活性なその断片もしくは変異体と、任意選択で、エラスチン、フィブロネクチン、ビトロネクチン、テネイシン、ラミニン、エンタクチン、アグリカン、デコリン、コラーゲンI、コラーゲンIII、およびコラーゲンIVなどの他のECMタンパク質(またはそれらの断片もしくは変異体)の1つまたは複数とを含む。ポリ−D−リジンまたはポリ−D−オルニチンなどのポリカチオン性ポリマーの1つまたは複数も、任意選択で該表面に存在する。この表面は、細胞培養において、(a)肝細胞(例えばHepG2腫瘍細胞および新たに発見されたラット肝臓上皮幹細胞系)、(b)マウス細胞系MC3T3細胞系などの骨芽細胞、ならびに、(c)初代骨髄細胞など、多数の異なった細胞型における細胞の付着、生存、および/または増殖を促進するのに使用される。該表面および追加の試薬を含むキットも開示する。 (もっと読む)
ヒドロラーゼ、それをコードする核酸並びにその製造および使用方法
本発明は、ヒドロラーゼ、それをコードするポリヌクレオチド、並びにこれらのポリヌクレオチドおよびポリペプチドを製造および使用する方法を提供する。ある特徴では、本発明は、ポリペプチド(例えばヒドロラーゼ活性(例えばエステラーゼ、アシラーゼ、リパーゼ、ホスホリパーゼ(例えばホスホリパーゼA、B、CおよびD活性、パタチン活性、脂質アシルヒドロラーゼ(LAH)活性)、またはプロテアーゼ活性であり、熱安定性および耐熱性のヒドロラーゼ活性を含む)を有する酵素)、およびこれらの酵素をコードするポリヌクレオチド、並びに、これらのポリヌクレオチドおよびポリペプチドの製造および使用を対象とする。本発明のポリペプチドおよびペプチドのヒドロラーゼ活性は、エステラーゼ活性、リパーゼ活性(脂質の加水分解)、酸分解反応(エステル化脂肪酸を遊離脂肪酸と交換するための反応)、エステル転移反応(トリグリセリド間の脂肪酸の交換)、エステル合成、エステル交換反応、ホスホリパーゼ活性およびプロテアーゼ活性(ペプチド結合の加水分解)を含む。本発明のポリペプチドは、化粧品および栄養補助食品の製造などを含む広範な薬学、農業、および工業用途に使用し得る。ある特徴では、本発明のポリペプチドはエナンチオマー的に純粋なキラル生成物の合成に使用される。 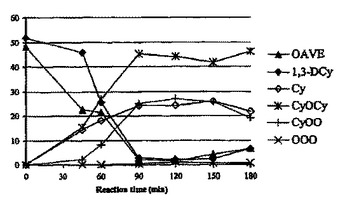 (もっと読む)
(もっと読む)
TIM−3ポリペプチド
本発明は、tim−3 IgVドメインおよびtim−3細胞内ドメインを含み、tim−3ムチンドメインまたはtim−3膜貫通ドメインを含まない単離ポリペプチドおよびポリペプチドをコードする核酸に関する。さらに、本発明は、治療有効量のtim−3活性を調整する薬剤を被験体に投与する工程を含む、被験体の免疫応答を調整する方法に関する。免疫応答には、免疫寛容、移植免疫寛容、Th1応答、およびTh2応答が含まれるが、これらに限定されない。 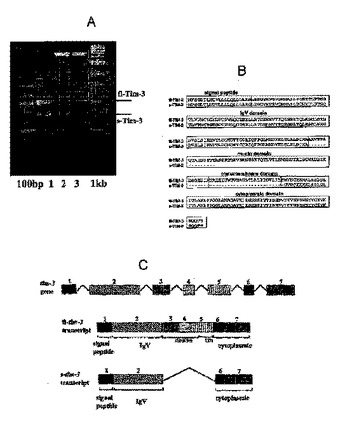 (もっと読む)
(もっと読む)
1,241 - 1,260 / 1,324
[ Back to top ]