Fターム[4H045DA75]の内容
ペプチド又は蛋白質 (143,989) | 機能によって特徴づけられるもの (16,938) | 免疫グロブリン(抗体) (7,528)
Fターム[4H045DA75]の下位に属するFターム
モノクロナール抗体 (4,713)
Fターム[4H045DA75]に分類される特許
1,981 - 2,000 / 2,815
ヒト−マウスキメラ抗呼吸シンシチアルウイルス抗体
【課題】少なくとも1つのモノクローナル抗体の可変重鎖および可変軽鎖のそれぞれのうち、少なくとも1個のCDRを含む、相補性決定領域(CDR)移植ヒト抗RSV抗原抗体を提供することである。モノクローナル抗体はいずれの非ヒト動物から誘導されてもよいが、望ましくは、げっ歯類、またもっとも望ましくはマウスの、モノクローナル抗体である。望ましくは、そのマウスモノクローナル抗体は中和抗体である。また、望ましくはマウス抗体は抗RSV F抗原抗体である。
【解決手段】この発明は、少なくとも一つのマウスモノクローナル抗体の可変重鎖および可変軽鎖のそれぞれに由来する一つのCDRを含む、MAb1129であるヒト抗呼吸シンシチアルウィルス抗体に関し、および、RSV感染の予防および/または治療のためのヒト抗呼吸シンシチアルウィルス抗体の使用に関する。
(もっと読む)
最適化特性を有するFc変異体
本発明は、最適化特性を有するFc変異体、それらの製造方法、最適化特性を有するFc変異体を含むFcポリペプチド、ならびに最適化特性を有するFc変異体の使用方法に関する。 (もっと読む)
癌高発現遺伝子
配列番号1−65のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント、これらを認識する抗体またはその抗原結合性フラグメント、または配列番号1−65のいずれかに記載されるヌクレオチド配列の少なくとも12個の連続するヌクレオチド配列もしくはこれに相補的なヌクレオチド配列を有するポリヌクレオチドが開示される。本発明の遺伝子およびタンパク質は、癌の診断および治療剤として有用である。  (もっと読む)
(もっと読む)
酸性環境中において高エステルペクチンを用いてタンパク質を安定化するためのプロセス
【課題】酸性環境であるがその環境の粘度に不利な影響を及ぼすことなくタンパク質を安定化する方法の提供。
【解決手段】以下:a)ペクチンをブロックワイズで酵素的に脱エステル化し得る精製PME酵素を、該ペクチン骨格の長さを実質的に減少するために酵素ポリガラクツロナーゼで事前に処理されていないペクチンに添加する工程;b)ペクチンをブロックワイズで酵素的に脱エステル化し得る精製PMEによって、該ペクチンからブロックワイズの酵素的に脱エステル化したペクチンを調製する工程;c)該ブロックワイズの酵素的脱エステル化したペクチンを少なくとも1つのタンパク質を含む酸性環境に添加する工程;およびd)該ブロックワイズの酵素的に脱エステル化したペクチンによって、該タンパク質を安定化する工程を包含する、プロセス。
(もっと読む)
GITR結合分子およびその使用
本発明は、T細胞および樹状細胞上でGITR、例えば、ヒトGITR(hGITR)に特異的に結合する結合分子を提供する。本発明の結合分子は、刺激剤、例えば、CD3の存在下で、hGITRに高いアフィニティーで結合することを特徴とし、アゴニスト的であり、Treg細胞によるTeff細胞の抑制を取り消す。本発明の種々のアスペクトは、結合分子、およびその医薬組成物、ならびにそのような結合分子を作製するための核酸、組換え発現ベクターおよび宿主細胞に関する。本発明の結合分子を用いて、インビトロまたはインビボでヒトGITRを検出し、またはヒトGITR活性を調節する方法も本発明に包含される。 (もっと読む)
ダイヤモンドチップへの蛋白質/ペプチドの固定化方法
【課題】蛋白質の機能を損なわずにチップ基板に蛋白質/ペプチドを固定化したり、基板上でその機能を損なわずに維持することができるように固定化する方法を提供すること。
【解決手段】化学修飾したダイヤモンド/DLC(Diamond-like Carbon)チップを活性化試薬により活性化した後、蛋白質/ペプチドを前記チップ上にスポッティングしてカップリング反応を行い、次いで未反応活性基のブロッキング操作を行う、チップ上に蛋白質/ペプチドを固定する方法において、スポティング添加剤として30%ジメチルスルホキシド(DMSO)又は30%ポリエチレングリコール(PEG)を用いたり、活性化試薬により活性化した後、MilliQ水で洗浄した後の乾燥を1時間の減圧乾燥処理により行う。
(もっと読む)
食道癌の抗原およびその利用
本発明の目的は、食道癌をはじめとする各種癌や腫瘍の診断・治療に応用することができるヒト食道癌抗原や、それをコードする遺伝子、それを用いた抗癌ワクチン等を提供することである。本発明によれば、配列番号1に示されるアミノ酸配列からなる蛋白質からなる抗原;上記の蛋白質の一部からなり、かつ免疫誘導活性を有するペプチド;該ペプチドを含む抗癌ワクチン;配列番号2に示される塩基配列又はその相補的配列並びにこれらの配列の一部または全部を含むDNA、該DNAを含む抗癌ワクチンが提供される。また、本発明の抗原蛋白は食道癌の悪性度に関係している可能性があり、その発現を抑制するRNAi(例えば、5’−GAACAGCACUCCUGGAAUC−3’など(配列番号17))は、本発明の抗原蛋白を高発現している食道癌などの治療に使うことができる。 (もっと読む)
再標的化
本発明は予め決定した特異性を有する免疫グロブリン分子の生成方法に関する。特に本発明は、優性のエピトープ結合特異性を示す単一可変ドメインを用いた、1以上の抗体のエピトープ結合特異性を再標的化する方法に関する。 (もっと読む)
可溶性ポリペプチドの単離方法
ポリペプチドをスクリーニングするためのハイスループット法を使用して、可溶性、安定性、高発現性、単量体性、結合特異性又は非凝集性等の望ましい生物物理学的特性を有するポリペプチド(単量体のヒトVH及びヒトVLを含む)を同定し、この方法は、ファージディスプレイライブラリを得る工程と、ライブラリファージによって細菌層の感染を可能にする工程と、細胞の層上の平均よりも大きいプラークを形成するファージを同定する工程とを含む。単量体のヒトVH及びヒトVLの配列を同定し、これは免疫治療に又は診断用薬剤として有用であり得る。ヒトVH及びヒトVLの多量体の複合体も同定する。同定されたVH及びVLを使用して、さらなるポリペプチドを同定するさらなるライブラリを作ることができる。さらに、VH及びVLをDNAシャッフリングにかけて、生物物理学的特性を改良するために選別することができる。 (もっと読む)
セネカバレーウイルスを基盤とする組成物及び疾患を治療する方法
本発明は、セネカバレーウイルス(「SVV」)と呼ばれる新規RNAピコルナウイルスに関連する。本発明は、単離したSVV核酸及びこれらの核酸でコードされるタンパク質を提供する。更に、本発明はSVVタンパク質に対して発生された抗体を提供する。SVVが腫瘍の幾つかの種類を選択的に死滅させる能力を有するので、本発明は、SVV及びSVVポリペプチドを使用して癌を治療する方法を提供する。SVVが特定の腫瘍を特異的に標的にするので、本発明は、SVV核酸及びタンパク質を使用して癌を検出する方法を提供する。加えて、SVVの腫瘍特異的な機構により提供される情報によって、本発明は、新たな腫瘍溶解ウイルス誘導体を作製する方法、及び腫瘍特異的親和性を有するようにウイルスを変える方法を提供する。  (もっと読む)
(もっと読む)
生体成分精製溶液、生体成分分離方法および生体成分分離装置
【課題】臨床プロテオーム解析をする際に、微量成分の検出に対して妨害となる過剰な
タンパク質を取り除くための方法を得る。
【解決手段】血液由来試料から、分子量6万のデキストランのふるい係数が0.001以上0.5以下であり、分子量3万のデキストランと分子量6万のデキストランの透過比率が3以上である分離膜を用いた分離システムを用い、更に分子量3万以上の特定のタンパク質に対するアフィニティーリガンドおよび/または抗体を用いて特定のタンパク質に対するアフィニティーリガンドおよび/または抗体を用いない場合に比べ、特定のタンパク質を10%以下の濃度に低減した生体成分分離方法および生体成分分離装置。
本分離方法および装置により得られた溶液は、質量分析、電気泳動、液体クロマトグラフィー等のプロテオーム解析を目的としたタンパク質分析に用いられ、高感度の分析が可能になる。
(もっと読む)
GDF−8モジュレート物質の検出
生体試料中の外因性のGDF−8モジュレート物質、例えば、GDF−8阻害物質の存在を検出するための方法を含む、ヒトを含む動物においてGDF−8モジュレート物質を検出するための方法が、本出願で提供される。特に、生体試料中のGDF−8モジュレート物質の存在および/または量を評価する方法が提供される。 (もっと読む)
ウイルス感染の治療及び予防又は治療及び予防の改善
HCV遺伝子型1〜6の各々を代表するHCV E2試料に結合することができる、抗体結合部位を含むポリペプチドをコードするポリヌクレオチド、並びにそのような性質を有するポリペプチド及びHCV感染を検出し治療する際のそのようなポリペプチドの使用を開示する。 (もっと読む)
TGFβ結合タンパク質のリガンドおよびその使用
予期しない特異的会合に関連する組成物および方法を提供し、これは、(i)複合体を形成する、TGFβ結合タンパク質スクレロスチンとBMPアンタゴニストタンパク質コーディンとの特異的会合、および(ii)複合体を形成する、TGFβ結合タンパク質スクレロスチンとBMPアンタゴニストタンパク質ノギンとの特異的会合であり、この複合体のいずれも、TGFβスーパーファミリーメンバー(例えば、BMP)に結合し得ない。本発明は、骨の鉱質化作用を調節する因子を同定するためのスクリーニングアッセイにおいて使用するための単離された複合体を提供し、他の関連する利点を提供する。 (もっと読む)
Gタンパク質共役レセプターリガンドおよび方法
【課題】Gタンパク質共役レセプターおよびこのレセプターに結合するリガンドの同定する方法等の提供。
【解決手段】SP9155レセプターのアゴニストまたはアンタゴニストを同定する方法であって:(a)標識した既知量のSP9155レセプターリガンドの存在下で、該アゴニストまたはアンタゴニストの存在について試験するサンプルと、SP9155レセプターまたはその機能的フラグメントとを接触する工程;および(b)該レセプターに特異的に結合した該リガンドの量を測定する工程、を包含し、該サンプルは、該レセプターへの該標識リガンドの結合の、該サンプルの非存在下で測定される結合と比較しての実質的な減少を測定することによりアンタゴニストまたはアゴニストを含むことが同定される、方法。
(もっと読む)
PD−1に対する抗体およびその使用
本開示は、PD−1(Programmed Death 1)のアゴニストおよび/またはアンタゴニストとして作用し得る抗体および抗体結合性フラグメントを提供するのであって、それによって、概して、免疫応答、ならびに詳細にはTcRおよびCD28によって介される免疫応答を調節する。これらの開示される組成物および方法は、例えば、自己免疫疾患、炎症性障害、アレルギー、移植拒絶、癌、および他の免疫系障害の処置において使用され得る。 (もっと読む)
抗体のフレームワーク・シャッフル
本発明は、抗体を再設計または再構成して、抗原に対する抗体の免疫特異性を維持する一方、抗体の免疫原性を低下させる方法に関する。特に、本発明は、フレームワーク領域のサブバンク由来のフレームワーク領域とインフレームで融合されたドナー抗体由来の相補性決定領域(CDR)を含んでなるコンビナトリアルライブラリーを合成することにより、抗原に免疫特異的な抗体を作製する方法を提供する。 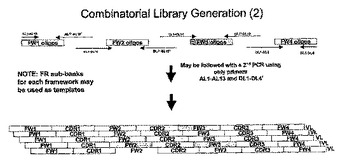 (もっと読む)
(もっと読む)
抗体精製
【課題】正しく折りたたまれジスルフィド結合した抗体断片を、正しく折りたたまれておらずかつ/または正しくジスルフィド結合していない汚染抗体断片から精製する方法の提供。
【解決手段】抗体と汚染物質を含有する混合物を、疎水相互作用クロマトグラフィーカラム(LPHIC)に添加し、そのカラムからpH2.5〜4.5の緩衝液で抗体を溶出させる抗体の精製方法。重鎖と軽鎖の間にジスルフィド結合を欠く抗体と不適切に結合した軽鎖および重鎖種が除去できる。
(もっと読む)
非アナフィラキシー誘発性IgEワクチン
【課題】本発明はIgE媒介アレルギー性疾患の治療および予防のためのワクチンとしての、2つの関係のない種のIgE分子のイプシロン重鎖のFc部分由来の抗原性ペプチドの組成物および使用法を提供する。特に、本発明は1以上の抗原性ペプチドの免疫原性量を含む、IgE媒介アレルギー性疾患の治療および予防のための組成物を提供する。
【解決手段】以下のものを含む単離された抗原性ペプチド:
(i)第1の種由来のIgE分子のCH3ドメインのアミノ酸残基;
(ii)第2の関連性のない種のIgE分子のCH3ドメインのアミノ酸残基、
ここで、第1の種由来のIgE分子のCH3ドメインのアミノ酸残基は第2の種のIgE分子のCH3ドメインに保存され、第2の種由来のIgE分子のCH3ドメインのアミノ酸残基は第1の種のIgE分子のCH3ドメインに保存されず、そして抗原性ペプチドは動物に投与するとき、アナフィラキシーを引き起こさない抗−IgE免疫反応を誘発する。
(もっと読む)
抗原エピトープの同定
本発明は、蛋白抗原のT細胞エピトープの同定および/または検出方法、蛋白抗原に対するペプチドワクチンの製造方法、受容体-リガンド複合体および/またはその成分の品質管理方法、少なくとも1つの固定化受容体ユニットまたは固定化受容体を有するナノ粒子の製造方法、受容体-リガンド固定化複合体、特にペプチド提示MHC分子を有するナノ粒子の製造方法、特定のCD4+-TまたはCD8+-Tリンパ球の末梢血単核細胞からの富化および/または分離方法、in vitroでのCD8+-Tリンパ球反応の初回抗原刺激方法、固定化受容体ユニット、特にMHC分子の固定鎖を有するナノ粒子、固定化受容体、特に固定化MHC分子を有するナノ粒子、受容体-リガンド固定化複合体、特にペプチド提示MHC分子を有するナノ粒子、ペプチドワクチン、蛋白抗原のT細胞エピトープの同定および/または検出用キット、ならびに、T細胞エピトープの同定および/または検出、ペプチドワクチンの製造、特異なTリンパ球の富化および/または分離、また、in vitroでのCD8+-Tリンパ球反応の初回抗原刺激を目的としたナノ粒子の適用に関する。 (もっと読む)
1,981 - 2,000 / 2,815
[ Back to top ]


