Fターム[4C076GG21]の内容
Fターム[4C076GG21]の下位に属するFターム
Fターム[4C076GG21]に分類される特許
41 - 60 / 228
固体脂を使ったマイクロカプセルの製造方法
【課題】親水性生理活性物質が高含量で封入され、食品や医薬品をはじめとした、幅広い用途に適応することのできる微細なマイクロカプセルを効率的に工業生産できる製造方法を提供する。
【解決手段】(1)固体脂と親水性生理活性物質含有水溶液の混合物を、固体脂の融点以上の温度で、乳化分散してW/Oエマルションを得る、(2)固体脂の融点以上かつ沸点未満の温度で、上記W/Oエマルション中の水分を除去してS/Oサスペンションを得る、(3)上記S/Oサスペンションを噴霧冷却することによって、S/Oサスペンション液滴を固体脂の融点未満まで冷却して固体脂を固化させる、工程を含有するS/O型マイクロカプセルの製造方法。
(もっと読む)
ナノ粒子メゲストロール製剤
【課題】ナノ粒子メゲストロールを含むナノ粒子活性組成物の提供。
【解決手段】メゲストロールと、薬剤の表面に結合した表面安定剤を含む組成物でメゲストロール粒子は、約2,000nm以下の有効平均粒径を有する。このナノ粒子メゲストロール組成物の利点は、例えば(1)低粘度の液体投与形態(2)飲みやすく消化しやすくコンプライアンスが向上(3)カップ又は注射器を用いることができ、投薬が容易(4)作用開始が速い(5)同じ薬理学的効果を得るのに必要なメゲストロールの用量が少ない(6)バイオアベイラビリィティが高い(7)薬物動態プロファイルが実質的に高い、等があげられる。
(もっと読む)
部位特異的タンパク質結合体を調製する方法
【課題】タンパク質−ポリマー結合体を迅速にかつ効率的に調製する方法を提供すること。
【解決手段】本発明は、インスリン−ポリマー結合体を含む、タンパク質−ポリマー結合体を迅速にかつ効率的に調製する単一工程の方法に関する。本発明の方法によると、タンパク質と親水性のポリマーを、少なくとも1種の有機溶媒および少なくとも1種の金属キレート剤の存在下で、上記タンパク質とポリマーの結合体の形成が促進される条件下で、接触させる。そのように、本発明は、インスリンのような選択されたタンパク質とポリ(エチレングリコール)との残基PheB1での位置特異的改変に関する。本発明はまた、生分解性ポリマーの結合体をカプセル化する薬学的処方物を提供する。
(もっと読む)
制御放出分配デバイス
「超圧縮」されて制御放出分配デバイスを形成するミクロ粒子またはナノ粒子の形で治療薬と組み合わされたポリマーを含む分配デバイス、および前記ミクロ粒子を使用して治療薬を局所投与する方法。 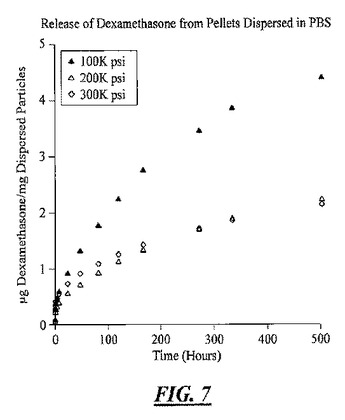 (もっと読む)
(もっと読む)
徐放性組成物およびその製造法
【課題】乳酸重合体またはその塩からなるマイクロカプセル中に水溶性の生理活性ペプチドが実質的に均一に分散した徐放性組成物の提供。
【解決手段】生理活性ペプチドをマイクロカプセル全体に対して15〜35(重量/重量)%の量で含有し、乳酸重合体の重量平均分子量(Mw)が約11,000〜約27,000であり、生理活性物質の高い含有量、投与から1日以内の初期過剰放出の抑制および長期間にわたる薬物の安定した徐放を行う徐放性組成物、およびその製造方法。
(もっと読む)
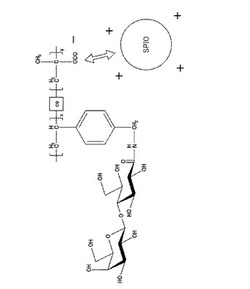
組織撮像用MRI造影剤
【課題】血中安定性、組織指向性及び腫瘍集積性に優れたMRI造影剤を提供する。
【解決手段】糖鎖含有モノマーとアニオンモノマーとの共重合体で表面修飾した超常磁性酸化鉄(Superparamagnetic iron oxide:SPIO)粒子を含む組織撮像用MRI造影剤。好ましくは、糖鎖含有モノマーの末端糖鎖が、ガラクトース、グルコース、マンノース、フコース、アセチルグルコサミン、アセチルガラクトサミンからなる群から選ばれる少なくとも1つであり、アニオンモノマーが、カルボン酸を側鎖にもつアミノ酸、リンゴ酸、メタクリル酸、マレイン酸、ビニル安息香酸及びアクリル酸を有するモノマーからなる群から選ばれる少なくとも1つである。
(もっと読む)
微生物または生物由来物質含有微細粒子およびその製造方法
【課題】微生物または生物由来物質を含有し、保存安定性に優れた微細粒子を提供する。
【解決手段】最外殻層と、中間層と、芯部とからなる3重構造を有する粒子であって、前記最外殻層が、ゼラチンおよび天然ガムを含む組成物からなり、該組成物の水溶液のゲル化温度が60℃以下であり、前記中間層が、40℃における粘度が250cps以下、かつ5℃における粘度が300cps以上である疎水性物質からなり、前記芯部が、微生物または生物由来物質を含有する組成物からなり、粒子全体の水分量が5%以下、かつ水分活性が0.5以下であることを特徴とする微生物または生物由来物質含有微細粒子。
(もっと読む)
ナノバブルの形成方法
【課題】超音波造影剤を用いるナノバブルの形成方法の提供。
【解決手段】本発明はナノバブルの形成方法を開示するものであり、前記形成方法は公知技術に使用する油水乳化反応とは異なる特徴を持つ。本発明のナノバブルの形成方法は、無機粒子を中心核として、前記中心核の表面に最低一つの第一高分子をコーティングして有機/無機複合粒子を形成する。次に、第一溶剤によって前記有機/無機複合粒子の中心核を溶解して除去し溶剤型ナノ粒子を形成する。続いて冷凍乾燥プロセスにおいて前記第一溶剤を除去し前記溶剤型ナノ粒子に中空ナノ粒子を形成させる。最後に前記中空ナノ粒子を第二溶剤に溶かして前記ナノバブルを形成する。
(もっと読む)
インビボにおける栄養素持続放出
長時間にわたり持続可能な時間制御型様式でインビボにおいて送達される栄養組成物は、運動パフォーマンスの増強、取り組んでいる仕事に対する手/眼の協調及び集中の向上を提供する。 (もっと読む)
ブロックコポリマーおよびその使用
酸化または加水分解に感受性の高い荷電ブロックまたは化学部分を含有するブロックコポリマーを開発した。本発明者らは、超分子構造(例えば、ミセルまたはベシクル)および医薬組成物、ならびに前記超分子構造および医薬組成物の調製方法における、こうしたブロックコポリマーの使用を記載する。本発明は、細胞への薬剤、例えば核酸の送達に特に有用である。 (もっと読む)
有効成分保持体
【課題】多分岐高分子を用い、有効成分を安定的かつ効果的に保持可能であり、有効成分が親水性あるいは疎水性のいずれであっても、有効成分の徐放性、溶解性などの有用な機能を実現することのできる有効成分保持体を提供する。
【解決手段】本発明にかかる有効成分保持体は、分子量500〜100000の分岐状ポリグリセリンの球状多分岐構造分子に所望の有効物質が保持されてなる構成を有し、好ましくは、前記球状多分岐構造分子の表面に存在する分岐状ポリグリセリンの末端水酸基と反応する化合物から構成され、前記球状多分岐構造分子の表面の少なくとも一部を覆うシェルを有する。
(もっと読む)
多層被覆粒子及びその製造方法並びにそれを含有する皮膚外用剤
【課題】薬効成分を製剤中に長期間安定となるように配合させ、かつ薬効成分を徐放させるべく、その放出性を制御できる技術の提供。
【解決手段】平均粒径が50nm〜1mmで薬効成分を含有する多孔性粒子が、正電荷を有する多糖重合体と負電荷を有するアクリル酸系重合体とを交互に吸着させて形成した重合体・積層膜により被覆された多層被覆粒子を用いる。該重合体・積層膜はその多孔性粒子を保護するシェルとしての機能を有しており、積層膜の厚さや密度を変化させることにより、その薬効成分の加水分解等に対する経時安定性を向上できる。
(もっと読む)
核酸送達系のための放出性カチオン脂質
本発明は、核酸の送達のための放出性カチオン脂質及びナノ粒子組成物、並びにそれを用いて標的遺伝子の発現を調節する方法を対象とする。特に、本発明は、酸不安定性リンカーを含むカチオン脂質、及びそれを含有するナノ粒子組成物に関する。 (もっと読む)
高分子微粒球の製造方法及びその方法により製造された高分子微粒球
本発明は高分子微粒球の製造方法及びその方法により製造された高分子微粒球に関するもので、具体的には高分子化合物、薬物、水不溶性有機溶媒及び分散溶媒を含む乳剤を製造する段階、及び製造された乳剤に塩基又は酸を添加し、水不溶性有機溶媒を乳剤から除去する段階を含む高分子微粒球の製造方法、その方法により製造された高分子微粒球及び前記微粒球を含む薬物伝達用組成物に関するものである。本発明は塩基又は酸を利用して水不溶性有機溶媒を乳剤から除去する新たな高分子微粒球の製造方法、前記製造方法により製造された高分子微粒球及び前記高分子微粒球を含む薬物伝達用組成物を提供する。従って、本発明の製造方法は既存の溶媒蒸発又は溶媒抽出工程とは異なり、少量の水を使用して廃水発生を最小化しながら短時間内に簡便に目的とする薬物含有高分子微粒球を製造するために使用できる。
 (もっと読む)
(もっと読む)
新規オリゴヌクレオチド、および脱色剤として、メラニン色素合成に含まれる酵素の発現を調節するオリゴヌクレオチドの使用
【課題】メラニン色素の合成経路に含まれる必須酵素の1つをコードする遺伝子および遺伝子転写物とハイブリダイズできる新規オリゴヌクレオチド配列、および/または、その誘導体を提供する。
【解決手段】チロシナーゼをコードする遺伝子もしくは遺伝子転写物、またはチロシナーゼ関連タンパク質1(TRP−1)をコードする遺伝子もしくは遺伝子転写物と特異的にハイブリダイズできる新規オリゴヌクレオチド配列。また、化粧用組成物または皮膚病用組成物における脱色剤または漂白剤としての、これらの新規オリゴヌクレオチド配列の使用。
(もっと読む)
プロリンベースの生分解性ポリマー
本発明は、プロリンから誘導され、最終的にポリエステルの熱重縮合(thermal polyesterification method)反応を行う2段階法により合成される連続ポリ(エステルアミド)を提供する。この方法により調製されるポリマーの分子量は、14,000Da〜約77,000Daである。本発明のプロリンベースのPEAの熱的特性を解明したところ、、そのガラス転移温度は、内部に水素結合がないため、他のα−アミノ酸ベースのポリ(エステルアミド)より低かった。こうしたプロリンベースのPEAは水溶液中でナノ粒子として集まり、疎水性小分子薬剤および生物学などの様々なカチオンおよび生物学と錯体を形成する。このため本発明のプロリンベースのPEAは、分子量が14,000Da〜約77,000Daの範囲のポリマーを必要とする薬物送達分野、および疎水性薬剤を送達するためのナノ粒子の製造に有用である。 (もっと読む)
T細胞抗原なしにIgG体液性応答を提供する免疫ナノ治療剤
本発明は、免疫系の細胞へのナノキャリアの送達のための組成物およびシステムを提供する。本発明は、抗体産生の形態で免疫系応答を誘導することができる合成ナノキャリアを提供し、ナノキャリアは、いかなるT細胞抗原も欠く。いくつかの実施形態では、本発明は、抗原提示細胞に対するナノキャリアの高いアビディティの結合をもたらす免疫特徴表面を含むナノキャリアを提供する。本発明は、本発明のナノキャリアを含む薬学的組成物を提供する。本発明は、本発明のナノキャリアおよびその薬学的組成物を設計し、製造し、使用するための方法を提供する。 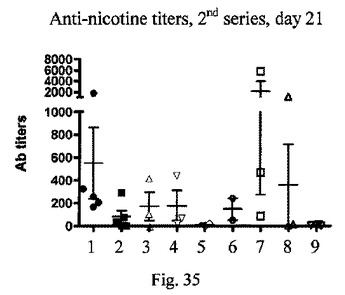 (もっと読む)
(もっと読む)
刺激可能な非対称ポリマーソーム
本発明は、非対称単層膜を有するポリマーベシクルに関し、該膜は、2つの異なる層、すなわち層(A)及び層(B)、によって構成されており、該2つの層は、該層(B)とは対照的に、少なくとも1つの刺激可能な疎水性ポリマーブロックを有する両親媒性ブロックコポリマーの有効量を有する層(A)を有する各両親媒性ブロックコポリマーを有し、該ブロックポリマーは、外因性刺激に応答して新規立体配置を採ることができる該コポリマーにより提供され、該単層膜の破裂を条件付ける。本発明は、該ベシクルの製造方法、該ベシクル中に活性成分をカプセル化する方法、該活性成分の制御された放出の方法も提供する。 (もっと読む)
調整可能な抽出速度を有する溶媒抽出マイクロカプセル化
本開示は、抽出相の制御された添加および/または除去を含む、溶媒抽出技術を使用した、微粒子の調製のためのプロセスに関する。本発明により例えば、微粒子を生成するためのプロセスであって、(a)連続プロセス媒体において、薬剤、ポリマー、および前記ポリマーのための第1の溶媒を含む第1の相を含むエマルションを形成することと、(b)前記微粒子を形成するために、前記第1の相から抽出相へ、前記第1の溶媒を抽出するために、原位置で、前記エマルションを前記抽出相に接触させることと、を含み、前記抽出相の一部分が連続的に除去され、補充抽出相流体が、前記抽出相に再び添加される、プロセスが提供される。 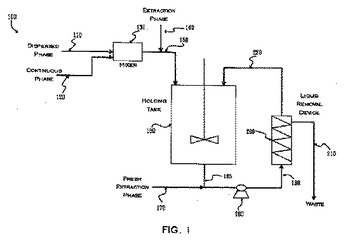 (もっと読む)
(もっと読む)
GLP−1ペプチドまたはその類似体をコードし、分泌する、封入された細胞を用いた、急性心筋梗塞(AMI)の処置
本願は、GLP−1、そのフラグメントまたはバリアント、あるいはGLP−1、そのフラグメントまたはバリアントを含んでいる融合ペプチドをコードし、分泌する細胞、例えば、間葉系の幹細胞または間葉系の間質細胞あるいは任意のさらなる適切な細胞の、急性心筋梗塞(AMIまたはMI)の処置のための、使用に関する。このGLP−1、そのフラグメントまたはバリアント、あるいはGLP−1、そのフラグメントまたはバリアントを含んでいる融合ペプチドをコードし、分泌する細胞は、処置される患者の免疫系の応答を防止するように、(球状の)マイクロカプセルに封入されている。また、本願は、これらの(球状の)マイクロカプセル、またはこれらの細胞もしくは(球状の)マイクロカプセルを含んでいる薬学的組成物の、急性心筋梗塞(AMIまたはMI)の処置のための使用にも関する。 (もっと読む)
41 - 60 / 228
[ Back to top ]