Fターム[4G169BE36]の内容
Fターム[4G169BE36]の下位に属するFターム
Fターム[4G169BE36]に分類される特許
241 - 260 / 263
α−アミノオキシケトン/α−アミノオキシアルデヒド及びα−ヒドロキシケトン/α−ヒドロキシアルデヒド化合物の製造方法並びに環式α,β−不飽和ケトン基質及びニトロソ基質からの反応生成物の製造方法
本発明は、α−アミノオキシケトン及びアルファ−ヒドロキシケトン化合物を製造する方法を対象とする。合成経路は通常、式(IV):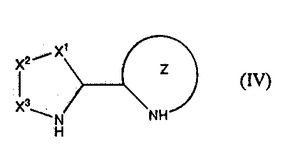
[上式中、X1〜X3は独立に、窒素、炭素、酸素又はイオウを表し、Zは、置換基を伴うか伴わない4〜10員環を表す]の触媒の存在下に、アルデヒド又はケトン基質とニトロソ基質とを反応させるステップ及び場合によって、生じたα−アミノオキシケトン化合物をαヒドロキシケトン化合物に変換させるさらなるステップを必要とする。本発明は、α−アミノオキシケトン及びアルファ−ヒドロキシケトン化合物を高いエナンチオ選択性及び高純度で生じさせる。本発明はさらに、触媒による不斉O−ニトロソアルドール/マイケル反応を対象とする。この反応の基質は通常、環式α,β−不飽和ケトン基質及びニトロソ基質である。この方法論は通常、プロリンベースの触媒の存在下に環式α,β−不飽和ケトン基質とニトロソ基質とを反応させて、複素環式生成物を得ることを含む。  (もっと読む)
(もっと読む)
遷移金属錯体
式(I)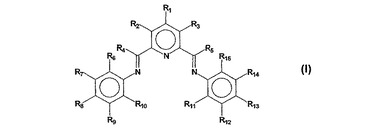
[式中、R1〜R5、R7〜R9、R12およびR14は、それぞれ独立に、水素、置換されていてもよいヒドロカルビル、不活性官能基であるか、互いに隣接した、R1〜R3およびR7〜R9の任意の2つを一緒にして環を形成することができ、R6は水素、置換されていてもよいヒドロカルビル、不活性官能基であるか、R7またはR4と一緒になって環を形成し、R10は水素、置換されていてもよいヒドロカルビル、不活性官能基であるか、R9またはR4と一緒になって環を形成し、R11は水素、置換されていてもよいヒドロカルビル、不活性官能基であるか、R12またはR5と一緒になって環を形成し、R15は水素、置換されていてもよいヒドロカルビル、不活性官能基であるか、R14またはR5と一緒になって環を形成し、ただし、R13は、およびR12とR14の少なくとも1つは、置換されていてもよいC1〜C30アルキル、置換されていてもよいC4〜C30アルキルオキシ、ハロゲンおよび置換されていてもよいC5〜C20アリールから独立に選択されるか、R13はR12またはR14と一緒になって環を形成し、またはR12はR11と一緒になって環を形成し、R14はR15と一緒になって環を形成し、R12、R13およびR14の少なくとも1つは置換されていてもよいC4〜C30アルキルオキシであり;Mは、Ti、V、Cr、Mn、Fe、Co、Ni、Pd、Rh、Ru、Mo、Nb、Zr、Hf、Ta、W、Re、Os、IrまたはPtから特に選択された遷移金属原子であり;nは遷移金属原子Mの形式的な酸化状態に等しく;Xはハロゲン化物、置換されていてもよいヒドロカルビル、アルコキシド、アミドまたは水素化物である。]を有するビス−アリールイミンピリジン配位子を含む、ビス−アリールイミンピリジンMXn錯体である遷移金属錯体。本発明の遷移金属錯体、非配位アニオンを有するこれらの錯体およびこのような錯体を含有する触媒系は、無極性媒質および化学的に不活性な無極性溶媒、特に芳香族炭化水素溶媒中で良好な溶解度を有する。この触媒系を、様々な(コ)オリゴマー化、重合および二量体化反応のために使用することができる。 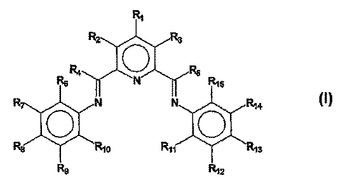 (もっと読む)
(もっと読む)
C1対称ビスホスフィンリガンド及びプレガバリンの不斉合成におけるそれらの使用
【課題】プレガバリン及び構造的に関連した化合物を製造するための材料及び方法を提供する。
【解決手段】遷移金属に結合されたC1対称ビスホスフィンリガンドを含む新規キラル触媒を用いて、プロキラルオレフィンのエナンチオ選択性水素化を経た(S)−(+)−3−(アミノメチル)−5−メチル−ヘキサン酸及び構造的に相関した化合物を製造する。
(もっと読む)
高分子内包ルイス酸金属触媒
【課題】 ルイス酸金属を高分子中に内包させ、ルイス酸金属触媒としての機能を保ったまま、この触媒の回収を可能とすることを目的とする。
【解決手段】 本発明は、ルイス酸金属を架橋高分子に内包させてなり、該架橋高分子が架橋性高分子に含まれる架橋基を架橋させてなる高分子内包ルイス酸金属触媒であって、該架橋性高分子が疎水性置換基及び架橋基を有する親水性置換基を有する少なくとも一種のモノマー単位を含み、かつ該疎水性置換基が芳香族置換基を含むことを特徴とする高分子内包ルイス酸金属触媒である。この架橋性高分子は、疎水性置換基及び架橋基を有する親水性置換基を有する少なくとも一種のモノマー単位、及び疎水性置換基を有するモノマー単位から成ることが好ましい。この触媒は、架橋性高分子とルイス酸金属とを含む有機溶液と、貧溶媒とを混合して得られたルイス酸金属内包ポリマーミセルを、架橋反応に付して得ることができる。この触媒は、アルドール反応、シアノ化反応、アリル化反応、マイケル反応、マンニッヒ反応、ディールスアルダー反応又はフリーデルクラフツ反応のための触媒として有用である。
(もっと読む)
オレフィンメタセシスおよび原子またはグループ移動反応に使用するための金属錯体
オレフィンメタセシスおよび原子またはグループ移動反応のような数多くの有機合成反応において有用な改良された触媒を、多座配位性シッフ塩基配位子と、1つ以上の他の配位子とを含む多配位金属錯体と酸とを、酸が少なくとも部分的に金属錯体の金属と多座配位性シッフ塩基配位子との間の結合を、任意でシッフ塩基配位子の中間体プロトン化を経て、開裂するような条件下で接触させることによって生成する。 (もっと読む)
触媒系
本発明は、エチレン系不飽和化合物のカルボニル化を触媒することが可能な触媒系であって、a)VIB族もしくはVIIIB族の金属またはそれらの化合物、b)二座ホスフィン、アルシンまたはスチビン配位子、およびc)酸を組み合わせることにより得られ、該配位子は、該金属または該金属化合物中の該金属に対して少なくとも2:1のmol過剰で存在し、該酸は、該配位子に対して少なくとも2:1のmol過剰で存在する、触媒系、エチレン系不飽和化合物をカルボニル化する方法、反応媒質および該触媒系の使用方法を提供する。 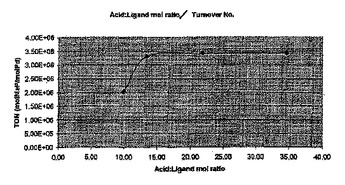 (もっと読む)
(もっと読む)
(1H−テトラゾール−5−イル)−ビフェニル誘導体の製造において有用なカップリング反応
本発明は、共通な構造的特徴として(1H−テトラゾール−5−イル)−ビフェニル環を含む、ARB(アンギオテンシンII受容体アンタゴニストまたはAT1受容体アンタゴニストとも呼ばれる)の製造のために使用されうる、中間体の製造方法に関する。 (もっと読む)
不斉変換触媒を製造するための方法
本発明は、キラルリガンドを製造するための方法であって、式(A):[式中、X★は、キラルまたはアキラル誘導基であり;(i)は、場合によっては、置換された単-または多-環式アリールまたはシクロアルキル基である]で表される出発物質を用意し;その基質をオルトリチオ化し;そのオルト-リチオ化された基質を、式-PR1R1”[R1は、置換および未置換分岐および直鎖アルキル、置換および未置換シクロアルキル、置換および未置換炭素環式アリール;および、置換および未置換ヘテロアリールから選択され、そのまたは各ヘテロ原子は、硫黄、窒素および酸素から独立に選択され、R1”は、R1とは異なり、置換および未置換分岐および直鎖アルキル、置換および未置換シクロサイクル、置換および未置換炭素環式アリール;および、置換および未置換ヘテロアリールから選択され、そのまたは各ヘテロ原子は、硫黄、窒素および酸素から独立に選択される]を有するホスフィン基に変換し;場合によっては、または、必要とされる場合には、X★を異なる基に変換して、キラルリガンドを生成させる方法に係る。 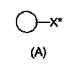 (もっと読む)
(もっと読む)
ペプチドまたは核酸マイクロパターン形成を使用してカーボンナノチューブを製造する方法
本明細書に開示する方法、装置およびシステムはカーボンナノチューブの規則アレイに関する。本発明の特定の態様では、ナノチューブアレイは、触媒ナノ粒子(140, 230)をポリマー(120, 210)に結合する段階、ポリマー(120, 210)分子を基板に結合する段階、ポリマー(120, 210)分子を脱離する段階および触媒ナノ粒子(140, 230)上でカーボンナノチューブを製造する段階を含む方法によって製造される。ポリマー(120, 210)分子整列法。ナノチューブアレイを基板の選択した領域(110, 310)に結合することができる。選択した領域(110, 310)内において、ナノチューブは非ランダムに分布される。本明細書に開示する他の態様は、基板に結合されている規則的アレイのナノチューブ、主張されている方法によって製造された、基板に結合されている規則的アレイのカーボンナノチューブを含むシステムに関する。ある態様において、2本鎖DNA分子に分子ワイヤーを連結することによって、分子ワイヤーを整列させる方法が本明細書において提供される。 (もっと読む)
芳香族炭化水素類の酸化における活性剤としてのアントラセン及び他の多環式芳香族化合物
本発明は、アントラセン又は他の多環式芳香族化合物の少なくとも1により活性化される少なくとも1の重金属酸化触媒及び臭素の存在下での芳香族カルボン酸類を製造するための芳香族炭化水素の液相酸化に関する。 (もっと読む)
シクロヘキセニルアルキルまたはアルケニルケトンの異性化法
本発明は、触媒としてルテニウムの有機金属前駆物質と酸との反応により得られるルテニウム錯体を使用して、2−アルキル−シクロヘキセ−3−エニルアルキルまたはアルケニルケトンを、相応する2−アルキル−シクロヘキセ−2−エニルケトンと相応する2−アルキレン−シクロヘキシルケトンとを含有する混合物へと炭素−炭素二重結合を異性化する方法に関する。 (もっと読む)
触媒およびその製造方法
本発明は、炭化水素変換用の貴金属触媒、気相技術に基づくその製造方法、開環、異性化、アルキル化、炭化水素改質、乾式改質、水素化および脱水素化反応のような反応における該触媒の使用、および中間留分の製造方法に関する。前記貴金属触媒は、支持体上に白金、パラジウム、ルテニウム、ロジウム、イリジウム、またはその組合せの混合物から選択される第VIII族金属を含み、該触媒は323K未満の温度で一酸化炭素を活性化する。 (もっと読む)
基質の触媒的漂白のためのビスピドン−誘導(bispidon−derivated)配位子およびこれらの錯体
本発明は、少なくとも1つのC8−C22−アルキル鎖を有する、式(I)の[3.3.1]ビシクロ化合物を含んでいる漂白組成物であって、過酸素源(I)を実質的に持っていない組成物を提供する。
 (もっと読む)
(もっと読む)
オレフィンモノマーの接触三量化
a)クロム、モリブデンまたはタングステン源、b)一般式(I);(R1)(R2)P−X−P(R3)(R4)(式中、Xは、二価有機架橋基であり、R1およびR3は、独立に、炭化水素基、置換炭化水素基、ヘテロ炭化水素基および置換へテロ炭化水素基から選択され(但し、R1およびR3が環状芳香族基である場合、それらは、いずれのオルト位置においても極性置換基を含まない)、R2およびR4は、独立に、場合によって置換された環状芳香族基から選択され、各R2およびR4は、オルト位置の少なくとも1つに極性置換基を有している)の配位子およびc)助触媒を含む、オレフィンモノマーの三量化に適した触媒組成物。本発明は、さらに、少なくとも1つのオレフィンモノマーを上記に記載された触媒組成物と接触させることを含む、オレフィンモノマーの三量化、特にエチレンの1−ヘキセンへの三量化方法に関する。 (もっと読む)
高多孔性ハニカムおよびその製造方法
自動車の触媒コンバータ・システムに使用するためのセラミック・ハニカム基体であって、2.0ミル(0.0508mm)を超える、好ましくは2.5ミル(0.0635mm)〜7ミル(0.1778mm)の、より好ましくは2.5ミル(0.0635mm)〜3ミル(0.1778mm)の壁厚を保ちながら、45〜75%の高い気孔率によって
改良された着火特性を示す。細孔径中央値は2〜10μm、25〜800℃における熱膨張係数(CTE)は5×10−7/℃未満である。 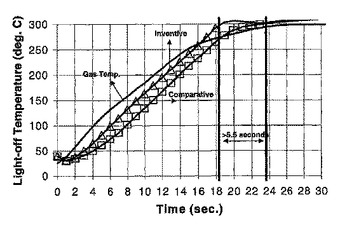 (もっと読む)
(もっと読む)
カチオン性ロジウム錯体の製造方法
本発明は、式:[Rh(配位子)m(ジオレフィン)]+X-(式中、配位子は、1個又は2個の連結リン原子を有する、エナンチオマー的に富化された有機化合物である)を有する非無定形カチオン性ロジウム錯体の製造及び単離方法を含む。 (もっと読む)
金属コアと有機二重コーティングとを有するナノ粒子の触媒としての利用、及び触媒として有用なナノ粒子
本発明は金属コア、より詳しくは白金族金属または白金族金属の合金を材料とする金属コアと、有機二重コーティングとを有するナノ粒子の触媒としての利用などに関するものであり、前記ナノ粒子は、少なくとも一つの白金族金属または白金族金属の合金を含む金属コアと、前記金属コアの表面に結合された分子から形成される第1有機コーティングと、前記第1有機コーティングの分子とは異なる分子であり、且つ前記第1有機コーティングの分子上にグラフトされた分子から形成される第2有機コーティングとを含む。 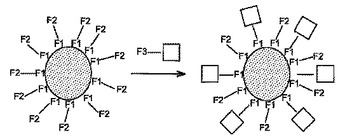 (もっと読む)
(もっと読む)
シアノピリジンを製造するための方法とそれに適した触媒
本発明は、メチルピリジンから、それらのアンモニアおよび酸素;ならびに、バナジウムおよびリン以外にさらなる遷移金属を含有するそのために適した触媒でのそれらの変換によるシアノピリジンを製造するための方法に関する。 (もっと読む)
マイクロカプセル化された触媒−配位子系、その調製方法および使用方法
マイクロカプセル化触媒−配位子系は、触媒および/または配位子を第1相(たとえば有機相)中に溶解または分散させ、第1相を第2の連続相(たとえば水相)中に分散させてエマルジョンを形成させ、分散された第1相と連続第2相との間の界面で1以上のマイクロカプセル壁形成物質を反応させて、分散された第1相核を封入するマイクロカプセルポリマーシェルを形成させ、第1相が触媒もしくは配位子だけを含む場合には、マイクロカプセルを触媒−配位子系の残りの配位子もしくは触媒成分で処理することにより調製される。触媒は好ましくは遷移金属触媒であり、配位子は好ましくは有機配位子である。 カプセル化触媒−配位子系は慣用の触媒反応に用いることができる。カプセル化触媒−配位子系は、反応媒体から回収され、リサイクルされてもよい。 (もっと読む)
光学活性なリン複素環二量体の製造方法
下記一般式(1)
【化1】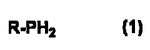
(Rは直鎖状、分岐状又は環状の炭素数2〜20のアルキル基を示す)
で表わされる一級ホスフィンに下記一般式(2)
【化2】
(Yはハロゲン原子または−Ots、−Otf、−Omsから選ばれる脱離基、nは3〜6の数を示す)で表わされる化合物を塩基の存在下で作用させ、続いて三水素化ホウ素、酸素又は硫黄を作用させて下記一般式(3)
【化3】
(Rは前記と同義、nは1〜4の数、Xは三水素化ホウ素基、酸素原子又は硫黄原子、===はXが三水素化ホウ素基の時は単結合、Xが酸素原子、硫黄原子の時は二重結合を示す)で表わされるリン複素環化合物を得、該化合物を二量化することにより下記一般式(4)
【化4】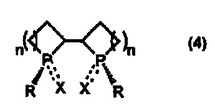
(R、n及びXは前記と同義)で表わされるリン複素環の二量体を得、続いて該リン複素環の二量体を脱酸素、脱硫黄、又は脱ボラン処理し、下記一般式(5)
【化5】
(R及びnは前記と同義)で表わされる光学活性なリン複素環の二量体を得る。
(もっと読む)
241 - 260 / 263
[ Back to top ]

