Fターム[4H039CA42]の内容
触媒を使用する低分子有機合成反応 (28,076) | 生成した置換基による反応の分類 (13,033) | 複素環化 (1,212)
Fターム[4H039CA42]に分類される特許
241 - 260 / 1,212
2−(1−フェニルエチル)イソインドリン−1−オン化合物を調製する方法
2−(1−フェニルエチル)イソインドリン−1−オン化合物を調製する方法が記載されている。 (もっと読む)
新規アミノアルコール誘導体塩、アミノアルコール誘導体塩構造を有する不斉有機分子触媒及び該不斉有機分子触媒を用いた光学活性化合物の製造方法
【課題】新規アミノアルコール誘導体塩、アミノアルコール誘導体塩構造を有する不斉有機分子触媒及び該不斉有機分子触媒を用いた光学活性化合物の製造方法を提供する。
【解決手段】下記式(1)で表わされる不斉有機分子触媒とする。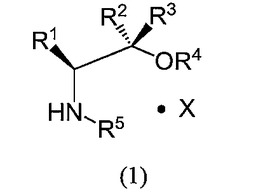
(式(1)中、R1はアルキル基又はアリール基であり、R2、R3はそれぞれ独立に水素原子又はアリール基であり、R4は水素原子又は一価の置換基であり、R5は水素原子又はアルキル基であり、Xは式(1)中のアミノアルコール誘導体骨格と塩を形成する有機酸を表わす。)
(もっと読む)
3,4−アルキレンジオキシチオフェン類の製造方法
【課題】機能性材料の原料または中間体として有用な3,4−アルキレンジオキシチオフェン類の高収率、高選択的な製造。
【解決手段】式(1)のチオフェン類と式(2)のジオール類とを、芳香族炭化水素溶媒中、スルホン酸触媒としてオルト位にアミノ基を有するベンゼンスルホン酸類、またはオルト位またはペリ位にアミノ基を有するナフタレンスルホン酸類の存在下に反応させる。
 (もっと読む)
(もっと読む)
(4−フルオロ−3−ピペリジン−4−イル−ベンジル)−カルバミン酸TERT−ブチルエステルの合成及びその中間体
本発明は、4−フルオロ−3−ピペリジン−4−イル−ベンジル)−カルバミン酸tert−ブチルエステル、式Iの化合物の製造のための改善された方法である。本発明は、3工程での式Iの化合物の合成方法に関し、該方法は、5−((tert−ブトキシカルボニル)アミノメチル)−2−フルオロベンゼンボロン酸(化合物11)の形成、Suzukiカップリング条件下で化合物11を反応させて(4−フルオロ−2−ピリジン−4−イル−ベンジル)−カルバミン酸tert−ブチルエステルを得ること、及び水素添加条件下で上述の生成物を選択的水素添加して化合物Iを得ることを含む。本発明はまた、中間体5−((tert−ブトキシカルボニル)アミノ−メチル)−2−フルオロベンゼンボロン酸(化合物11)、及び(4−フルオロ−2−ピリジン−4−イル−ベンジル)−カルバミン酸tert−ブチルエステル(化合物13)に関する。 (もっと読む)
N−アシルビフェニルアラニンを製造するための方法
薬学的に活性な化合物、特に、中性エンドペプチダーゼ(NEP)インヒビターの合成に有用な新規な方法、新規なプロセスステップおよび新規な中間体。 (もっと読む)
不均一系ロジウム金属触媒
下式(I)(式中、R1〜R8、X、A、m、n及びpは、本出願で定義されるものである)の繰り返しサブユニットを有する新規なポリマーロジウム触媒を説明し、そして更に、化学合成変換におけるそれらの触媒並びに前記触媒のための前駆体を使用する方法も説明する。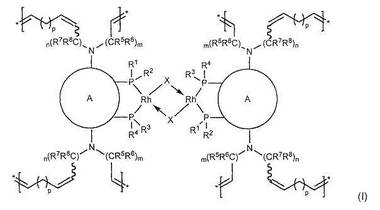
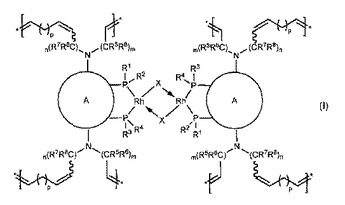 (もっと読む)
(もっと読む)
4−ヒドロキシベンゾチオフェン誘導体の製造方法
【課題】 医薬品の製造中間体として有用である4−ヒドロキシベンゾチオフェン誘導体を、工業的に簡便で有利な製造方法を用いることにより提供すること。
【解決手段】 3−(2−チエニル)アリルアルコールと一酸化炭素を、パラジウム触媒、リガンド、有機酸無水物及び塩基存在下、シクロカルボニル化反応を行いベンゾチオフェン骨格を構築し、当該中間体を単離又は単離することなく、その後加水分解反応することを特徴とする4−ヒドロキシベンゾチオフェン誘導体の工業的に有利な製造方法を解決手段とする。
(もっと読む)
光学活性な環状エーテル化合物の製法及びそれに用いる触媒
【課題】ジヒドロベンゾフランやクロマンなどの環状エーテルの酸素に隣接する2位の不斉炭素にカルボニル炭素が結合した化合物を高エナンチオ選択的に合成する。
【解決手段】N−スピロC2軸不斉四級アンモニウムヨージド又はP−スピロC2軸不斉四級ホスホニウムヨージドを触媒として、ケトフェノール化合物とヒドロペルオキシドとを反応させることにより、ケトフェノール化合物に対応するジヒドロベンゾフランを有する光学活性な環状エーテル化合物を良好な収率、鏡像体過剰率で得る。
【化1】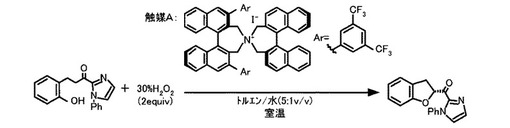 (もっと読む)
(もっと読む)
グルタミニルシクラーゼ阻害剤としてのヘテロ環式誘導体
本発明は、グルタミニルシクラーゼ(QC、EC 2.3.2.5)の阻害剤としての、式(I)の新規ピロリジン誘導体(式中、R1、R2、及びR3は、本明細書において定義されている)に関する。QCは、アンモニアの遊離下でのN-末端グルタミン残基のピログルタミン酸(5-オキソ-プロリル、pGlu*)への分子内環化、及び水の遊離下でのN-末端グルタミン酸残基のピログルタミン酸への分子内環化を触媒する。
【化1】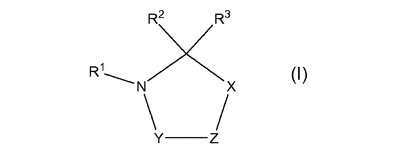 (もっと読む)
(もっと読む)
PLAベースポリマーの混合物の立体特異的なリサイクル方法
本発明はポリ乳酸(PLA)ポリマー混合物を立体特異的に化学的にリサイクルして、そのモノマーまたはその誘導体のうちの1種を再形成するための方法に関する。後者は伝統的なラクタート市場で使用できるし、またはPLAの合成のための原料として再使用できる。 (もっと読む)
α−カルボキサミド誘導体の製造方法
本出願は、式(I)のα-カルボキサミドピロリジン誘導体の製造方法を提供する:
【化1】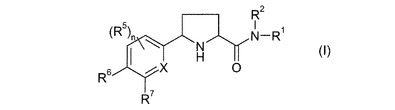
(式中、R1及びR2は、独立に、水素、C1-6アルキル又はC3-6シクロアルキルC1-6アルキルであり;又は、このようなR1及びR2は、それらが結合している窒素と共に、非置換3-、4-、5-又は6-員飽和環を形成でき;Xは、炭素又は窒素であり;nは0、1又は2であり、存在する場合には、各R5は、独立に、C1-3アルキル、ハロゲン、シアノ、ハロC1-3アルキル、ヒドロキシ、C1-3アルコキシ及びC1-3ハロアルコキシからなるリストから選択され;R6又はR7の一方は、-O-R8、-OCHR9R8、-NCH2R8又は-(CH2)2R8であり、R6又はR7の他方は、水素又はR5であり;R8は、フェニル環であり、又は該フェニル環は、独立にC1-3アルキル、ハロゲン、シアノ、ハロC1-3アルキル、ヒドロキシ、C1-3アルコキシ及びC1-3ハロアルコキシからなるリストから選択される1つ以上の基によって任意に置換され;R9は、水素又はC1-3アルキルである。)。
(もっと読む)
環状不飽和化合物の製造方法
【課題】α,β−不飽和カルボン酸と不飽和有機化合物とを用いて環状不飽和化合物を製造するに際し、収率の点で優れた、効率のよい環状不飽和化合物の製造方法を提供する。
【解決手段】α,β−不飽和カルボン酸と不飽和有機化合物とを触媒存在下に反応させて環状不飽和化合物を製造する方法であって、
該不飽和有機化合物は、下記一般式(1);
[化1]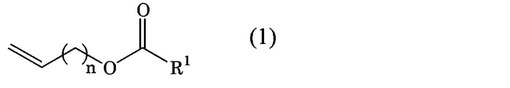
(式中、R1は、水素原子又は炭素数1〜30の有機基を表す。nは、0〜10の数を表す。)で表される化合物であり、
該製造方法は、カルボン酸系溶媒を用いる反応系又は無溶媒の反応系で行われることを特徴とする環状不飽和化合物の製造方法。
(もっと読む)
ナラトリプタンの合成方法
本発明は、ナラトリプタン又はその塩の製造方法に関し、この方法は:(a)式(3)の化合物を、式HCCRの化合物と反応させ(式中、Zは保護基であり、Yは脱離基であり、かつRは、トリアルキルシリル基、トリアルキルスタンニル基又はハロゲン化亜鉛(II)である。)、式(4)の化合物を得る工程;(b)式(4)の化合物を、式(5)の化合物へ変換する工程(式中、Z'は水素又はベンジル基である。);(c)式(5)の化合物をナラトリプタンへ変換する工程;並びに、(d)任意にナラトリプタンをその塩に変換する工程を含む。本発明は、新規化合物(3)及び(4)、並びにそれらの製造方法も提供する。
【化1】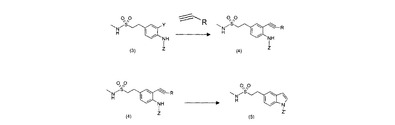 (もっと読む)
(もっと読む)
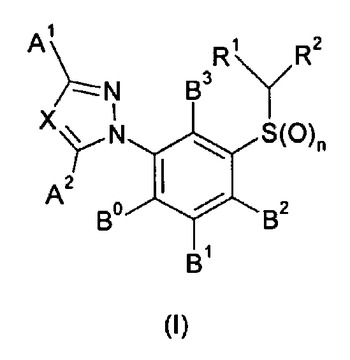
殺ダニ剤および殺虫剤としての3−トリアゾリルフェニル置換スルフィド誘導体
本発明は、式(I)〔式中、A1、A2、B0、B1、B2、B3、X、R1、R2およびnは、明細書中で定義されているのと同様に定義される〕で表される新規3−トリアゾリルフェニル置換スルフィド誘導体、害虫を防除するための殺ダニ剤および殺虫剤としてのそれらの使用、並びに、それらを調製する方法に関する。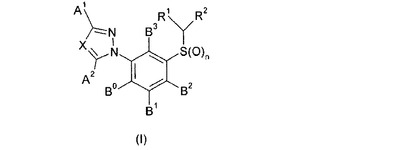
 (もっと読む)
(もっと読む)
ハロアルキルスルホンアニリド化合物の製造方法
【課題】除草剤として有用なハロアルキルスルホンアミド化合物の効率よい製造方法の提供。
【解決手段】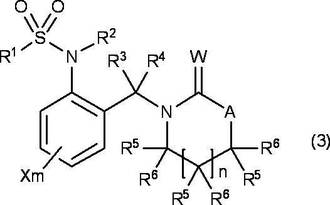
R1、R2、R3およびR4を含む、対応するベンジルアルコール化合物とR5およびR6を含む、対応する環状アミド化合物とを脱水反応させることによる式(3)で表されるハロアルキルスルホンアニリド化合物の製造方法。〔式中、R1、R2,R3およびR4は水素原子、アルキル基等を表し、Xは、アルキル基等を表し、mは、0から4の整数を表す。R5およびR6は、水素原子、アルキル基等を表し、Aは、酸素原子または硫黄原子を表し、nは、0、1または2を表す。〕
(もっと読む)
放射性ヨウ素化方法
本発明は、検査対象の生物学的標的化分子(BTM)を放射性ヨウ素で標識するための新規な方法を提供する。また、本方法を用いて製造される新規な放射性ヨウ素化BTM並びにかかる放射性ヨウ素化BTMを含む放射性医薬組成物も提供される。本発明はまた、本方法で有用な放射性ヨウ素化中間体並びにかかる放射性ヨウ素化BTMを用いるインビボイメージング方法も提供する。 (もっと読む)
ヒドロキシアルキルトリエチレンジアミン類の製造方法
【課題】発火の危険性が高い還元剤を用いることなく、簡便且つ安全にヒドロキシアルキルトリエチレンジアミン類を製造する方法を提供する。
【解決手段】下記式(3)
(式中、R1、R2は各々独立して、水素原子、メチル基、エチル基、又は直鎖状若しくは分枝状の炭素数3〜4のアルキル基を表す。m、nは各々独立して0〜2の整数を表す。ただし、1≦m+n<4である。)で示されるジヒドロキシアルキルピペラジン誘導体及び/又はその類似ジヒドロキシアルキルピペラジン誘導体を、酸触媒の存在下で分子内脱水縮合反応させる。
(もっと読む)
1,2,4−トリアゾール誘導体の製造方法
【課題】容易に入手可能な出発原料を利用し、安全性が高く安価な触媒の存在下、多様な1,2,4−トリアゾール誘導体を一工程で効率的に収率良く製造する方法の提供。
【解決手段】下記の反応式(7)及び(8)による方法。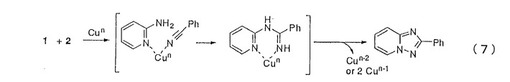
((1)は置換又は未置換の2−ピリジル基あるいは置換又は未置換の1−イソキノリル基を有するアミン、(2)は置換又は未置換のアリール基あるいは置換又は非置換の複素環基を有するニトリルを示す。)
((3)はアミジン誘導体、(4)はアルキル基あるいは置換又は非置換のアリール基あるいは置換又は非置換の複素環基を有するニトリルを示す。)
(もっと読む)
新規β−ラクタム合成法
【課題】簡便な操作で、しかも、収率よく、さらには良好な立体選択性をもって、アゼチジン-2-オン(β−ラクタム)骨格の4位にアルキリデン基を持っている有用なアゼチジン-2-オン誘導体を製造する方法の提供。
【解決手段】次の反応式(1)で示される環化異性化反応により、O-プロパルギルアリールアルドキシム化合物(1)を銅触媒などの触媒の作用によりβラクタム誘導体(2、2′)に変換する。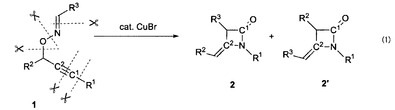
本反応は医薬品の合成中間体として有用な新規βラクタム化合物の高効率的合成法として期待できる。
(もっと読む)
環状カーボネートの製造方法
【課題】常温常圧付近の反応でも環状カーボネートを高収率で製造できる方法を提供する。
【解決手段】エポキシ化合物と二酸化炭素との反応により環状カーボネートを製造する方法であって、前記反応をインジウム系触媒及び有機リン系触媒の存在下で行うことを特徴とする環状カーボネートの製造方法。
(もっと読む)
241 - 260 / 1,212
[ Back to top ]