Fターム[4H045BA21]の内容
Fターム[4H045BA21]に分類される特許
81 - 100 / 123
オリゴペプチド
本発明の目的は、毛成長促進作用を有するオリゴペプチドを提供することである。本発明によれば、式(I):X1−X2−X3−X4−X5−X6−X7(式中、X1は、Serなどのアミノ酸残基を示し、X2はIleなどのアミノ酸残基を示し、X3はGluなどのアミノ酸残基を示し、X4はGlnなどのアミノ酸残基を示し、X5はSerなどのアミノ酸残基を示し、X6は、カルボニル基を含有する修飾基が結合しているCysのアミノ酸残基、またはカルボニル基を含有する修飾基が結合しているLysのアミノ酸残基を示し、そしてX7はGluまたはAlaなどのアミノ酸残基を示す)等で表されるオリゴペプチドが提供される。 (もっと読む)
アペリン組成物によって血管新生を調節するための方法
アペリン/APJシグナル伝達経路を阻害する組成物によって血管新生又は腫瘍形成を阻害する新規方法を提供する。また、アペリンポリペプチド又は低分子アゴニストを含有する組成物によって血管新生又は腫瘍形成を促進する方法も提供する。本発明はさらに、血管新生に影響を及ぼす治療薬を特定するための方法を提供する。 (もっと読む)
分子量マーカー
【目的】室温で安定なタンパク質分子量マーカーを提供する。
【解決手段】 (イ)分子量が5kDa乃至500kDaの範囲内であり、
(ロ)システイン残基を含まず、
(ハ)N末端又は/及びC末端にヒスチジンタグが融合されている
タンパク質を少なくとも2種以上含有し、かつ2種以上のタンパク質の分子量がそれぞれ異なることを特徴とするタンパク質分子量マーカー。
(もっと読む)
アレルゲンペプチド断片およびその利用
本願発明は、概して、アレルゲン特異的免疫療法のためのin vivo方法および組成物に関する。 この組成物は、アレルゲンのアミノ酸配列全体と共に、複数の連続する重複ペプチド断片を含んでいる。 (もっと読む)
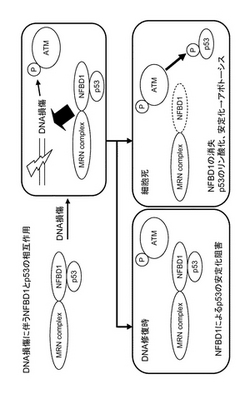
アポトーシスを促進又は抑制する化合物をスクリーニングする方法、アポトーシス抑制剤
【課題】 p53の不活性化の分子メカニズムを解明し、そして、そのメカニズムから導き出されたアポトーシスを促進又は抑制する化合物のスクリーニング方法を提供する。
【解決手段】 p53とNFBD1との相互作用を阻害する化合物を、アポトーシスを促進する化合物と判定する判定工程を備える、アポトーシスを促進する化合物のスクリーニング方法。
(もっと読む)
心臓血管障害で減少する分泌ポリペプチド種(チトトリオシダーゼ由来のフラグメント)
本発明は、配列番号3−4のアミノ酸配列を含む、新規ヒト分泌ポリペプチドを提供する。本発明のポリペプチドは、心臓血管障害の血漿において減少したレベルで循環している。本発明はまたポリペプチド、それらをコードするポリヌクレオチドおよび、これらのポリペプチドに特異的な抗体を含む組成物を提供する。また提供されるのは、このような組成物の製造法、および本発明の組成物の心臓血管障害の診断、予後および処置における使用法である。 (もっと読む)
レプリキンペプチド及びその使用
本発明は、高速複製及び高ひと死亡率に関係するペプチドの新規なクラス、並びに新興ウイルス疾患のワクチン及び治療を含んで成る疾患の診断、予防及び治療におけるこれらの使用、並びにペプチドの新規なクラス及び関連構造を同定するための方法を提供する。 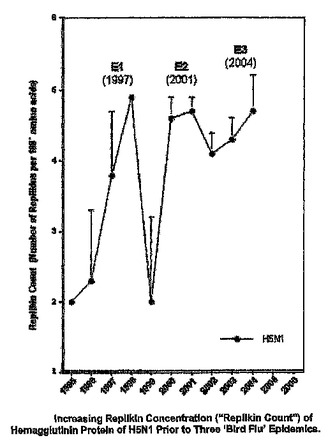 (もっと読む)
(もっと読む)
ヒトまたは動物の組織、血液もしくは体液中のヘプシジンをスクリーニングすることによる疾患の診断方法およびそのための治療的使用
本発明は、プロヘプシジンおよびそのフラグメントを含むヘプシジンタンパク質の非生理的レベルを特徴とする疾患状態を診断するための方法およびキットに関しており、この方法は、被験者から組織または液体サンプルを入手するステップと、このサンプルをヘプシジンタンパク質の中央部分またはC末端に対応するポリペプチドに特異的に結合するそれらの抗体またはそのフラグメントと接触させるステップと、抗体およびポリペプチドの結合に基づくアッセイを使用してヘプシジンレベルを定量するステップとを含み、ヘプシジンの非生理的レベルが疾患状態を表示する。本発明は、さらにまた例えばヘプシジンを過剰発現させる、またはダウンレギュレートするためのような遺伝子工学的アプローチにおける用途のための診断方法およびキットに関する。本発明は、さらにヘプシジンおよびヘプシジンのアゴニストもしくはアンタゴニストを用いた被験者の治療による特定の疾患の治療的処置に関する。 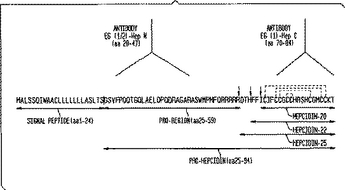 (もっと読む)
(もっと読む)
BMPまたはPTHを放出するマトリックスを用いた骨欠陥の局所治療
骨粗しょう症または骨嚢胞などの特定の骨欠陥の局所治療法は、PTHまたはBMP2またはBMP7を含む第一のドメイン、および共有的に架橋可能な基質ドメインを含む第二のドメインを含有する融合ペプチド;ならびに細胞増殖または内殖に適した生物分解性マトリックスを形成するのに適した材料を含む、配合物を局所投与する工程を含み、融合ペプチドはマトリックスに共有連結している。1つの態様において、マトリックスは、1以上の造影剤を含有し、そして好ましくは、増殖因子の非存在下で形成される。マトリックスは、Tarlov嚢胞、卵巣嚢胞、クモ膜嚢胞、動脈瘤性骨嚢胞、または肝嚢胞などの液体充満嚢胞の治療に使用可能である。 (もっと読む)
新規抗菌性ペプチド
本発明は、少なくとも1つのアミノ酸残基が、抗菌組成物の製造のための抗菌性ペプチドの有効性を改善するために置換されている、ペプチドの使用に関する。当該組成物は、微生物、例えば細菌、ウイルス、真菌、寄生虫及び酵母と闘うための、医薬組成物として使用することができる。  (もっと読む)
(もっと読む)
KDRおよびVEGF/KDR結合ペプチドならびに診断および治療におけるその使用
本発明は、KDRまたはVEGF/KDR複合体に対する結合ポリペプチドを提供する。それらは血管形成を治療、検出、単離または局在化することが好都合であるどのような場合でも多様な用途を有する。特に、KDRまたはVEGF/KDR複合体を高親和性(たとえばKD<1μMを有する)で結合可能な、合成され、単離されたポリペプチドが開示される。 (もっと読む)
心不全を診断するための特異性抗体
本発明は、心不全のin vitro診断に関する。更に特には、本発明は、プロBNP(1−108)のヒンジ領域R76S77の何れかの側に位置するペプチドドメインの特異的抗体に関する。特に、本発明は、前記抗体を取得する方法、及びBNP(1−76)及びBNP(77−108)以外の血中のプロBNP(1−108)を検出するための前記抗体の使用に関する。本発明は、血中プロBNP(1−108)の検出方法、試薬及びそのキットにも関する。 (もっと読む)
G型肝炎ウイルスおよびその分子クローニング
【課題】実質的に単離された形態の非A非B非C非D非E型肝炎ウイルス(HGV)を提供する。
【解決手段】実質的に単離された形態の非A非B非C非D非E型肝炎ウイルス(HGV)であって、ここでHGVが、(i)霊長類において伝染可能であり、(ii)A型肝炎ウイルス(HAV)、B型肝炎ウイルス(HBV)、C型肝炎ウイルス(HCV)、D型肝炎ウイルス(HDV)、およびE型肝炎ウイルス(HEV)と血清学的に異なり、(iii)フラビウイルス科のメンバーであり、そして(iv)複数の特定の配列、またはそれらの相補体として示される配列を有するポリヌクレオチドに対してストリンジェントな条件でハイブリダイズするポリヌクレオチドを含有することを特徴とする肝炎ウイルス。
(もっと読む)
胸腺特異的タンパク質
本発明は、ヒト胸腺から単離された84−アミノ酸ポリペプチドである新規な胸腺特異的ヒトタンパク質T101を提供する。完全T101ペプチドは、33−アミノ酸シグナルペプチド及び51−アミノ酸T101ペプチド配列を含有し、双方とも免疫刺激活性と阻害活性とを有する。修飾ペプチド類及び部分的T101ペプチド配列をも提供する。  (もっと読む)
(もっと読む)
プレプロインスリンの精製方法
本発明は、フロースルー式の陰イオン交換体の第一のクロマトグラフィー、それに続く吸着式の陽イオン交換体での第二のクロマトグラフィーによって、より高分子量の物質が、プレプロインスリン水溶液から分離されることによる、プレプロインスリンのクロマトグラフィー精製方法に関し、および、プレプロインスリンを生産する方法を含むインスリンの生産方法に関する。 (もっと読む)
結合分子
本発明は、側鎖サブユニットが天然および/または非天然のD−および/またはL−アミノ酸からなるポリペプチド鎖であり、そして側鎖サブユニットが支持体構造に共有結合で結合している、少なくとも一つの環状分子サブユニットおよび少なくとも二つの側鎖サブユニットの担体構造からなる結合分子に関する。 (もっと読む)
uPARターゲティング造影剤
本発明は、ウロキナーゼプラスミノーゲン活性化因子受容体(uPAR)の検出用の造影剤に関する。さらに具体的には、本発明は、造影性部分で標識された、uPARに結合するペプチドベクターを含む造影剤に関する。 (もっと読む)
リン脂質に対して親和性を有する標識ペプチドおよびその使用
本発明は、脂質ベクターの特異的認識のためのフッ素-18で標識したペプチドに関する。 (もっと読む)
合成ヘパリン結合成長因子類似体
本発明は、ペプチド鎖または複数の鎖が、ヘパリン結合成長因子レセプターを結合し、そして特に、疎水性リンカーでありうるリンカーによって、ヘパリン結合ドメインを含む非シグナル発生ペプチドに共有結合で結合されるものである、少なくとも1個のペプチド鎖、好ましくは2つの三官能アミノ酸残基から構成されるジペプチド分岐部位から分岐した2個のペプチド鎖を有する合成ヘパリン結合成長因子類似体を提供する。合成ヘパリン結合成長因子類似体は、医薬上の薬剤、可溶性生体薬剤として、または医療用デバイスのための表面被覆剤として有用である。 (もっと読む)
ネコおよびイヌのproBNPの決定
本発明は、ネコまたはイヌのproBNPまたはそのフラグメントを決定する方法であって、
下記のステップ:
−ネコまたはイヌのサンプルを提供するステップ、
−該サンプルを、ネコのproBNPまたはそのフラグメントを決定する場合に、ネコのproBNPのアミノ酸20〜42を含む領域および/またはアミノ酸57〜80を含む領域において少なくとも一つのエピトープと結合する少なくとも一つの抗体を接触させるステップ、またイヌのproBNPまたはそのフラグメントを決定する場合に、イヌのproBNPのアミノ酸20〜86を含む領域において少なくとも一つのエピトープに結合する少なくとも一つの抗体と接触させるステップ、
そして
−サンプル中に存在するネコまたはイヌのproBNPまたはそのフラグメントの存在および/または濃度を決定するステップ、
を含む方法。
(もっと読む)
81 - 100 / 123
[ Back to top ]